Крайова резекція нижньої щелепи: показання та протипоказання
Резюме. У статті представлено огляд літератури та власний досвід, присвячені проблемі крайової резекції нижньої щелепи у хворих зі злоякісними новоутвореннями порожнини рота. Описано сучасні погляди на механізм пухлинної інвазії нижньощелепної кістки та методи діагностики ураження нижньої щелепи. Розглянуто методики пластичного заміщення післяопераційних дефектів порожнини рота. Систематизовано показання та протипоказання до проведення крайової резекції нижньої щелепи.
Вступ
Сегментарна резекція нижньої щелепи (НЩ) протягом тривалого часу залишалася стандартом при хірургічному лікуванні хворих на рак порожнини рота (ПР). Навіть після того, як гістологічно було доведено, що у багатьох випадках резекція кістки не виправдана [1, 2], сегментарні та гемірезекції були оплотом хірургічного лікування пацієнтів, оскільки вони забезпечували добрий доступ та легке закриття післяопераційного дефекту [3].
Вивчення механізму пухлинної інвазії нижньощелепної кістки, досягнення променевих та клінічних методів діагностики ураження НЩ дозволили переглянути підходи до хірургічного лікування при раку ПР та запропонувати органозберігаючі резекції НЩ [3]. Резекцію НЩ зі збереженням неперервності (крайова резекція) виконують у хворих на рак слизової дна ПР, альвеолярного гребеня НЩ, щоки, ретромолярної ділянки і ротоглотки та язика [4–7]. Оскільки при крайовій резекції зберігаються неперервність НЩ і прикріплення м’язів, функціональні та косметичні порушення значно менші, ніж при сегментарній резекції [6]. Незважаючи на те що на сьогодні розроблено численні методики реконструкції НЩ [8–10], можливість її відновлення не є показанням до сегментарної резекції [6, 11].
Механізм пухлинної інвазії НЩ
До 70-х років минулого століття вважалося, що плоскоклітинний рак слизової оболонки ПР поширюється на нижньощелепну кістку через лімфатичну систему окістя язикової поверхні НЩ [12]. На сьогодні відомо, що поширення пухлинних клітин при злоякісних новоутвореннях слизової оболонки ПР відбувається шляхом прямого їх проникнення у губчату кістку в місці контакту пухлини з язиковою кортикальною пластинкою або альвеолярним гребенем НЩ (рис. 1) [13, 14]. Периневральне проростання новоутворення уздовж нижньощелепного нерва відбувається лише на пізніх стадіях пухлинного процесу [15]. Враховуючи вищевикладене, J. Brown вважає обґрунтованим проведення крайової резекції НЩ, при цьому включення судинно-нервового пучка в блок видалених тканин не є обов’язковим [14].
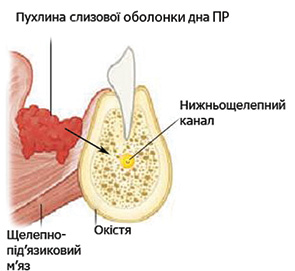
Існують два різні гістологічні типи пухлинної інвазії НЩ. Перший називається «інфільтративний», або «інвазивний». При цьому варіанті пухлина руйнує губчатий шар кістки без утворення проміжного шару сполучної тканини, визначається незначна активність остеокластів. Рентгенологічна картина характеризується деструкцією кісткової тканини з нечіткими контурами. Другий тип називається «ерозивний». У даному випадку пухлина поширюється на кістку з утворенням проміжного шару сполучної тканини, активні остеокласти сприяють формуванню різкої межі між пухлиною і кісткою. Рентгенологічна картина характеризується деструкцією кісткової тканини з чіткими межами зони ураження [11, 15, 16]. R. Wong та співавтори порівняли безрецидивну виживаність пацієнтів з різними типами пухлинної інвазії НЩ. У хворих з ерозивною інвазією НЩ 3-річна безрецидивна виживаність становила 73%, у пацієнтів з інфільтративною інвазією — 30%. Це означає, що гістологічні типи інвазії НЩ відображають біологічну агресивність пухлини [17].
Після проведеної променевої терапії картина пухлинної інвазії НЩ суттєво змінюється, оскільки опромінення порушує періостальне кровопостачання, та окістя втрачає бар’єрні властивості до інвазії пухлини. Гістологічне дослідження декальцинованих зразків НЩ показало, що деструкція у неопроміненій кістці зазвичай відбувається у одному місці, а у опроміненій часто визначалися мультицентрові вогнища деструкції. Крім того, показано, що 53% неопромінених нижньощелепних кісток реагували на прилеглу пухлину, збільшуючи відкладення нової кісткової тканини на межі з новоутворенням. Цей захисний механізм був значно порушений у опроміненій кістці. Наведені факти спонукали більшість хірургів, які спеціалізуються на голові та шиї, розглядати сегментарну резекцію НЩ як основний метод лікування рецидивів пухлини після променевої терапії [11, 18].
Променеві методи діагностики ураження НЩ
Дотепер немає єдиної точки зору щодо оптимального методу або поєднання діагностичних методів, які б з високою точністю дозволили визначити інвазію пухлини слизової оболонки ПР у нижньощелепну кістку [19, 20]. Для визначення ураження НЩ застосовують наступні методи променевої діагностики:
- ортопантомографію (ОПГ);
- комп’ютерну томографію (КТ);
- магнітно-резонансну томографію (МРТ);
- остеосцинтиграфію;
- позитронно-емісійну томографію з КТ-скануванням (ПЕТ-КТ).
ОПГ відіграє важливу роль у виявленні інвазії раку ПР в нижньощелепну кістку, особливо у визначенні вертикального розповсюдження пухлинного процесу, що є визначальним при виборі між крайовою та сегментарною резекцією НЩ [20]. S. Hong та співавтори, оцінюючи вертикальну інвазію пухлини, вважають за доцільне паралельно з ОПГ виконувати інтраоральні дентальні рентгенограми, оскільки вони дозволяють візуалізувати досить тонкі анатомічні деталі [21]. Проте ОПГ та інтраоральні рентгенограми не є методами ранньої діагностики ураження кістки тому, що кісткові зміни виявляють при втраті 30% кальцію. Крім того, при ОПГ достатньо важко оцінити зміни фронтального відділу НЩ у зв’язку з накладанням шийних хребців [19].
КТ є стандартним методом діагностики злоякісних новоутворень голови та шиї. Спіральна КТ з контрастуванням є чутливим методом оцінки плоскоклітинного раку ПР з точки зору його розмірів, локалізації, поширення на нижньощелепну кістку, м’які тканини та регіонарні лімфатичні вузли [22]. Слід відзначити низьку специфічність спіральної КТ у пацієнтів із металевими пломбами, імплантатами або ортопедичними конструкціями в ПР через наявність артефактів [23, 24]. Перспективні результати виявлення пухлинної інвазії НЩ продемонстровано при застосуванні конусно-променевої КТ, особливо при оцінці щічної та язикової кортикальної пластинки [11, 25, 26]. Конусно-променева КТ пацієнта з пухлиною ретромолярної ділянки, що поширюється на гілку НЩ, представлено на рис. 2.
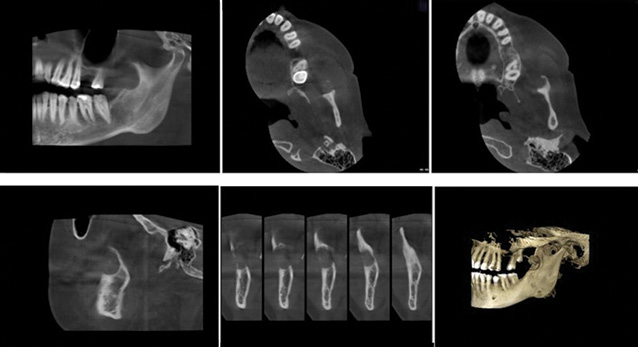
МРТ має переваги перед КТ при візуалізації м’яких тканин щелепно-лицьової ділянки та кістково-мозкових просторів НЩ [27]. Разом з тим МРТ недостатньо для оцінки кортикальної пластинки нижньощелепної кістки [28]. M. van den Brekel та співавтори досліджували ураження НЩ при раку слизової оболонки ПР з використанням ОПГ, КТ та МРТ. Автори виявили, що МРТ має найвищу чутливість (94%), але низьку специфічність (73%). Крім того, на думку авторів, при МРТ часто переоцінюють ступінь пухлинної інвазії НЩ. ОПГ і КТ, навпаки, мали нижчу чутливість (63 та 64% відповідно) та вищу специфічність (90 та 89% відповідно) [29]. A. Imaizumi та співавтори також повідомляють про низьку специфічність МРТ у виявленні пухлинної інвазії кортикального шару НЩ та нижньощелепного каналу [30]. E. van Cann та D. Gu, навпаки, відзначають низьку чутливість та високу специфічність МРТ [19, 31]. Хибнопозитивні результати МРТ при діагностиці ураження НЩ можуть бути викликані запальними захворюваннями періодонта, а також набряком або склерозом тканин унаслідок реакції на первинну пухлину [32].
Остеосцинтиграфію розглядають як один із найбільш надійних методів діагностики ураження НЩ, хоча результати досліджень неоднозначні. E. van Cann та співавтори повідомили про високу чутливість (100%) та низьку специфічність (56,5%) однофотонної емісійної комп’ютерної томографії (ОФЕКТ) [19]. Хибнопозитивні результати остеосцинтиграфії пов’язані з підвищеним накопиченням радіофармпрепарату в ділянці реактивно зміненого окістя або запальних процесів нижньощелепної кістки [19, 33]. R. Schimming та співавтори відзначають високу чутливість (100%) та високу специфічність (91,6%) ОФЕКТ [34].
У останні роки з’являються дослідження, присвячені вивченню ролі ПЕТ-КТ при діагностиці ураження НЩ. E. Babin та співавтори повідомляють про високу чутливість (100%) та високу специфічність (85%) цього методу [35]. Оскільки жоден із методів променевої діагностики самостійно не забезпечує 100% точності у визначенні інвазії НЩ, D. Gu та співавтори вважають, що надійна оцінка ураження нижньощелепної кістки може бути зроблена при комплексному аналізі КТ, МРТ та ПЕТ-КТ [31]. Інші автори для визначення пухлинної інвазії НЩ рекомендують поєднання КТ та ОФЕКТ або МРТ та ОФЕКТ [19]. Результати досліджень чутливості та специфічності різних методів променевої діагностики при оцінці пухлинної інвазії НЩ наведено в таблиці [19, 20, 22, 23, 27, 30, 31].
Таблиця. Результати досліджень чутливості та специфічності різних методів променевої діагностики при оцінці пухлинної інвазії НЩ
| Автор | ОПГ | КТ | МРТ | Остеосцинтиграфія | ||||
| Чутливість, % | Специфічність, % | Чутливість, % | Специфічність, % | Чутливість, % | Специфічність, % | Чутливість, % | Специфічність, % | |
| J. Brown та співавтори (1994) [14] | 76 | 93 | 53 | 90 | 100 | 92 | 95 | 72 |
| C. Acton та співавтори (2000) [22] | 80 | 72 | – | – | – | – | – | – |
| R. Schimming та співавтори (2000) [34] | 85 | 89,5 | – | – | – | – | 100 | 91,6 |
| A. Lane та співавтори (2000) [23] | – | – | 61 | 88 | – | – | – | – |
| A. Bolzoni та співавтори (2004) [27] | – | – | – | – | 93 | 93 | – | – |
| L. Rao та співавтори (2004) [3] | 92 | 88 | – | – | – | – | – | – |
| A. Imaizumi та співавтори (2006) [30] | – | – | 100 | 88 | 96 | 54 | – | – |
| E. van Cann та співавтори (2008) [19] | 61,4 | 60,9 | 58,1 | 95,7 | 62,8 | 100 | 100 | 56,5 |
| D. Gu та співавтори (2010) [31] | – | – | 41,7 | 100 | 58,3 | 97,1 | – | – |
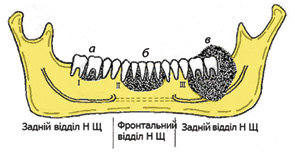
Базуючись на оцінці променевих методів діагностики, виділяють 3 ступені пухлинної інвазії нижньощелепної кістки (рис. 3). Крім того, променеві методи дозволяють визначити тип пухлинної інвазії НЩ (ерозивний або інфільтративний). K. Tei та співавтори рекомендують проводити крайову резекцію у пацієнтів з ерозивною або інфільтративною інвазією НЩ у межах альвеолярного гребеня (ступінь I) та у хворих з ерозивною інвазією, яка не поширюється до нижньощелепного каналу (ступінь II) [5]. Інші дослідники також рекомендують проведення крайової резекції при поверхневій інвазії НЩ [6] та при пухлинній інвазії, яка не поширюється до рівня нижньощелепного каналу [36].
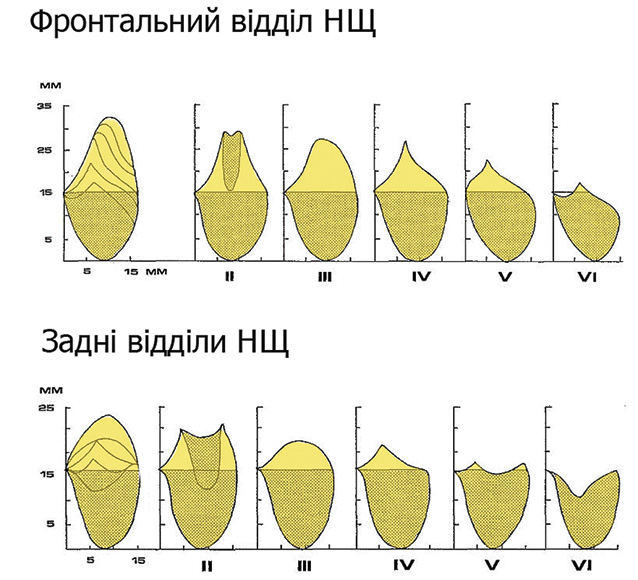
ОПГ та конусно-променева КТ дозволяють оцінити ступінь атрофії НЩ у пацієнтів із повною втратою зубів, що визначає можливість проведення крайової резекції у цієї категорії хворих. J. Brown та співавтори при плануванні типу резекції НЩ у пацієнтів з адентією використали класифікацію атрофії беззубих щелеп за J. Cawood та R. Howell (рис. 4). Автори вважають, що при виявленні променевими методами пухлинної інвазії нижньощелепної кістки, крайова резекція можлива при II класі атрофії НЩ, при III–VI класі перевагу слід віддати сегментарній резекції [37].
Клінічні методи діагностики ураження НЩ
Клінічний огляд дозволяє оцінити розповсюдження пухлини у ПР. У випадках, коли злоякісні новоутворення поширюються ближче 1 см до альвеолярного гребеня НЩ або безпосередньо до нього прилягають без глибокої інфільтрації тканин дна ПР та щільного прилягання пухлини до тіла НЩ з обох боків, виконують крайову резекцію [5, 6, 38]. Передопераційна оцінка ураження НЩ, на думку більшості дослідників, має включати клінічні дані та результати променевих методів діагностики. J. Werning та співавтори ретроспективно проаналізували результати обстеження та лікування 222 хворих на рак ПР. Автори виявили, що клінічна оцінка пухлинної інвазії НЩ має вищу чутливість, ніж променеві методи діагностики. Проте променеві методи оцінки були більш конкретними та мали вищий показник надійності. Поєднання клінічних та променевих методів діагностики ураження НЩ є більш точним, ніж використання їх самостійно [39].
Проведено ряд досліджень, які вивчали можливості інтраопераційних клінічних методів діагностики пухлинної інвазії НЩ. J. Brown та співавтори, аналізуючи декілька методів оцінки ураження нижньощелепної кістки, виявили, що інтраопераційне гістологічне дослідження заморожених зрізів окістя є точним провісником пухлинної інвазії НЩ. Із 35 проаналізованих випадків лише у одному автори відзначили хибний результат [40]. M. Pandey та співавтори вважають, що у всіх випадках плоскоклітинного раку ПР можна визначити ураження НЩ, використовуючи клінічний огляд, променеві методи діагностики та інтраопераційне гістологічне дослідження окістя. Проте дослідники застерігають, що забір окістя під час операції призводить до порушення принципів абластики [41]. L. Forrest та співавтори повідомили про результати інтраопераційного дослідження заморожених зрізів губчатої кістки, узятої з країв резекції НЩ. У 30 пацієнтів досліджено 61 край резекції. Чутливість методу становила 88,9%, специфічність — 100% [42]. Теоретично даний метод може бути використаний для визначення типу резекції НЩ. Якщо вискрібання губчатої кістки з країв резекції дасть позитивний результат, слід виконати сегментарну резекцію. Про цю техніку не повідомляли в літературі, але вона, на нашу думку, заслуговує на подальше вивчення. L. Oxford та Y. Ducic досліджували заморожені зрізи кортикальної кістки, узятої з країв резекції НЩ. Чутливість методу становила 89%, специфічність — 100% [43].
Отже, поєднання клінічних та променевих методів діагностики дозволяє визначити:
- розповсюдження пухлини в ПР або ротоглотки;
- зв’язок пухлини з альвеолярним гребенем та тілом або гілкою НЩ;
- ступінь пухлинної інвазії нижньощелепної кістки;
- тип пухлинної інвазії (ерозивний або інфільтративний);
- ступінь атрофії НЩ у пацієнтів з адентією;
- гістологічну чистоту країв резекції НЩ.
Саме ці чинники є визначальними при формуванні показань до крайової резекції НЩ.
Хірургічна техніка виконання крайової резекції та методики пластичного заміщення післяопераційних дефектів ПР
Крайову резекцію НЩ виконано у 28 хворих на рак ПР. У 14 (50%) пацієнтів встановлено II (T2N0M0), у 11 (39,3%) — III (T2N1M0, T3N0–1M0), у 3 (10,7%) — IV (T4N1–2M0) стадію пухлинного процесу. Для визначення пухлинної інвазії НЩ усім пацієнтам проводили ОПГ та спіральну КТ з контрастуванням. У випадках розбіжності між даними клінічних та променевих методів діагностики додатково виконували конусно-променеву КТ або ПЕТ-КТ. У всіх хворих крайову резекцію НЩ проведено після променевої терапії у сумарній вогнищевій дозі 40–56 Гр.
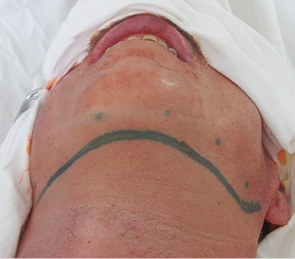
При локалізації пухлини у ділянці передніх та передньо-бічних відділів ПР доступ здійснювали шляхом викроювання козиркового клаптя (рис. 5, 6). Слизову оболонку розсікали по верхньому краю альвеолярного гребеня (якщо процес локалізувався у ділянці слизової оболонки дна ПР) або по перехідній складці (якщо процес локалізувався на слизовій оболонці альвеолярного гребеня). М’які тканини підборіддя та щоки разом з окістям зміщували вниз до нижньої межі крайової резекції НЩ. При викроюванні козиркового клаптя намагалися максимально зберегти окістя НЩ нижче лінії крайової резекції. Збереження окістя є важливим чинником профілактики післяопераційних ускладнень [44]. Далі електроножем намічали лінію резекції м’яких тканин, відступивши від країв пухлини на 1,5 см (рис. 7).
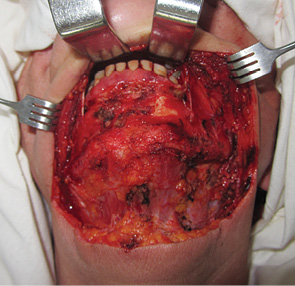
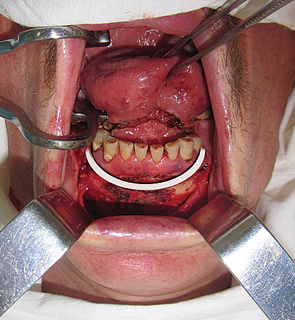
Досягнення гістологічної чистоти країв резекції м’яких тканин є надзвичайно важливим, оскільки саме цей фактор, а не інвазія НЩ та тип її резекції впливає на частоту місцевих рецидивів та виживаність пацієнтів [45]. Кістковою пилкою проводили крайову резекцію, відступивши від країв пухлинної інвазії НЩ як мінімум на 1 см. Лінію остеотомії формували дугоподібно без уступів та кутів, оскільки вони є точками концентрації сил при навантаженні, що може призвести до перелому НЩ. Резектовану частину щелепи мобілізували та по раніше намічених межах проводили електрорезекцію м’яких тканин. Одним блоком препарат видаляли (рис. 8, 9).
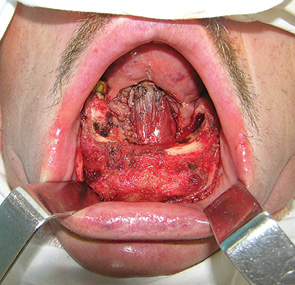
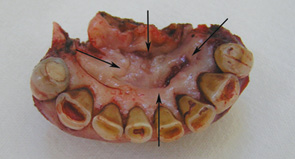
Слід зазначити, що мінімальна висота нижнього сегмента кістки після крайової резекції має залишатися не менше 10 мм, аби уникнути перелому НЩ [46]. Для пластичного заміщення післяопераційних дефектів передніх та передньо-бічних відділів ПР застосовували місцеві тканини, розщеплений автодерматотрансплантат, підгіоїдний шкірно-м’язовий клапоть, носогубний шкірно-жировий клапоть з нижньою основою (рис. 10, 11) та вільний променевий клапоть передпліччя.
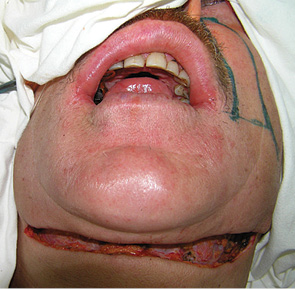
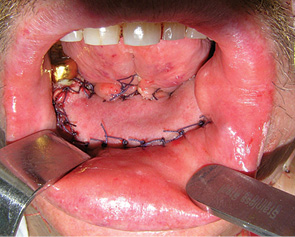
При локалізації пухлини у ділянці бічних та задніх відділів ПР або ротоглотки доступ здійснювали шляхом викроювання нижнього щічного клаптя. Етапи проведення крайової резекції гілки НЩ у пацієнта з новоутворенням ретромолярної ділянки представлено на рис. 12–15. Для пластичного усунення післяопераційних дефектів бічних відділів ПР використовували місцеві тканини, носогубний шкірно-жировий клапоть з нижньою основою та вільний променевий клапоть передпліччя (рис. 16). Для заміщення післяопераційних дефектів задніх відділів ПР та ротоглотки застосовували місцеві тканини, палатинальний (рис. 17, 18) та фасціально-апоневротичний скронево-тім’яний клапті.
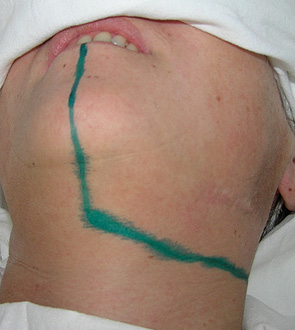
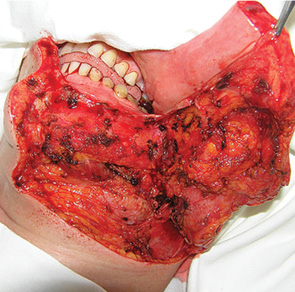
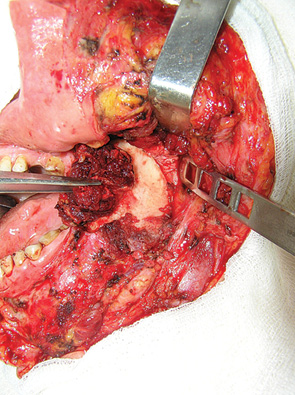
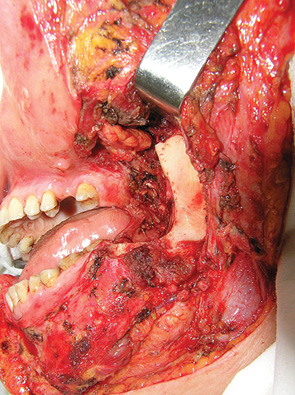
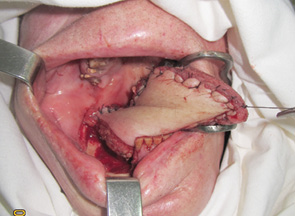
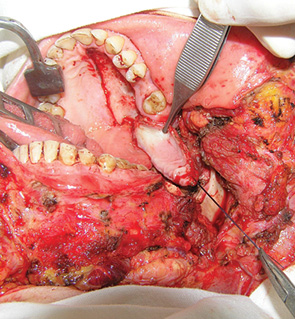
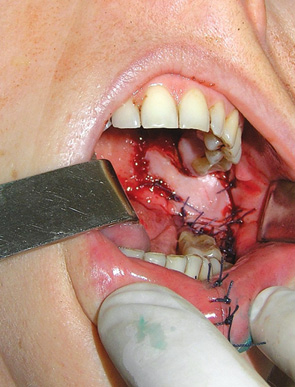
Збереження окістя та покриття резектованого фрагмента кістки добре васкуляризованими тканинами автотрансплантата сприяє профілактиці остеомієліту НЩ. Формування дугоподібної лінії остеотомії та збереження не менше 10 мм нижнього сегмента кістки після крайової резекції дозволяє знизити ризик перелому НЩ. Так, перелом НЩ у наших спостереженнях відзначено лише у 1 (3,6%) хворого. Остеомієліту та остеорадіонекрозу НЩ ми не діагностували.
ВИСНОВКИ
Крайова резекція НЩ є радикальним органозберігаючим оперативним втручанням у хворих на рак ПР та ротоглотки.
Показання до виконання крайової резекції:
- поширення злоякісних новоутворень ПР ближче 1 см до альвеолярного гребеня НЩ за відсутності пухлинної інвазії нижньощелепної кістки за даними променевих методів діагностики (у пацієнтів зі збереженим зубним рядом та хворих з адентією за умови початкової атрофії нижньощелепної кістки (II–III клас за класифікацією J. Cawood та R. Howell));
- ерозивна або інфільтративна інвазія НЩ у межах альвеолярного гребеня та ерозивна інвазія альвеолярного гребеня і тіла НЩ, яка не поширюється до рівня нижньощелепного каналу (у пацієнтів зі збереженим зубним рядом);
- ерозивна інвазія НЩ у межах альвеолярного гребеня у пацієнтів з адентією за умови початкової атрофії нижньощелепної кістки (II клас за класифікацією J. Cawood та R. Howell).
Протипоказання до виконання крайової резекції:
- злоякісні новоутворення ПР з глибокою інфільтрацією тканин дна ПР та щільним приляганням пухлини до тіла НЩ з обох боків;
- пухлинна інвазія НЩ, що поширюється до рівня нижньощелепного каналу або виходить за його межі;
- виражена атрофія НЩ у пацієнтів з адентією (IV–VI клас за класифікацією J. Cawood та R. Howell);
- рецидиви пухлини після раніше проведеної крайової резекції НЩ.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Marchetta F.C., Sako K., Murphy J.B. (1971) The periosteum of the mandible and intraoral carcinoma. Am. J. Surg., 122: 711–713.
2. Ord R.A., Sarmadi M., Papdimitrou J. (1997) A comparison of segmental and marginal bony resection for oral squamous cell carcinoma involving the mandible. J. Oral. Maxillofac. Surg., 55: 470–477.
3. Rao L.P., Shukla M., Sharma V. et al. (2012) Mandibular conservation in oral cancer. Surgical Oncology. 21: 109–118.
4. Muños Guerra M.F., Naval Gias L., Campo F.R. et al. (2003) Marginal and segmental mandibulectomy in patients with oral cancer: a statistical analysis of 106 cases. J. Oral. Maxillofac. Surg., 61(11): 1289–1296.
5. Tei K., Totsuka Y., Iizuka T. et al. (2004) Marginal resection for carcinoma of the mandibular alveolus and gingival where radiologically detected bone defects do not extend beyond the mandibular canal. J. Oral. Maxillofac. Surg., 62: 834–839.
6. Patbak K.A., Sbab C. (2009) Marginal mandibulectomy: 11 years of institutional experience. J. Oral. Maxillofac. Surg., 67: 962–967.
7. Pascoal M.N., Cbagas J.F., Alonso N. et al. (2007) Marginal mandibulectomy in the surgical treatment of tonsil and retromolar trigone tumours. Rev. Bras. Otorrinolaringol., 73(2): 180–184.
8. Rana M., Warraich R., Kokemüller H. et al. (2011) Reconstruction of mandibular defects-clinical retrospective research over a 10-year period. Head & Neck Oncol., 3: 23.
9. Goh B., Lee S., Tideman H. (2008) Mandibular reconstruction in adults: a review. J. Oral. Maxillofac. Surg., 37: 597–605.
10. Herford A.S. (2009) RhBMP-2 as an option for reconstructing mandibular continuity defects. J. Oral. Maxillofac. Surg., 67(12): 2679–2684.
11. Genden E.M., Rinaldo A., Jacobson A. et al. (2005) Management of mandibular invasion: When is a marginal mandibulectomy appropriate? Oral Oncology, 41: 777–782.
12. Ward G.E., Robben J.O. (1951) The composite operation for radical neck dissection and removal of cancer of the mouth. Cancer, 4: 98–109.
13. Brown J.S., Browne R.M. (1995) Factors influencing the pattern of invasion of the mandible by oral squamous cell carcinoma. Int. J. Oral. Maxillofac. Surg., 24: 417–426.
14. Brown J. (2003) Mechanisms of cancer invasion of the mandible. Curr. Opin. Otolaryngol. Head Neck Surg., 11: 96–102.
15. Slootweg P.J., Muller H. (1989) Mandibular invasion by oral squamous cell carcinoma. J. Craniomaxillofac. Surg., 17: 69–74.
16. Muller H., Slootweg P.J. (1990) Mandibular invasion by oral squamous cell carcinoma. Clinical aspects. J. Craniomaxillofac. Surg., 18: 80–84.
17. Wong R.J., Keel S.B., Glynn R.J. et al. (2000) Histological pattern of mandibular invasion by oral squamous cell carcinoma. Laryngoscope, 110: 65–72.
18. McGregor A.D., McDonald D.G. (1988) Routes of entry of squamous cell carcinoma to the mandible. Head Neck Surg., 10: 294–301.
19. Van Can E.M., Koole R., Oyen W.J.G. (2008) Assessment of mandibular invasion of squamous cell carcinoma by various modes of imaging: constructing a diagnostic algorithm. Int. J. Oral. Maxillofac. Surg., 37: 535–541.
20. Rao L.P., Das S.R., Mathews A. et al. (2000) Mandibular invasion in oral squamous cell carcinoma: investigation by clinical examination and orthopantomogram. Int. J. Oral. Maxillofac. Surg., 33: 454–457.
21. Hong S.X., Cha I.H., Lee E.W. et al. (2001) Mandibular invasion of lower gingival carcinoma in the molar region: its clinical implications on the surgical management. Int. J. Oral. Maxillofac. Surg., 30(2): 130–138.
22. Acton C.H., Layt C., Gwynne R. et al. (2000) Investigative modalities of mandibular invasion by squamous cell carcinoma. Laryngoscope, 110: 2050–2055.
23. Lane A.P., Buckmire R.A., Mukherji S.K. et al. (2000) Use of computed tomography in the assessment of mandibular invasion in carcinoma of the retromolar trigone. Otolaryngol. Head Neck Surg., 122: 113–117.
24. Imola M.J., Gapany M., Grund F. et al. (2001) Technetium 99m single positron emission computed tomography scanning for assessing mandible invasion in oral cavity cancer. Laryngoscope, 111: 372–381.
25. Brokenbrough J.M., Petruzzelli G.J., Lomasney L. (2003) DentaScan as an accurate method of predicting mandibular invasion in patients with squamous cell carcinoma of the oral cavity. Arch. Otolaryngol. Head Neck Surg., 129(1): 113–117.
26. Momin M.A., Okochi K., Watanabe H. et al. (2009) Diagnostic accuracy of cone-beam CT in the assessment of mandibular invasion of lower gingival carcinoma: comparison with conventional panoramic radiography. Eur. J. Radiol., 72(1): 75–81.
27. Bolzoni A., Cappiello J., Piazza C. et al. (2004) Diagnostic accuracy of magnetic resonance imaging in the assessment of mandibular involvement in oral-oropharyngeal squamous cell carcinoma: a prospective study. Arch. Otolaryngol. Head Neck Surg., 130(7): 837–843.
28. Tsue T.T., McCulloch T.M., Girod D.A. et al. (1994) Predictors of carcinomatous invasion of the mandible. Head Neck., 16: 116–126.
29. van den Brekel M.W., Runne R.V., Smeele L.E. et al. (1998) Assessment of tumour invasion into the mandible: the value of different imaging techniques. Eur. Radiol., 8: 1552–1557.
30. Imaizumi A., Yoshino N., Yamada I. et al. (2006) A potential pitfall of MR imaging for assessing mandibular invasion of squamous cell carcinoma in the oral cavity. AJNR Am. J. Neuroradiol., 27(1): 114–122.
31. Gu D.H., Yoon D.Y., Park C.H. et al. (2010) CT, MR, (18) F-FDGPET/CT, and their combined use for the assessment of mandibular invasion by squamous cell carcinomas of the oral cavity. Acta. Radiol., 51(10): 1111–1119.
32. Crecco M., Vidiri A., Angelone M.L. et al. (1999) Retromolar trigone tumors: evaluation by magnetic resonance imaging and correlation with pathological data. Eur. J. Radiol., 32: 182–188.
33. Tsuchimochi M., Katagiri M., Maeda K. et al. (1999) Autoradiographic evaluation of 99mTc-methylene diphosphonate accumulation in oral cancer invading the mandible. J. Oral. Maxillofac. Surg., 57(3): 245–254.
34. Schimming R., Juengling F.D., Lauer G. et al. (2000) Computeraided 3-D 99mTc-DPD-SPECT reconstruction to assess mandibular invasion by intraoral squamous cell carcinoma: diagnostic improvement or not? J. Craniomaxillofac. Surg., 28(6): 325–330.
35. Babin E., Desmonts C., Hamon M. et al. (2008) PET/CT for assessing mandibular invasion by intraoral squamous cell carcinomas. Clin. Otolaryngol., 33(1): 47–51.
36. Vicente J.C., Recio O.R., Pendas S.L. et al. (2001) Oral squamous cell carcinoma of the mandibular region: a survival study. Head Neck, 23: 536.
37. Brown J., Chatterjee R., Lowe D. et al. (2005) A new guide to mandibular resection for oral squamous cell carcinoma based on the Cawood and Howell classification of the mandible. Intr. J. Oral. Maxillofac. Surg., 34: 834–839.
38. Shaha A.R. (1992) Marginal mandibulectomy for carcinoma of the floor of the mouth. J. Surg. Oncol., 49: 116–119.
39. Werning J.W., Byers R.M., Novas M.A. et al. (2001) Preoperative assessment for and outcomes of mandibular conservation surgery. Head Neck, 23: 1024–1030.
40. Brown J.S., Griffith J.F., Phelps P.D. et al. (1994) A comparison of different imaging modalities and direct inspection after periosteal stripping in predicting the invasion of the mandible by oral squamous cell carcinoma. Br. J. Oral. Maxillofac. Surg., 32: 347–359.
41. Pandey M., Rao L.P., Das S.R. (2009) Predictors of mandibular involvement in cancers of the oromandibular region. J. Oral. Maxillofac. Surg., 67: 1069–1073.
42. Forrest L.A., Schuller D.E., Lucas J.G. et al. (1995) Rapid analysis of mandibular margins. Laryngoscope, 105: 475–477.
43. Oxford L.E., Ducic Y. (2006) Intraoperative evaluation of cortical bony margins with frozen-section analysis. Otolaryngol. Head Neck Surg., 134(1): 138–141.
44. Petruzzelli G.J., Knight F.K., Vandevender D. et al. (2003) Posterior marginal mandibulectomy in the management of cancer of the oral cavity and oropharynx. Otolaryngol. Head Neck Surg., 129: 713–719.
45. O’Brien C.J., Adams J.R., McNeil E.B. et al. (2003) Influence of bone invasion and extent of mandibular resection on local control of cancers of the oral cavity and oropharynx. Int. J. Oral. Maxillofac. Surg., 32: 492–497.
46. Barttelbort S.W., Ariyan S. (1993) Mandible preservation with oral cavity carcinoma: rim mandibulectomy with sagittal mandibulectomy. Am. J. Surg., 166: 411.
Краевая резекция нижней челюсти: показания и противопоказания
2Национальный институт рака, Киев
Резюме. В статье представлены обзор литературы и собственный опыт, посвященные проблеме краевой резекции нижней челюсти у больных со злокачественными новообразованиями полости рта. Описаны современные взгляды на механизм опухолевой инвазии нижнечелюстной кости и методы диагностики поражения нижней челюсти. Рассмотрены методики пластического замещения послеоперационных дефектов полости рта. Систематизированы показания и противопоказания к проведению краевой резекции нижней челюсти.
Ключевые слова: краевая резекция, нижняя челюсть.
Marginal mandibulectomy: indications and contraindications
2National Cancer Institute, Kyiv
Summary. This article provides an overview of the literature and personal experience on the problem of marginal mandibulectomy in patients with malignant tumors of the oral cavity. The study presents current views on the mechanism of tumor invasion of the mandible bone and diagnostic methods of the mandible lesions. The methods of plastic replacement of postoperative defects of the oral cavity are reviewed. Systematized indications and contraindications for the marginal mandibulectomy.
Key words: marginal mandibulectomy, mandible.














Leave a comment