Расширенная гистерэктомия (С1 nerve-sparing dissection) у больных инвазивным раком шейки матки
Свинцицкий В.С.1, Воробьева Л.И.1, Стаховский Э.А.1, Лигирда Н.Ф.1, Дерменжи Т.В.2, Яцина А.И.1
Резюме. Хирургические операции по поводу рака шейки матки (РШМ) часто сопровождаются нарушением нормального функционирования мочевыделительной и половой систем. Основной причиной этих нарушений является операционная травма элементов тазовой вегетативной нервной системы, иннервирующих органы мочевой и половой систем, располагающихся в непосредственной близости от области вмешательства. Цель исследования — обоснование внедрения расширенной гистерэктомии (С1 nerve-sparing dissection) в клиническую практику лечения больных инфильтративным РШМ и оценка непосредственных результатов терапии. В отделении онкогинекологии Национального института рака с 2012 г. проведено хирургическое лечение 20 больных инфильтративным РШМ с применением расширенной гистерэктомии (С1 nerve-sparing dissection) (средний возраст пациенток — 32,7±4,9 года). Первый опыт применения в клинической практике для лечения больных инфильтративным РШМ расширенной гистерэктомии (С1nerve-sparing dissection) дает обнадеживающие результаты по уменьшению количества ранних послеоперационных осложнений со стороны мочеполовой системы, однако для оценки отдаленных результатов лечения, количества осложнений, качества жизни этой категории больных необходим дальнейший набор клинического материала, выполнение рандомизированных исследований в специализированных центрах.
Введение
Рак шейки матки (РШМ) занимает 2-е место в структуре онкогинекологической патологии. По данным ВОЗ, ежегодно в мире выявляют около 500 тыс. новых случаев заболевания. Каждый год 250 тыс. женщин умирают от РШМ. В Украине в 2011 г. стандартизованный показатель заболеваемости составил 15,4 на 100 тыс. женского населения, стандартизованный показатель смертности — 5,5 на 100 тыс., всего заболели 5344 женщины, умерли 2194 [1]. В последнее время наблюдается рост заболеваемости РШМ среди молодых женщин в возрастной группе до 40 лет [1, 4].
История хирургического лечения инвазивного РШМ насчитывает более 100 лет. В настоящее время наиболее распространенным и часто применяемым в мире хирургическим вмешательством при инвазивном РШМ IВ–IIВ стадии является расширенная экстирпация матки с придатками (или без придатков), известная как операция Вертгейма. Безусловно, за столетие, прошедшее с момента ее выполнения Эрнстом Вертгеймом, она претерпела значительные технические изменения, но приоритет ее разработки, несомненно, принадлежит этому выдающемуся австрийскому гинекологу.
В США хирургические вмешательства, выполняемые при инвазивном РШМ, классифицированы по 5 типам [2, 8, 23]. Экстрафасциальная экстирпация матки обозначена как операция I типа. Модифицированная радикальная экстирпация матки (II тип) включает удаление медиальной половины кардинальных и крестцово-маточных связок, радикальная экстирпация матки (III тип), описанная J. Meigs (1944, 1951), предусматривает удаление большей части кардинальных, крестцово-маточных связок, верхней трети влагалища и лимфатических узлов таза [2, 8]. В США при инвазивном РШМ чаще всего выполняют именно эту операцию [8, 25]. При расширенной радикальной экстирпации матки IV типа удаляют периуретральные ткани, резецируют верхнюю пузырную артерию и ¾ влагалища. Операция V типа, которая является частичной экзентерацией, предусматривает удаление дистальных отделов мочеточников и мочевого пузыря, ее проводят при прорастании опухоли в мочевой пузырь (рис. 1, 2).
![Рис. 1. Классификация M. Piver, F. Ratledge, J. Smith (горизонтальный срез таза) [23]](http://www.clinicaloncology.com.ua/uploads/2013/07/wpid-259_1_fmt.jpeg)

В 2007 г. на согласительной конференции в Киото D. Querleu, C.P. Morrow предложена новая классификация гистерэктомий, выполняемых у больных инвазивным РШМ [13] (рис. 3).
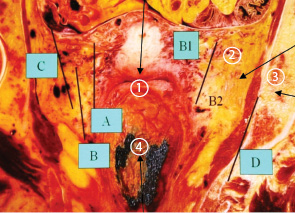
Тип А. Экстрафасциальная гистерэктомия.
При выполнении гистерэктомии типа А:
- латеральный параметрий удаляют до мочеточников;
- мочеточник не туннелируется;
- передний и задний параметрий не удаляют;
- сосуды удаляют максимально близко к матке;
- практически не выполняют резекцию влагалища.
Тип В. При гистерэктомии типа В проводят:
- туннелирование мочеточника;
- частичную резекцию крестцово-маточной связки;
- частичную резекцию пузырно-маточной связки;
- резекцию парацервикальной связки на уровне мочеточникового туннеля.
Тип С. При гистерэктомии типа С проводят:
- удаление латерального параметрия до подвздошных сосудов;
- резекцию переднего параметрия (пузырно-маточной связки) до мочевого пузыря;
- резекцию заднего параметрия (крестцово-маточной связки) до прямой кишки;
- полную мобилизацию мочеточника.
Тип С1 (с сохранением тазового нерва):
- латеральный параметрий — сохранение висцерального нерва (splanchnic nerves);
- вентральный параметрий — сохранение пузырной ветви тазового сплетения;
- дорсальный параметрий — сохранение гипогастрального нерва (рис. 4).
На рис. 4 показаны уровни пересечения кардинальной связки при различных типах гистерэктомий.
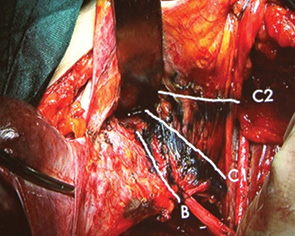
Тип С2 (без сохранения тазового нерва):
- латеральный параметрий — пересечение висцерального нерва (splanchnic nerves);
- вентральный параметрий — пересечение пузырной ветви тазового сплетения;
- дорсальный параметрий — все ветви гипогастрального нерва пересечены.
На рис. 5 представлен макропрепарат удаленной матки после расширенной гистерэктомии Тип С2.

Тип D. Латеральная параметрэктомия.
При гистерэктомии типа D:
- линия резекции проходит между внутренней запирательной мышцей и пояснично-крестцовым нервным сплетением;
- выполняют резекцию внутренних подвздошных артерий и вен (рис. 6–9).
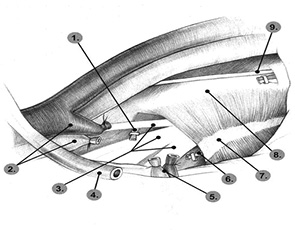
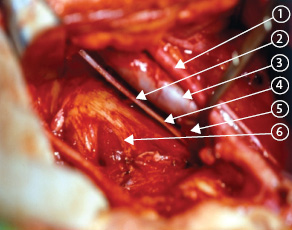
Хирургические операции по поводу РШМ часто сопровождаются нарушением нормального функционирования мочевыделительной и половой систем. Частота расстройств мочеиспускания после операции на шейке матки составляет 78%, частота половых расстройств — до 90%. Основной вероятной причиной этих нарушений является операционная травма элементов тазовой вегетативной нервной системы, иннервирующих органы мочевой и половой систем и располагающихся в непосредственной близости от области вмешательства [3, 9, 10]. Выделяют 5 основных элементов тазовой вегетативной нервной системы: непарное верхнее гипогастральное сплетение, парные гипогастральные нервы и нижние гипогастральные сплетения.
Основными симптомами нарушения функции мочевой системы являются задержка мочеиспускания или недержание мочи разной степени выраженности [3, 11]. Нарушения функций половой системы у женщин проявляются в виде расстройств вагинальной секреции и ритмичных сокращений влагалища [3, 12, 14]. В соответствии с «травматической» теорией причин возникновения послеоперационных мочеполовых расстройств, начиная со средины прошлого столетия, ведется разработка и внедрение в клиническую практику концепции нервосохраняющих операций, то есть комплекса хирургических приемов, направленных на сохранение нервных структур таза [5, 6, 16, 17]. К настоящему моменту многочисленными исследованиями подтверждено, что сохранение тазовых вегетативных нервов позволяет существенно уменьшить количество послеоперационных мочеполовых расстройств.
Высокая частота мочевых функциональных нарушений и урологических осложнений при расширенной гистерэктомии дала толчок для развития этого типа вмешательства со снижением радикальности операций. Щадящая техника диссекции дистальной части парацервикса (nerve-sparing dissection) позволяет избегать подобного риска, повышая частоту урологических осложнений. Функциональное сохранение тазовой иннервации возможно у больных онкогинекологического профиля при трансвагинальном удалении матки с выполнением микрохирургической диссекции, при внедрении лапароскопической техники, а также лапаротомном доступе, что является идеальным подходом.
Следует отметить, что большая часть исследований, касающихся нервосохраняющих операций в хирургии шейки матки, выполнена зарубежными авторами [24, 26, 27]. К сожалению, в нашей стране нервосохраняющая техника начинает развиваться только сейчас и только в специализированных крупных центрах. Не продемонстрирована возможность проведения нервосохраняющих операций в зависимости от стадии процесса, локализации опухоли, вида операции, вариантной анатомии тазовых вегетативных нервов и ряда других критериев. Как следствие, не сформулированы четкие показания к выполнению нервосохраняющих операций.
Материалы и методы
С целью изучения эффективности применения нервосохраняющей гистерэктомии в лечении больных инфильтративным РШМ в отделении онкогинекологии Национального института рака проведено исследование по определению показаний к применению этой методики, а также оценены ближайших и отдаленных результаты лечения.
С 2012 по 2013 г. в отделении выполнены расширенные гистерэктомии у 40 больных инфильтративным РШМ (средний возраст пациенток — 32,7±4,9 года), из них у 20 больных (I группа) — с сохранением тазового нервного сплетения и 20 — по стандартной методике, без сохранения тазового нервного сплетения (II группа, контрольная). Прогностические показатели тождественны в исследуемых группах. В табл. 1 представлено распределение больных инфильтративным РШМ в исследуемых группах по основным прогностическим критериям.
Таблица 1 Распределение больных инфильтративным раком шейки матки в исследуемых группах по основным прогностическим факторам
| Клиническая характеристика | Группа больных | ||
| основная (I) | контрольная (II) | ||
| Возраст больных, годы | 20–30 | 6 | 5 |
| 31–40 | 10 | 11 | |
| 40–50 | 4 | – | |
| 51–60 | 4 | ||
| Стадия РШМ | IBpT1bN0M0 | 13 | 8 |
| IIApT2aN0M0 | 7 | 12 | |
| Гистологический тип | Плоскоклеточный | 12 | 19 |
| Аденокарцинома | 2 | 1 | |
| Гистологическаядифференциация | GX | 2 | 2 |
| G1 | 5 | 7 | |
| G2 | 5 | 4 | |
| G3 | 8 | 7 | |
Для статистического анализа результатов использовали пакет прикладных программ STАTІSTІCA 5,0 for Wіndows, Stat Soft, Іnc., USA, параметрические и непараметрические критерии (t-критерий Стьюдента и критерий Манна — Уитни) для оценки расхождений показателей в группах.
Результаты и обсуждения
Концепция нервосохраняющей расширенной гистерэктомии заключается в выделении нижнего гипогастрального сплетения, его маточной ветви, отсечении только маточной ветви, что и позволяет сохранить гипогастральный (подчревный) нерв, тазовый чревный нерв и пузырную ветвь нижнего гипогастрального сплетения [18, 20]. Однако до недавнего времени топографическая анатомия нижнего гипогастрального сплетения, состоящего из подчревного нерва, тазового чревного нерва, маточной ветви и пузырной ветви изучена недостаточно для выполнения нервосохраняющих хирургических вмешательств [18, 19]. Чаще всего во время проведения расширенной гистерэктомии повреждается гипогастральный нерв при выделении маточно-крестцовых и ректо-вагинальных связок; тазовый чревный нерв — при выделении глубокой маточной вены кардинальной связки и пузырная ветвь верхнего гипогастрального сплетения — при перевязке и выделении паравагинальной клетчатки [18, 20]. Поэтому некоторые исследователи предлагают проводить менее радикальные операции, при которых уровень травматизма данных нервов ниже, чем при классической расширенной гистерэктомии. Однако, чтобы свести к минимуму эти нарушения, японские онкогинекологи начали сохранять тазовые нервы, иннервирующие мочевой пузырь и прямую кишку во время расширенной гистерэктомии приблизительно с 1950 г. [18, 19]. Н. Окабаяши предложил методику расширенной гистерэктомии, включающую разделение заднего листка пузырно-маточной связки, что дает возможность отделить только маточную ветвь нижнего гипогастрального сплетения и сохранить иннервацию мочевого пузыря, а также избежать грубых нарушений его сократительной функции в послеоперационный период [18, 20]. Без расслоения заднего листка пузырно-маточной связки трудно визуализировать нижнее гипогастральное сплетение, особенно во время стандартной операции Вертгейма, при которой это не проводится.
Есть много опубликованных результатов изучения нервосохраняющей хирургии с применением различных хирургических методик. Однако рандомизированных исследований по сравнению типа С1 и С2 расширенной гистерэктомии не проводили, что затрудняет анализ опубликованных данных по нарушению функций мочевыделительной и половой систем в результате хирургического лечения [18, 20].
Матка иннервируется частью plexus hypogastricus inferior, которая образует так называемое сплетение Рейна (передняя часть нижнего края plexus hypogastricus inferior). Сплетение Рейна некоторые авторы именуют plexus uterovaginalis, s. uterinus magnus.
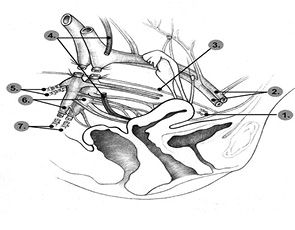
Сплетение Рейна образует ветви: 1) от передних корешков II, III и IV сакральных нервов за счет отходящих от последних 4–6 волоконец nn. erigentes (nn. erigentes называют также nn. pelvici). Последние соединяются по пути с ветками от сакральных ганглий симпатического пограничного ствола: 2) от сакрального и копчикового отдела пограничного симпатического ствола; 3) через plexus hypogastricus inferior, от поясничных симпатических стволов, а также от X, XI, XII грудных нервов; 4) от plexus haemorrhoidales inferior, отходящего от plexus mesogasrica inferior, чем устанавливается функциональная зависимость между генитальным аппаратом и прямой кишкой (рис. 10, 11).
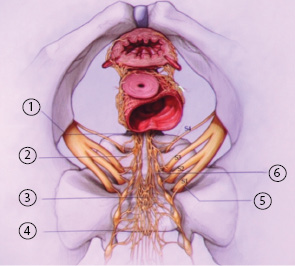
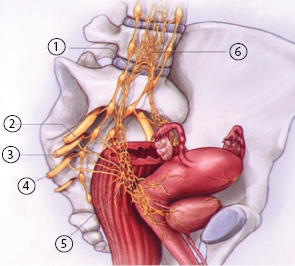
Тазовое сплетение содержит в себе в основном симпатические волокна, а также волокна nn. pelvici и поэтому является смешанным сплетением. Таким образом, матка, влагалище, мочевой пузырь и прямая кишка иннервируются двигательными и чувствительными нервами как симпатической, так и парасимпатической автономной нервной системы. Симпатические волокна, отходящие от Тh11–L2, образуют верхнее гипогастральное сплетение. Парасимпатические волокна, отходящие от S2–S4 к стенкам таза, образуют тазовый чревный нерв. Эти волокна сливаются и образуют нижнее подчревное (гипогастральное) сплетение, ветви которого иннервируют матку и мочевой пузырь.
Топографическая анатомия нижнего гипогастрального (тазового) сплетения, включающего подчревный нерв, тазовый внутренностный нерв, пузырную ветвь, маточную ветвь этого сплетения, достаточно сложна, и ее не так легко визуализировать во время расширенной гистерэктомии, особенно недостаточно квалифицированному хирургу. Для того чтобы сохранить тазовый чревный (внутренностный) нерв, необходимо визуализировать нижнее подчревное сплетение, для этого следует досконально знать анатомию таза и параметральной области (топографию глубоких вен матки) [18, 20, 21]. Кроме того, очень важным является знание анатомии пузырно-маточной связки, особенно заднего ее листка. Необходимо также владеть определенными хирургическими технологиями по бережной препарации этих тканей с целью визуализации структуры нижнего гипогастрального сплетения.
Анатомия пузырно-маточной связки (передний/задний листок) представлена на рис. 12.
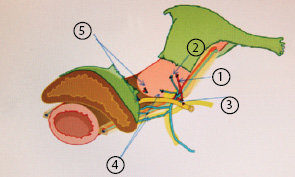
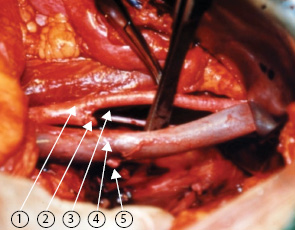
В переднем листке пузырно-маточной связки визуализируются: маточная артерия; поверхностные вены матки; мочеточниковая ветвь маточной артерии; верхние пузырные вены, впадающие в поверхностные маточные вены; шеечно-пузырные сосуды. Представлен этап выделения кровеносных сосудов из соединительной ткани переднего листка пузырно-маточной связки.
В заднем листке пузырно-маточной связки обычно локализуются 2 основные пузырные вены, впадающие в глубокие вены матки (рис. 13).
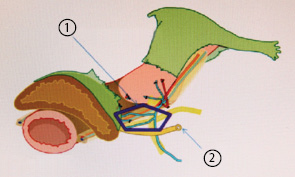
Рассечение этих вен дает доступ к нижнему гипогастральному сплетению, позволяющий отделить только маточную ветвь от этого сплетения. После выделения паравагинальной клетчатки визуализируется Т-образная плоскость гипогастрального нерва, пересекают только его маточную ветвь, выделяют вагинальную манжетку, удаляют матку (рис. 14, 15).
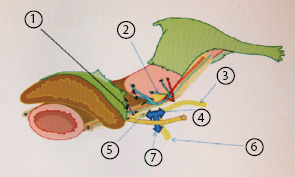
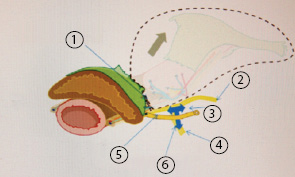
На схематических изображениях (см. рис. 14, 15) представлена расширенная гистерэктомия (С1 nerve-sparing dissection) у больных инвазивным РШМ (Textbook of gynaecological oncology, 2012) [18].
Ниже представлены этапы нервосохраняющей гистерэктомии, которую проводили в онкогинекологическом отделении Национального института рака:
Отделение маточной ветви от нижнего гипогастрального сплетения. Ниже подчревного нерва пузырную ветвь нижнего гипогастрального сплетения отделяют от кровеносных сосудов паравагинальной клетчатки (рис. 16, 17). Выделение происходит между пузырной ветвью и кровеносными сосудами паравагинальной клетчатки в соединительной ткани между плоскостью тазового нерва и шейкой/верхней частью влагалища на уровне гипогастрального нерва с вентральной стороны и глубоких маточных вен с дорсальной. Со стороны матки маточную ветвь нижнего гипогастрального сплетения зажимают, отсекают после появления ощущения, напоминающего разрыв натянутой струны.
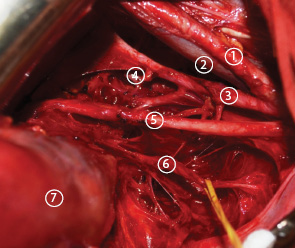
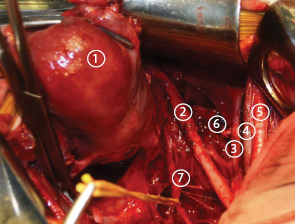
Диссекция ректовагинальной связки позволяет отделить кровеносные сосуды паравагинальной ткани от Т-образной плоскости нерва. После отделения ректовагинальной связки от верхней части влагалища, пузырной ветви нижнего гипогастрального сплетения, формирующего Т-образную плоскость нерва, поэтапно производят пересечение и лигирование кровеносных сосудов паравагинальной ткани дистально вдоль влагалища ниже уровня поражения шейки матки (рис. 18, 19).
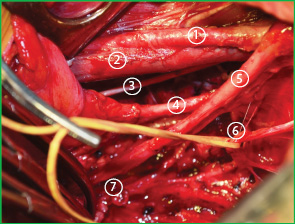
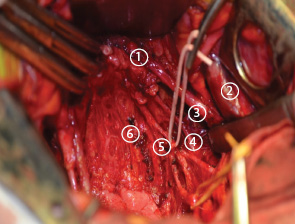
При отсепаровке мочевого пузыря от стенки влагалища и паракольпальной клетчатки до уровня пересечения влагалища нужна предельная осторожность, чтобы не пересечь остающиеся висцеральные нервные волокна.
Формирование защитной стенки для юкставезикальной порции мочеточника стенками прямой кишки и мочевого пузыря. Перегиб мочеточника – одна из наиболее серьезных послеоперационных проблем, которая может приводить к гидроуретеру и гидронефрозу с возможным нарушением функции почки. Для предупреждения погружения юкставезикального отдела мочеточника в таз и перегиба его накладывают два шва латерально от мочеточника между наружной стенкой прямой кишки и мочевым пузырем.
Функцию нижних мочевыводящих путей у больных в исследуемых группах после выполнения радикальной гистерэктомии с сохранением тазового нервного сплетения у больных инфильтративным РШМ изучали при помощи цистоманометрии на уродинамической стойке УРО-ПРО по стандартной методике.
В ранний послеоперационный период у всех больных проводили оценку сократительной функции мочевого пузыря.
Цистометрия (цистоманометрия) — это регистрация изменений внутрипузырного давления в процессе его заполнения и при мочеиспускании. Цистометрия отражает: 1) сенсорные характеристики мочевого пузыря; 2) адаптационные свойства детрузора (то есть его способность к сохранению низкого внутрипузырного давления при заполнении и отсутствие незаторможенных сокращений; 3) динамику внутрипузырного давления при мочеиспускании [7, 15, 22].
Растяжимость мочевого пузыря (комплаентность) рассматривали как изменение детрузорного давления при определенном изменении объема заполнения. Высчитывали по формуле:
К=∆V/∆Р,
где К – растяжимость стенки мочевого пузыря (в мл/см вод. ст.);
∆V — изменение объема;
∆Р – изменение давления детрузора в момент изменения объема.
При сохранении нервного тазового сплетения растяжимость стенки мочевого пузыря была более 10 мл/см вод. ст. при объеме до 100 мл и более 25 мл/см вод. ст. при объеме до 500 мл (рис. 20, 21).
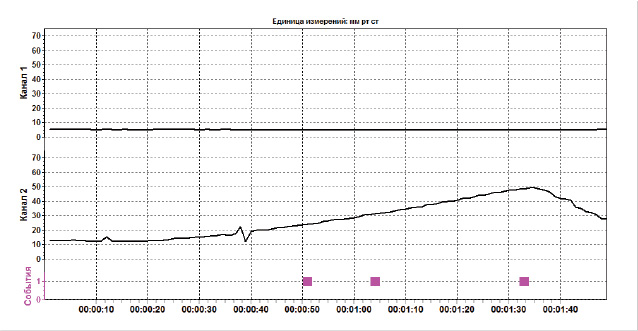
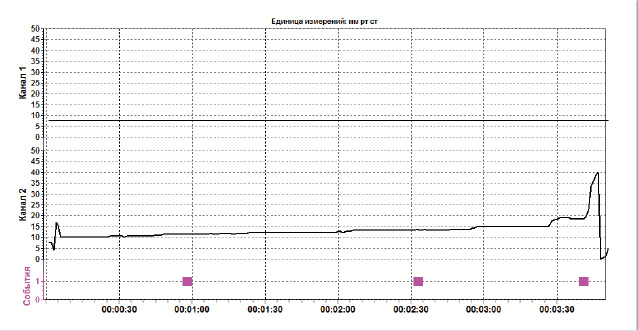
После выполнения нервосохраняющей гистерэктомии у 80% больных I группы сократительная функция мочевого пузыря восстанавливалась полностью на 2-е–3-и сутки после оперативного вмешательства, а в контрольной группе — только в 20% случаев. Через 7 сут после расширенной гистерэктомии у всех больных I группы возобновлялась нормальная функция нижних мочевыводящих путей, у пациенток II группы восстановительный период длился от 7 до 21 сут (табл. 2).
Таблица 2. Восстановление функции нижних мочевыводящих путей у больных в исследуемых группах
| Восстановление функции нижних мочевыводящих путей, сут | Исследование (I группа) | Контроль (II группа) |
| 1–3 | 16 | 3 |
| 4–7 | 4 | 1 |
| 8–14 | – | 7 |
| 15–21 | – | 9 |
Проведенное исследование по внедрению расширенной гистерэктомии (С1 nerve-sparing dissection) в клиническую практику лечения больных инфильтративным РШМ дает обнадеживающие результаты по уменьшению количества ранних послеоперационных осложнений со стороны мочеполовой системы, однако для оценки отдаленных результатов лечения, количества осложнений, качества жизни этой категории больных необходим дальнейший сбор клинического материала, проведение рандомизированных исследований в специализированных центрах.
Выводы
1. Выполнение радикальной нервосохраняющей гистерэктомии у больных инфильтративным РШМ позволяет в послеоперационный период сохранить функцию нижних мочевыводящих путей: показатели цистоманометрии у них на 60% выше, чем у пациенток контрольной группы.
2. Нервсохраняющую РГЭ не следует проводить у пациенток с РШМ стадии IIB по FIGO (Féderation Internationale de Gynécologie et d’Obstétrique), так как нижнее гипогастральное сплетение расположено очень близко к очагу поражения.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Рак в Україні, 2010–2011. Захворюваність, смертність, показники діяльності онкологічної служби (2012) Бюл. Нац. канцер-реєстру України, 13: 124.
2. Вернер П., Зедерль Ю. (1960) Радикальная операция Вертгейма при раке шейки матки. Медицина, Москва: 74 с.
3. Беляев А.М., Манихас Г.М., Доманский А.А., Братов О.З. (2010) Возможность выполнения нервосохраняющих операций у различных категорий больных раком прямой кишки. Биомедицинский журн. Medline.ru, 11: 597–610.
4. Воробйова Л.І. (2010) Сучасні підходи до діагностики, лікування і профілактики раку шийки матки. Жіночий лікар, 5: 18–21.
5. Воробьев Г.И., Царьков П.В., Подмаренкова Л.Ф. и др. (2005) Нервосохраняющие операции в хирургии рака прямой кишки. Хирургия. Журнал им. Н.И. Пирогова, 8: 22–28.
6. Беляев А.М., Доманский А.А., Захаренко А.А. и др. (2011) Результаты применения нервосохраняющих операций в хирургии осложненного рака прямой кишки. Биомедицинский журн. Medline.ru, 12: 495–510.
7. Атдуев В.А., Строганов А.Б., Любарская Ю.О. и др. (2009) Результаты создания артифициального мочевого пузыря после радикальной цистэктомии у больных раком мочевого пузыря. Саратовский научный медицинский журнал, 5(4): 615–619.
8. Кузнецов В.В., Лебедев А.И., Морхов К.Ю., Грицай А.Н. (2002) Хирургия инвазивного рака шейки матки. Практическая онкология, 3(3): 178−182.
9. Levickis J., Boucher N.R., Parys B.T. et al. (1995) Bladder and erectile disfunction before and after rectal surgery for cancer. Br. J. Urol., 76: 752–756.
10. Hanna N.N., Guillem J., Dosoretz A. et al. (2002) Intraoperative parasympathetic nerve stimulation with tumescence monitoring during total mesorectal excision for rectal cancer. J. Am. Coll. Surg., 195: 506–512.
11. Havenga K., Maas C.P., DeRuiter M.C. et al. (2000) Avoiding long-term disturbance to bladder and sexual function in pelvic surgery, particularly with rectal cancer. Semin. Surg. Oncol., 18: 235–243.
12. Maurer C.A., Z’graggen K., Renzulli P. et al. (2001) Total mesorectal excision preserves male genital function compared with conventional rectal cancer surgery. Brit. J. Surg., 88: 1501–05.
13. Querleu D., Morrow C.P. (2008) Classification of radical hysterectomy. Lancet Oncol., 9: 297–303.
14. Daniels I.R., Woodward S., Taylor F.G. et al. (2006) Female urogenital dysfunction following total mesorectal excision for rectal cancer. World J. Surg. Oncol., 4: 6.
15. Lowery A.E., Holland J.C. (2011) Screening cancer patients for distress guidelines for routine implementation. Community oncology, 8(11): 502–505.
16. Moriya Y., Sugihara K., Akasu T. et al. (1995) Nerve-sparing surgery with lateral node dissection for advanced lower rectal сancer. Eur. J. Cancer, 31A: 1229–32.
17. Maas C.P., Moriya Y., Steup W.H. et al. (2000) A prospective study on radical and nerve-preserving surgery for rectal cancer in the Netherlands. Eur. J. Surg. Oncol., 26(8): 751–757.
18. Ayhan A., Reed N., Gultekin M., Dursun P. (2012) Textbook of gynaecological oncology, 106: 635–639.
19. Dursun P., Ayhan A., Kuscu E. (2009) Nerve-sparing radical hysterectomy for cervical carcinoma. Crit. Rev. Oncol. Hematol., 70(3): 195–205.
20. Fujii S., Takakura K., Matsumura N. et al. (2007) Anatomic identification and functional outcomes of the nerve sparing Okabayashi radical hysterectomy. Gynecol. Oncol., 107: 4–13.
21. Fujii S. (2008) Anatomic identification of nerve-sparing radical hysterectomy: A step-by-step procedure. Gynecol. Oncol., 111: S33–S41.
22. Chin-Peuckert L., Pippi Salle J.L. (2001) A modified biofeedback program for children with detrusor-sphincter dyssynergia: 5-year experience. J. Urol.,166: 1470–75.
23. Piver M.S., Rutledge F., Smith J.P. (1974) Five classes of extended hysterectomy for women with cervical cancer. Obstet. Gynecol., 44: 265–272.
24. Li B., Zhang R., Wu L.Y. (2008) A prospective study on nerve-sparing radical hysterectomy in patients with cervical cancer. Chin. J. Gynecol. Oncol., 43: 606–610.
25. Hatch K.D., Fu Y.S. (1996) Cancer cervical and vaginal. Novak editor. Gynecology. 12-th ed. Williams Wilkins, New York: 1111–44.
26. Raspagliesi F., Ditto A., Fontanelli R. et al. (2004) Nerve-sparing radical hysterectomy: a surgical technique for preserving the autonomic hypogastric nerve. Gynecol. Oncol., 93: 307–314.
27. Sakuragi N., Todo Y., Kudo M. et al. (2005) A systematic nerve-sparing radical hysterectomy technique in invasive cervical cancer for preserving postsurgical bladder function. Int. J. Gynecol. Cancer, 15: 389–397.
Розширена гістеректомія (С1 nerve-sparing dissection) у хворих на інвазивний рак шийки матки
Резюме. Хірургічні операції з приводу раку шийки матки (РШМ) часто супроводжуються порушенням нормального функціонування сечової та статевої систем. Основною причиною цих порушень є операційна травма елементів тазової нервової системи, які іннервують органи сечової та статевої систем і розташовані в безпосередній близькості від ділянки втручання. Мета дослідження — обґрунтування впровадження розширеної гістеректомії (С1 nerve-sparing dissection) в клінічну практику при лікуванні хворих на інфільтративний рак шийки матки і оцінка безпосередніх результатів терапії. У відділенні онкогінекології Національного інституту раку з 2012 р. проведено хірургічне лікування 20 хворих на інфільтративний рак шийки матки з застосуванням розширеної гістеректомії (С1 nerve-sparing dissection) (середній вік хворих — 32,7±4,9 року). Перший досвід застосування в клінічній практиці лікування хворих на інфільтративний рак шийки матки розширеної гістеректомії (С1 nerve-sparing dissection) дає обнадійливі результати щодо зменшення кількості ранніх післяопераційних ускладнень з боку сечостатевої системи, однак для оцінки віддалених результатів лікування, кількості ускладнень, якості життя цієї категорії хворих потрібен подальший відбір клінічного матеріалу, виконання рандомізованих досліджень у спеціалізованих центрах.
Ключевые слова: рак шийки матки, розширена гістеректомія (С1 nerve sparing dissection), цистоманометрія, гіпогастральний нерв.
Extended hysterectomy (С1 nerve-sparing dissection) in patients with infiltrative cervical cancer
Summary. Surgical operations for cervical cancer are often accompanied by disruption of the normal functioning of urinary and reproductive systems. The main cause of these disorders is the surgical trauma of the pelvic autonomic nervous system innervating the urinary and reproductive systems’ organs and are located in the immediate proximity from the area of surgical intervention. The aim of the study was to justify the use of an extended hysterectomy (C1 nerve-sparing dissection) in the clinical practice for treatment of patients with infiltrative cervical cancer and to evaluate the results of such treatment. 20 patients (mean age 32,7±4,9 year) with infiltrative cervical cancer underwent extended hysterectomy (C1 nerve-sparing dissection) in gyneacological oncology department of the National Cancer Institute in 2012. The first experience of extended hysterectomy for treatment of patients with infiltrative cervical cancer shows promising results in reducing the number of early postoperative complications in the urinary system. But for assessment the long-term results of treatment, the frequency of complications and quality of life in these patients further set of clinical data, randomized trials in specialized centers is required.Surgical operations for cervical cancer are often accompanied by disruption of the normal functioning of urinary and reproductive systems. The main cause of these disorders is the surgical trauma of the pelvic autonomic nervous system innervating the urinary and reproductive systems’ organs and are located in the immediate proximity from the area of surgical intervention. The aim of the study was to justify the use of an extended hysterectomy (C1 nerve-sparing dissection) in the clinical practice for treatment of patients with infiltrative cervical cancer and to evaluate the results of such treatment. 20 patients (mean age 32,7±4,9 year) with infiltrative cervical cancer underwent extended hysterectomy (C1 nerve-sparing dissection) in gyneacological oncology department of the National Cancer Institute in 2012. The first experience of extended hysterectomy for treatment of patients with infiltrative cervical cancer shows promising results in reducing the number of early postoperative complications in the urinary system. But for assessment the long-term results of treatment, the frequency of complications and quality of life in these patients further set of clinical data, randomized trials in specialized centers is required.
Key words: cervical cancer, extended hysterectomy (С1 nervesparing dissection), cystomanometry, nerve hypogastric.














Leave a comment