Лікування та профілактика токсичних флебітів, індукованих хіміотерапією у хворих на рак грудної залози
Сивак Л.А., Губарева Г.О., Лялькін С.А., Майданевич Н.М., Алексик О.М., Філоненко К.С., Кліманов М.Ю., Аскольський А.В., Касап Н.В., Ульянченко К.О.
Резюме. У статті представлено огляд літератури щодо розвитку, діагностики та лікування токсичних флебітів та екстравазацій хіміопрепаратів внаслідок проведення хіміотерапії, наведено власний досвід із вивчення даних ускладнень у хворих на рак грудної залози. Виявлено, що місцеві ускладнення хіміотерапії є досить частими (до 15%) та серйозними ускладненнями лікування, розвиток яких може призводити до зниження ефективності хіміотерапії та вимагає активного лікування і профілактики.

Злоякісні пухлини грудної залози (ЗПГЗ) — найбільш поширене онкологічне захворювання серед жіночого населення. Більшість хворих на ЗПГЗ отримують хіміотерапію (ХТ): ад’ювантну (після операції), при поширених стадіях та несприятливих прогностичних факторах неоад’ювантну (передопераційну) та паліативну (у разі метастатичного ураження лімфатичних вузлів та інших органів) [1]. Таким чином, ХТ одержують понад 80% хворих на ЗПГЗ.
Пацієнти онкологічних закладів зазвичай отримують чисельні інфузії, що часто призводять до ламкості, порушень рухомості судин та складностей катетеризації судини. Супутні захворювання периферичних вен, кахексія, зміни еластичності тканин після радіотерапії, вторинна лімфедема також сприяють високому ризику розвитку зворотної екстравазації судин [2]. Ушкодження судин у пацієнтів онкологічного профілю зумовлено багаторазовими внутрішньовенними втручаннями, іноді — недостатньо надійним закріпленням інфузійного обладнання (інфузійної системи, голки, катетера), часом — надмірно активними маніпуляціями з катетером [2].
Ризик розвитку токсичних флебітів та екстравазацій хіміопрепаратів залежить від властивостей розчинів, осмолярності, а також наявності певних компонентів розчину (етиловий спирт, поліетиленгліколь).
Завдяки механізму дії цитостатичних препаратів питання їх екстравазації є дуже актуальним. Більшість із них належать до везикантів, тобто речовин, які призводять до тяжких ушкоджень тканин. Вони безпосередньо взаємодіють з ДНК клітини, спричиняючи поступове вмирання здорових клітин, що проявляється появою виразки [3].
На виникнення токсичних флебітів та екстравазацій хіміопрепаратів впливає фактор пацієнта, тобто наявність супутньої патології, проведення попередньої променевої терапії на зону введення хіміопрепарату та соціальні особливості.
Застосування певних медикаментів сприяє підсиленню місцевих ускладнень ХТ за рахунок певного механізму дії.
На розвиток екстравазацій також може впливати швидкість інфузії, яку необхідно обрати відповідно до пропускної спроможності вени, загального об’єму інфузії, особливо при одночасному введенні декількох розчинів [4]. Цитостатики має вводити лише досвідчена та компетентна медична сестра, обізнана з токсичними ефектами ХТ та правилами надання екстреної медичної допомоги. Інфузійний розчин слід готувати лише за правилами, вказаними виробником. Якісна робота медичного персоналу потребує постійного його навчання, створення відповідних правил роботи.
Токсичні флебіти розвиваються у 12–15% інфузій. Згідно з дослідженнями, проведеними S. Ikeda та співавторами (2004), частіше токсичні флебіти виникають внаслідок лікування цитарабіном, доксорубіцином, епірубіцином, дакарбазином та таксанами. Частота токсичних флебітів прямо пропорційна кількості введень препаратів та концентрації хіміопрепарату в розчині [5].
Тактика лікування екстравазацій хіміопрепаратів залежить від індивідуального перебігу. Нагляд можуть здійснювати спеціалісти від медичної сестри до пластичного хірурга та анестезіолога. Особливу увагу слід звертати на знеболення та профілактику інфекцій [6]. Окрему роль, за рекомендаціями групи North Trent Cancer Network, відводять знеболенню, яке має дуже важливе значення для пацієнта. Цей фактор забезпечує можливість дотримання та виконання усіх призначень лікарів, позитивне ставлення до дій медичного персоналу з боку пацієнта, уникнення зайвого стресу для організму [7].
При екстравазації препаратів групи А (таблиця) лікування розпочинається із застосування холоду/тепла (тільки для вінкаалкалоїдів) по 20 хв 4 рази на добу впродовж 3 днів, не допускаючи безпосереднього контакту зі шкірою, якщо в пацієнта є місцеві прояви. Так, за даними T.V. Goolsby та співавторів (2006), стрибкоподібне місцеве охолодження без іншої терапії має ефективність 89% у профілактиці виразкування [8]. Кінцівці надається підвищене положення впродовж 48 год, рухи кінцівкою мають бути обережними. За наявності місцевих симптомів використовують 1% мазь гідрокортизону. Як правило, це єдине необхідне лікування. Медикаментозна підтримка потрібна завжди при екстравазації великого об’єму рідини. У такому випадку згідно з розробленими алгоритмами тактика лікування екстравазації має відповідати алгоритму терапії при екстравазації хіміопрепаратів групи C.
Таблиця. Класифікація цитотоксичних агентів залежно від їх потенційної ушкоджуючої дії
| Нейтральні речовини (група А) |
Ірританти (група А) |
Ексфоліанти (група В) |
Везиканти (група С) |
|---|---|---|---|
| Аспарагіназа | Карбоплатин | Цисплатин | Кармустин |
| Блеоміцин | Іринотекан | Доцетаксел | Дакарбазин |
| Кладрибін | Тенипозид | Доксорубіцин | |
| ліпосомальний | Доксорубіцин | ||
| Циклофосфамід | Етопозид | Мітоксантрон | Епірубіцин |
| Цитарабін | Флоуроурацил | Оксаліплатин | Ідарубіцин |
| Флударабін | Метотрексат | Топотекан | Мітоміцин |
| Гемцитабін | Паклітаксел | ||
| Іфосфамід | Вінбластин | ||
| Мелфалан | Вінкристин | ||
| Ритуксимаб | Вінорельбін | ||
| Тіотепа |
Для препаратів групи В (див. таблицю) необхідно додатково застосовувати медикаментозне лікування. Якщо шкіра інтактна (немає везикул), використовують місцево аплікації розчину або крему з диметилсульфоксидом (антидот при екстравазації доксорубіцину, даунорубіцину, мітоміцину) або компреси з ним (з анальгетиками, кортикостероїдами) — наносять пензликом — 4 рази на добу впродовж 14 днів. Залишають оброблену ділянку непокритою. Якщо наявні везикули, диметилсульфоксид не застосовують [7].
Значну увагу також приділяють застосуванню антидотів [7]. Для групи С необхідне ін’єкційне введення гіалуронідази S/C відповідно до полюсів компаса навколо площі ураження (128 одиниць у 2 мл 0,9% хлориду натрію) до 14 днів [9]. Тіосульфат натрію рекомендований як антидот до мехлоретаміну, мустину, цисплатину. Використовують 1,6 мл 25% розчину цього препарату численними інсталяціями у та навколо місця екстравазації (підшкірно та внутрішньовенно) [2].
Згідно з результатами останніх досліджень при доксорубіцинових виразках практикують локальне введення гранулоцитарно-макрофагального фактора росту. Але тактика недостатньо вивчена й потребує подальшого дослідження. Це стосується застосування піридоксину гідрохлориду для лікування екстравазацій мітоміцину [2]. Доведено успішне використання локального введення фізіологічного розчину у стадії початку екстравазації та з метою профілактики виразкування [2].
Матеріали та методи
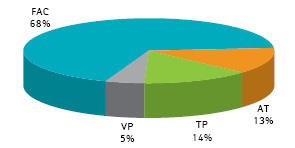
Вивчено розвиток місцевих ускладнень ХТ у 130 хворих із ЗПГЗ віком від 25 до 75 років (медіана віку — 50 років). Використовували схеми FAC (циклофосфамід, доксорубіцин, флуороурацил), АТ (доксорубіцин, паклітаксел), ТР (паклітаксел, цисплатин), VP (вінорельбін, цисплатин) (рис. 1).
Кожна пацієнтка в плані комплексного лікування отримала від 4 до 6 курсів поліхіміотерапії.
Враховували клінічні прояви та результати лабораторно-інструментальних методів дослідження (сонографічне обстеження ушкодженої вени, консультація хірурга). Оцінювали фактори ризику розвитку токсичних флебітів та екстравазацій. Місцеві прояви токсичності поліхіміотерапії оцінювали за шкалою NCI-CNC V.4.0.
Результати та їх обговорення
Усього проведено 732 курси поліхіміотерапії. Із них за схемою FAC — 496 (68%) курсів, АТ — 92 (13%), ТР — 106 (14%) та VP (5%) — 38 курсів.
Екстравазації хіміопрепаратів зареєстровано у 4 (3%) хворих. Виникнення екстравазацій частіше відбувалося після 4–7-го курсу ХТ. У 2 із цих пацієнтів розвиток даного ускладнення призвів до зниження інтенсивності ХТ шляхом редукції дози або подовження інтервалу між курсами. У 3 випадках виявили екстравазацію доксорубіцину, у 1 — циклофосфану. У 3 хворих зареєстровано екстравазації ІІ ступеня, у 1 пацієнтки екстравазації хіміопрепаратів супроводжувалися порушенням шкірного покриву.
Для лікування вводили знеболювальні та антигістамінні препарати, місцево — 1% мазь гідрокортизону, при збереженні цілісності шкірних покривів — аплікації 25–50% розчину димексиду та компреси з ним. Процес репарації тривав у середньому 76 днів (від 40 до 156 днів). У всіх хворих він завершився повним одужанням.
Розвиток токсичних флебітів виявлено у 16 пацієнтів: у 8 хворих флебіт виник після 4 курсів поліхіміотерапії, у 2 — після 5, у 6 — після перших 2 курсів. У 11 випадках зареєстровано токсичність І ступеня, у решті 5 — ІІ ступеня.
На рис. 2 продемонстровано випадок токсичного флебіту ІІ ступеня у хворої Н. після 4-го курсу ХТ за схемою FAC.
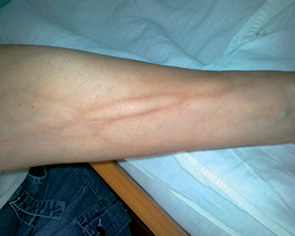
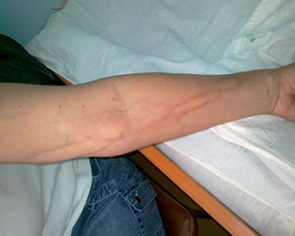
У разі виникнення токсичного флебіту застосовували консервативні методи лікування. Лікування пацієнтів з токсичними флебітами проводили з використанням нестероїдних протизапальних препаратів, антиагрегантів та знеболювальних препаратів. Місцево наносили гепаринові мазі та з нестероїдними протизапальними препаратами. Процес репарації тривав від 30 до 64 днів (у середньому — 41 день). Залишкові зміни у вигляді індурації стінки вени виявлено лише при вінорельбінових флебітах. В усіх випадках виникнення токсичного флебіту не впливало на подальшу терапію основного захворювання.
Таким чином, токсичні флебіти є менш тяжким ускладненням ХТ, ніж екстравазації. Поява токсичних флебітів може відбуватися вже після 1-го курсу ХТ. Кількість цих ускладнень збільшується зі збільшенням кількості курсів ХТ. Препарати, що найчастіше їх спричиняють, — це вінорельбін та доксорубіцин. Причому введення вінорельбіну у 100% випадків призводить до виникнення токсичного флебіту. Лікування їх у цілому консервативне. Виникнення токсичного флебіту не впливало на подальшу терапію основного захворювання.
Естравазації є більш серйозним ускладненням, що може призвести до тяжких наслідків, таких як порушення інтенсивності терапії основного захворювання, завдання шкоди здоров’ю пацієнта. Вони вимагають додаткових фінансових затрат на терапію, допомоги суміжних спеціалістів, спричиняють погіршення якості життя пацієнтів, функціонування їх органів та систем.
Висновки
Розвиток токсичних флебітів та екстравазацій може призвести до досить серйозних наслідків (виразкування шкіри, стриктура м’язів, ампутація кінцівок), що супроводжуються вираженим больовим синдромом, порушенням функції ураженої ділянки, погіршенням якості життя хворих, та вимагає додаткових суттєвих фінансових витрат на лікування. Дотримання правил профілактики та вчасно розпочате адекватне лікування токсичних ускладнень дозволяють уникнути їх розвитку та попередити подальше поглиблення ступеня токсичних флебітів та екстравазацій хіміопрепаратів.
Список використаної літератури
1. Клинические рекомендации (2008) Онкология / под ред. В.И. Чиссова, С.Л. Дарьяловой. ГЭОТАР-Медиа, Москва: 269–314.
2. Wickham R., Engelking C., Sauerland C., Corbi D. (2006) Vesicant extravasation part II: Evidence-based management and continuing controversies. Oncol. Nurs. Forum, 27; 33(6): 1143–50.
3. Sauerland C., Engelking C., Wickham R., Corbi D. (2006) Vesicant extravasation part I: Mechanisms, pathogenesis, and nursing care to reduce risk. Oncol. Nurs. Forum, 27; 33(6): 1134–41.
4. Kagel E.M., Rayan G.M. (2004) Intravenous catheter complications in the hand and forearm. J. Trauma, 56: 123–7.
5. Ikeda S., Douchi T., Nagata Y. (2004) Effective prevention of chemotherapy-induced phlebitis by low-dose heparin: A prospective randomised trial. Ann. Oncol., 16(7): 942–45.
6. Mader I. et al. (2006) Extravasation of cytotoxic agents. Infect. Control, 34: 308–12.
7. Extravasation guidlines North Trent Cancer Network Approved: 13.11.2008 To be reviewed by: Extravasation Sub-Group from North Trent Haemato-Oncology Nurse Group and the Pharmacist Group.
8. Goolsby T.V., Lombardo F.A. (2006) Extravasation of chemotherapeutic agents: prevention and treatment. Semin. Oncol., 33(1): 139–43.
9. Disa J.J., Chang R.R., Mucci S.J., Nelson H. (2005) Goldberg Prevention of Adriamycin-Induced Full-Thickness Skin Loss Using Hyaluronidase Infiltration. New Engl. J. Med., 15: 987–993.
Лечение и профилактика токсических флебитов, индуктируемых химиотерапией у больных раком грудной железы
Резюме. В статье представлен обзор литературы относительно развития, диагностики и лечения токсических флебитов и экстравазаций химиопрепаратов в результате проведения химиотерапии, приведен собственный опыт по изучению данных осложнений у больных раком грудной железы. Выявлено, что местные осложнения химиотерапии являются достаточно частыми (до 15%) и серьезными осложнениям лечения, развитие которых может приводить к снижению эффективности химиотерапии и требует активного лечения и профилактики.
рак грудной железы, токсический флебит, экстравазация химиопрепаратов, химиотерапия.














Leave a comment