Неоад’ювантна хіміотерапія у хворих зі злоякісними пухлинами яєчника
Свінціцький В.С.1, Клименко Е.С.2
Резюме. Проведено аналіз комплексного лікування 857 хворих із занедбаними формами злоякісних пухлин яєчника (ЗПЯ), які на першому етапі лікування одержали неоад’ювантну хіміотерапію (НАХТ). Проведення НАХТ дозволяє підвищити резектабельність пухлин, а також частоту виконання оптимальних циторедукцій, покращує суб’єктивний статус і якість життя пацієнток із ЗПЯ. Аналіз загальної 5-річної виживаності хворих зі ЗПЯ показав, що для всіх пацієнток після НАХТ вона становить 17,1%. Розмір залишкової пухлини після проміжних циторедуктивних операцій є найважливішим прогностичним чинником, який впливає на виживаність хворих із занедбаними формами ЗПЯ.
Вступ
За даними Міжнародного агентства з вивчення раку (LARC), злоякісні пухлини яєчника (ЗПЯ) займають 7-е місце в структурі загальної онкологічної захворюваності і 5-е місце серед причин смерті від усіх злоякісних пухлин у жінок. Щорічно у світі реєструється більше 165 тис. нових випадків ЗПЯ, і більше 100 тис. жінок помирають від цього захворювання. Причому на I–II стадію захворювання припадає тільки 30% вперше виявлених патологій, тоді як поширені форми становлять 70% випадків (рис. 1).
У жінок в постменопаузальний період захворюваність на ЗПЯ в 10 разів вища, ніж у жінок в пременопаузі. Летальність хворих зі ЗПЯ на першому році після встановлення діагнозу становить 35%. За даними ракових популяційних реєстрів країн Європи, 1-річна виживаність хворих зі ЗПЯ дорівнює 65%, 3-річна — 41%, 5-річна — 35%.
В Україні реєструють стабільні показники захворюваності на ЗПЯ з тенденцією до зростання та стабільно високі показники смертності від даної патології: ЗПЯ діагностують більш ніж у 4000 жінок (15,8 на 100 тис.). Цей показник займає 7-ме місце в структурі загальної онкологічної захворюваності (5%) і 3-тє — в структурі гінекологічної, після раку тіла і шийки матки. Від ЗПЯ помирають майже 2 тис. молодих жінок. Результати 5-річної виживаності знаходяться на рівні 25–30%, незважаючи на застосування в лікуванні комплексних сполук платини, а останнім часом і таксанів.
Більшість новоутворень яєчника (85%) розвивається з поверхневого покривного епітелію. Половина епітеліальних пухлин — доброякісні, 33% — злоякісні, 16% — граничні. Стандартним лікуванням хворих зі ЗПЯ є комбінація хірургічного й хіміотерапевтичного компонентів. Однак послідовність їх застосування постійно стає темою обговорень і є основою дискусій серед онкогінекологів. Потенційно всім пацієнткам зі ЗПЯ III–IV стадії мають проводити первинну циторедуктивну операцію, мета якої — максимальне видалення первинної пухлини та осередків дисемінації у черевній порожнині. Вона включає екстирпацію матки з додатками, надпіхвову ампутацію матки або двосторонню аднексектомію з обов’язковим субтотальним видаленням великого сальника. Таке хірургічне втручання в оптимальному обсязі можливе тільки у 50% хворих зі ЗПЯ і лише в 10–15% із занедбаними формами захворювання. Після первинної циторедуктивної операції проводять 6 курсів хіміотерапії (ХТ) I лінії, що включає похідні платини й таксани [1–2].
Нерідко в результаті клінічного обстеження (дані ультразвукової діагностики, колоноскопії, іригоскопії, екскреторної урографії, ангіографії, комп’ютерної або магнітно-резонансної томографії) виявляють ознаки, які свідчать про сумнівність доцільності проведення циторедуктивної операції: наявність пухлини, що вростає в заочеревинний простір, множинні метастази в брижах або по очеревині тонкого й товстого кишечнику, метастази у воротах печінки. Як правило, перелічені ознаки проявляються у хворих з нерухомим пухлинним конгломератом з інфільтративним характером росту, що заповнює всю порожнину таза. Наявність таких масивних пухлинних утворень у черевній порожнині зумовлює різке зниження компенсаторних можливостей організму. Пацієнтки з розповсюдженим пухлинним процесом та масивною дисемінацією становлять найбільш складний для лікування контингент хворих зі ЗПЯ, тому що на момент початку терапії в більшості з них виражені асцит, плеврит, імуносупресія і пухлинна інтоксикація, які погіршують загальний статус і якість життя хворих [3–6].
Передопераційна ХТ дає можливість уповільнити темпи накопичення асциту та плевриту, підвищити резектабельність пухлини за рахунок її редукції, збільшити абластичність хірургічного втручання внаслідок елімінації субклінічних осередків, визначити індивідуальну чутливість пухлини до використаних цитостатиків, прогнозувати клінічний перебіг хвороби, поліпшити суб’єктивний статус і якість життя пацієнток [7, 8].
Мета даної роботи — аналіз впливу неоад’ювантної хіміотерапії (НАХТ) на результати проміжних циторедуктивних операцій (ПрЦРО) та віддалені результати лікування хворих зі ЗПЯ.
Об’єкт і методи дослідження
У відділенні онкогінекології Національного інституту раку проведено дослідження, метою якого було визначення ефективності неоад’ювантної платино- і таксановмісної поліхіміотерапії, а також шляхів введення цитостатиків, її вплив на результати комплексного лікування хворих із поширеними форми ЗПЯ.
У дослідження включено 857 хворих із розповсюдженими ЗПЯ (ІІB–ІV стадії) віком від 11 до 81 року (середній вік пацієнток — 48,7±5,8 року), яким на першому етапі лікування проводили НАХТ. Із 857 первинних хворих у 72 (8,3%) діагностовано ІІ стадію захворювання, у 534 (61,9%) — III, у 251 (29,8%) — IV стадію. У 631 (76,6%) пацієнтки виявлено епітеліальні ЗПЯ (ЕЗПЯ), у 66 (7,7%) — пухлини строми статевого тяжа (ПССТ), у 71 (8,3%) — герміногенні ЗПЯ (ГЗПЯ), у 89 (10,4%) — інші гістологічні типи пухлин яєчника (табл. 1).
Таблиця 1. Розподіл хворих за віком та морфологією пухлин
| Вік | Гістотип пухлин | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ЕЗПЯ | ПССТ | ГЗПЯ | Інші | Усього | ||||||
| n | % | n | % | n | % | n | % | n | % | |
| <19 | 0 | – | 7 | 10,6 | 2 | 2,8 | 0 | – | 9 | 1,1 |
| 20–29 | 3 | 0,5 | 5 | 7,6 | 6 | 8,5 | 0 | 0 | 14 | 1,6 |
| 30–39 | 31 | 4,9 | 8 | 12,1 | 21 | 29,9 | 2 | 2,2 | 62 | 7,2 |
| 40–49 | 98 | 15,5 | 14 | 21,2 | 29 | 40,8 | 30 | 33,7 | 172 | 20,1 |
| 50–59 | 269 | 42,6 | 20 | 30,3 | 13 | 18,3 | 4 | 4,5 | 306 | 35,7 |
| 60–69 | 198 | 31,4 | 9 | 13,6 | 0 | 43 | 48,3 | 250 | 29,2 | |
| >70 | 23 | 3,6 | 3 | 4,5 | 0 | 17 | 19,3 | 43 | 5,1 | |
| Усього | 631 | 100 | 66 | 100 | 71 | 100 | 89 | 100 | 857 | 100 |
За даними табл. 1, 63% хворих були в найбільш працездатному віці — 30–60 років, із них 27% пацієнток репродуктивного віку. Переважна більшість хворих з ЕЗПЯ (58,1%) — у віці від 40 до 60 років. У 576 (67,2%) був асцит, плеврит виявили у 215 (25,1%) пацієнток (158 випадків — односторонній і 57 — двосторонній), метастази в печінку або селезінку — у 75 (8,7%) і 16 (1,9%) хворих відповідно. У 41 (4,8%) пацієнтки було ураження пупкового кільця. У 251 (29,8%) хворої визначали поєднання кількох ознак, що характеризує IV стадію захворювання: ураження діафрагми, селезінки, печінки, проростання пухлиною передньої черевної стінки, метастази в легені та інші органи.
Переважна більшість хворих (73,6%) мали ЕЗПЯ, із них у 82,9% був серозний гістотип пухлини, у 5,4% — муцинозний, у 7,3% — мезонефроїдний, у 2,4% — змішані та ін. Розподіл пацієнток залежно від одержуваних схем передопераційної ХТ продемонстровано в табл. 2.
Таблиця 2. Розподіл хворих залежно від схем передопераційної ХТ
| Схеми ХТ | Кількість хворих | |||
|---|---|---|---|---|
| n | % | |||
| Платиновмісні схеми | СР/САР | Цисплатин 100 мг/м2, циклофосфамід 600 мг/м2 або цисплатин 100 мг/м2, циклофосфамід 600 мг/м2, доксорубіцин 40 мг/м2 | 552 | 64,4 |
| СС | Карбоплатин AUC-6, циклофосфамід 600 мг/м2 | 146 | 17,0 | |
| Усього | 698 | 81,4 | ||
| Платино-таксановмісні схеми | TP | Паклітаксел 175 мг/м2, цисплатин 100 мг/м2 | 55 | 6,4 |
| TC | Паклітаксел 175 мг/м2, карбоплатин AUC-5–6 | 34 | 3,4 | |
| DP | Доцетаксел 75 мг/м2, цисплатин 100 мг/м2 | 21 | 2,5 | |
| Усього | 110 | 12,8 | ||
| BEP | Цисплатин 20 мг/м2 та етопозид 100 мг/м2 в/в 1–5-й дні, повтор циклу через 3 тиж 4 цикли блеоміцин 30 мг в/в 1; 8; 15-й дні кожні 3 тиж |
12 | 1,4 | |
| Інші схеми | Гемцитабін, топотекан, оксаліплатин, доксорубіцин | 37 | 4,3 | |
| Усього | 857 | 100 | ||
Примітка: в/в — тут і далі — внутрішньовенно.
Більшість хворих у якості НАХТ отримували стандартні платиновмісні режими: СР/САР — 552 (64,4%) пацієнтки і СС — 146 (17,0%), а також платино- і таксановмісні режими ТР, ТС, DP — 110 (12,8%) хворих, інші режими ХТ застосували у 45 (5,7%) осіб.
На прикладі серозної сосочкової цистаденокарциноми яєчника вивчено лікувальний патоморфоз ЗПЯ після НАХТ.
Результати та їх обговорення
У 63,4% хворих із занедбаними ЗПЯ відзначено позитивний ефект НАХТ: відбулося зменшення кількості асциту, повне його зникнення зареєстровано в 89,8% випадків, зменшився обсяг пухлинних осередків, вимірюваних при ультразвуковому дослідженні, покращилися суб’єктивний статус і якість життя хворих.
Ефективнішою НАХТ була у хворих з ПССТ та ГЗПЯ — 72,7 та 71,8% відповідно. У пацієнток з ЕЗПЯ ефективність НАТХ виявилася дещо нижчою (61,6% випадків), ефективнішою передопераційна ХТ була при серозному гістотипі ЕЗПЯ (66,2%), малоефективною при муцинозному гістотипі (38,2%) та мезонефроїдному (32,6%).
При неефективній НАХТ спостерігалися симптоми накопичення асциту, збільшення розмірів пухлин, компресії кишечника, астенізації та інтоксикації. НАХТ ефективнішою була у хворих із ІІІ стадією захворювання (67,2% випадків), менш ефективною у пацієнток із IV стадією ЗПЯ (44,6% випадків).
Зменшення величини СА-125 від 57 до 81% від первинних показників після НАХТ було віддзеркаленням високої ефективності лікування, підтвердженої зниженням маркера на 68% і більше від початкової величини у 58,4% хворих. На 75% маркер зменшився у 24,9% пацієнток. Зниження маркера <50% у процесі НАХТ, що є несприятливим чинником прогнозу перебігу захворювання, відзначено в 13,3% хворих.
Безперечним успіхом проведеного лікування стало значне зниження середнього рівня пухлинного маркера СА-125, який перед операцією становив 231,9±7,9 од./мл, що майже в 2 рази менше, ніж у групі без НАХТ.
Усім 857 хворим після НАХТ проведено ПрЦРО.
Основним чинником, що впливає на результати лікування і виживаність хворих, є розмір резидуальної пухлини, тому для вивчення прогностичної значущості цього показника всіх 857 пацієнток з ІІ–ІV стадією залежно від типу виконаної операції розподілено на 4 групи (табл. 3).
Під час хірургічного втручання виявлено наступне розповсюдження пухлинного процесу у хворих: метастази по очеревині — 528 (61,6%); у великий сальник — 571 (66,6%); у печінку — 41 (4,8%); селезінку — 27 (3,2%); у лімфатичні вузли — 129 (15,1%); плеврит — 12 (1,4%); асцит — 26 (3,0%).
Таблиця 3. Типи ПрЦРО, виконаних у хворих зі ЗПЯ
| Тип ПрЦРО | Кількість хворих | |
|---|---|---|
| n | % | |
| Стандартні | 475 | 55,4 |
| Комбіновані | 255 | 29,8 |
| Розширені | 73 | 8,5 |
| Інші (частіше паліативні) | 54 | 6,3 |
| Усього | 857 | 100 |
Стандартні операції виконано у більшості хворих (55,4%) із розповсюдженими формами ЗПЯ, що включали пангістеректомію та резекцію сальника або оментектомію.
До цієї групи ввійшли 303 хворих у віці від 11 до 80 років. Середній вік становив 50,7±2,5 року. Розподіл за стадіями в даній групі був наступним: III стадію ЗПЯ діагностовано у 263 (86,9%) пацієнток, а IV стадію — у 40 (13,1%).
Стандартний обсяг включав 4 варіанти хірургічних втручань (табл. 4).
Таблиця 4. Стандартні операції, виконані у хворих зі ЗПЯ після НАХТ
| Тип операції | Кількість хворих | |
|---|---|---|
| n | % | |
| Суправагінальна ампутація матки з додатками та резекція сальника | 17 | 3,6 |
| Суправагінальна ампутація матки з додатками та оментектомія | 28 | 5,9 |
| Екстирпація матки з додатками та резекція великого сальника | 174 | 36,6 |
| Екстирпація матки з додатками та оментектомія | 256 | 53,9 |
| Усього | 475 | 100 |
Проведено аналіз радикальності виконаних хірургічних втручань. Встановлено, що оптимальну циторедуктивну операцію (макроскопічно залишкова пухлина не візуалізувалася) виконано у 91 (19,2%) хворої; субоптимальну циторедуктивну операцію (макроскопічно залишкова пухлина <1 см) — у 299(62,9%) хворих; неоптимальну циторедуктивну операцію (макроскопічно залишкова пухлина > 1 см) — у 85 (17,9%) пацієнток.
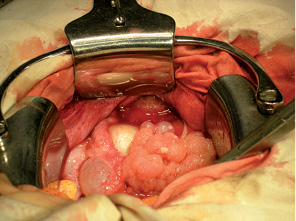
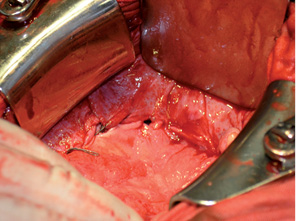
Найбільшу кількість оптимальних стандартних операцій проведено в обсязі пангістеректомії та оментектомії — 57 (62,6%) хворих (рис. 2). При виконанні суправагінальної ампутації матки з додатками з резекцією великого сальника оптимально прооперовано тільки 5 (5,5%) пацієнткам. Максимальний обсяг циторедукції досягнуто при видаленні великого сальника (табл. 5).
Таблиця 5. Ступінь циторедукції у хворих зі ЗПЯ після НАХТ та стандартного обсягу ПрЦРО
| Тип операції | Кількість хворих | |||||||
|---|---|---|---|---|---|---|---|---|
| n | % | Оптимальна | Субоптимальна | Неоптимальна | ||||
| n | % | n | % | n | % | |||
| Суправагінальна ампутація матки з додатками та резекція сальника | 17 | 3,6 | 1 | 1,1 | 8 | 2,7 | 8 | 9,4 |
| Суправагінальна ампутація матки з додатками та оментектомія | 28 | 5,9 | 4 | 4,4 | 17 | 5,7 | 7 | 8,2 |
| Пангістеректомія та резекція сальника | 174 | 36,6 | 29 | 31,9 | 107 | 35,8 | 38 | 44,8 |
| Пангістеректомія та оментектомія | 256 | 53,9 | 57 | 62,6 | 167 | 55,8 | 32 | 37,6 |
| 91 | 100 | 299 | 100 | 85 | 100 | |||
| Усі операції | 475 | 100 | 91 | 19,2 | 299 | 62,9 | 85 | 17,9 |
Комбіновані операції виконано у 255 хворих у віці від 29 до 79 років. Середній вік становив 51,2±8,5 року. Розподіл за стадіями в групі «комбінованих операцій» наступний: III стадію ЗПЯ встановлено у 206 (80,8%) пацієнток, а IV — у 49 (9,2%). Характеристику обсягів проміжних циторедуктивних комбінованих операцій, крім пангістеректомії та оментектомії, подано в табл. 6.
Таблиця 6. Обсяг комбінованих ПрЦРО у хворих зі ЗПЯ після НАХТ
| Обсяги ПрЦРО, крім пангістеректомії та оментектомії | Кількість хворих | |
|---|---|---|
| n | % | |
| Часткова тазова перитонектомія | 79 | 31,0 |
| Видалення імплантаційних метастазів на очеревині | 41 | 16,1 |
| Екстирпація кукси шийки матки з додатками та частковою тазовою перитонектомією | 14 | 5,5 |
| Апендектомія | 18 | 7,1 |
| Спленектомія | 14 | 5,5 |
| Резекція тонкої кишки | 32 | 12,5 |
| Правобічна геміколектомія | 23 | 9,0 |
| Лівобічна геміколектомія | 21 | 8,2 |
| Операція Гартмана | 24 | 9,4 |
| Резекції ректосигмоїдного відділу товстої кишки | 37 | 14,9 |
| Атипові резекції печінки | 23 | 9,0 |
| Нефректомія | 1 | 0,4 |
| Резекція сечового міхура | 24 | 9,4 |
| Резекція передньої черевної стінки з пухлиною | 27 | 10,4 |
| Гастроентероанастомоз | 3 | 1,2 |
| Ілеотрансверзоанастомоз | 11 | 4,3 |
| Нефростомія | 2 | 0,8 |
| Формування трансверзостоми | 9 | 3,5 |
| Поєднані комбіновані втручання | 193 | 75,7 |
Показаннями до виконання комбінованих операцій були: наявність резектабельної пухлини на сусідніх органах і тканинах після проведення стандартного обсягу хірургічного втручання та залишкові пухлини, що впливають на нормальну функцію сусідніх органів, які неможливо видалити без резекції сусідніх органів після видалення основної маси первинної пухлини.
Обсяг комбінованого хірургічного втручання в групах варіював, крім пангістеректомії та видалення великого сальника, від апендектомії до правобічної чи лівобічної геміколектомії, причому часто в поєднанні з іншими хірургічними втручаннями, тому що при ревізії органів черевної порожнини у 80% хворих виявлено пухлинне ураження тонкої кишки — у 32 (12,5%) пацієнток; ураження товстої кишки — у 125 (49,3%); поєднане ураження — у 193 (75,7%).
У всіх випадках при ураженні тонкої кишки виявляли залучення клубової кишки, а при залученні товстої кишки переважно були уражені ректосигмоїдний і попереково-ободовий відділи.
За результатами гістологічного дослідження у 97 (38,1%) хворих підтверджено залучення кишки в пухлинний процес. Це дозволило зробити висновок, що наявність макроскопічного залучення кишки в більшості випадків пов’язана з її метастатичним ураженням або проростанням, що вимагало застосування до неї відповідного хірургічного підходу. Апендектомію виконано у 18 (7,1%) пацієнток за наявності макроскопічного залучення червоподібного відростка в пухлинний процес. При дослідженні гістологічної будови пухлини встановлено, що метастазували або проростали в червоподібний відросток частіше муцинозні пухлини — 77,7% (14/18).
Залучення сечовивідних шляхів у пухлинний процес діагностовано у 26 (10,2%) хворих. У 24 (9,4%) пацієнток виявлено залучення сечового міхура в пухлинний конгломерат, а у 2 (0,8%) — сечоводу. У цій клінічній ситуації вдалися до резекції сечового міхура у 24 (9,4%) хворих і нефростомії — у 2 (0,8%).
Для аналізу радикальності оперативних втручань у даній групі використовували критерії, описані раніше, що дозволило одержати наступні результати (табл. 7). У табл. 7 подано характеристики лише хворих, у яких виконано поєднані комбіновані хірургічні втручання.
Таблиця 7. Ступінь циторедукції після комбінованих ПрЦРО
| Тип операції | Кількість хворих | |||||||
|---|---|---|---|---|---|---|---|---|
| n | % | Оптимальна | Субоптимальна | Неоптимальна | ||||
| n | % | n | % | n | % | |||
| Тазова перитонектомія | 81 | 31,7 | 37 | 14,4 | 35 | 13,7 | 9 | 3,6 |
| Резекція печінки або спленектомія | 37 | 14,5 | 19 | 7,5 | 11 | 4,3 | 7 | 2,7 |
| Операції на кишечнику | 106 | 41,6 | 49 | 19,1 | 36 | 14,1 | 21 | 8,3 |
| Інші комбіновані хірургічні втручання | 31 | 12,2 | 16 | 6,2 | 8 | 3,1 | 7 | 2,7 |
| Усього | 255 | 100 | 121 | 47,2 | 90 | 35,3 | 44 | 17,3 |
Оптимальні комбіновані хірургічні втручання у хворих із ЗПЯ виконано у 121 (47,6%) хворої, в основному за рахунок оментектомії — у 79 (31,0%), резекції ураженої кишки — у 105 (41,5%) та тазової перитонектомії — у 93 (36,5%), субоптимальні — у 90 (35,3%) та неоптимальні — у 44 (17,3%) хворих.
Використання розробленої методики тазової перитонектомії з ретроградною екстирпацією матки дозволяє зберегти цілісність ректосигмоїдного відділу товстого кишечнику, дотримуючись принципу радикалізму у хворих із ЗПЯ, збільшити кількість оптимальних операцій у пацієнток з розповсюдженими формами ЗПЯ
За результатами дослідження у 70 (66,0%) пацієнток резекцію кишечнику проведено з первинним анастомозуванням. У 37 (14,5%) — комбіновані операції, пов’язані з резекцією печінки та спленектомією.
Розширені операції виконано 73 хворим зі ЗПЯ у віці від 18 до 74 років. Середній вік становив 50,7±7,9 року. Показаннями до розширених хірургічних втручань була наявність збільшених лімфовузлів (клубових або парааортальних) за відсутності залишкової пухлини в черевній порожнині після проведення стандартного обсягу або при виконанні операції, що супроводжувалася вростанням первинної пухлини в заочеревинний простір. Теоретичною передумовою для розширення обсягу операції є дані про лімфогенне метастазування ЗПЯ. Так, частота ураження заочеревинних лімфовузлів у хворих зі ЗПЯ III–IV стадії, за даними літератури, становить 63–82%. Враховуючи шляхи лімфогенного метастазування при ЗПЯ, проводили різні хірургічні втручання в поєднанні з пангістеректомією та оментектомією — від резекції збільшених клубових лімфатичних вузлів до клубово-парааортальної лімфаденектомії. Характеристику варіантів розширених проміжних циторедуктивних хірургічних втручань представлено в табл. 8.
Таблиця 8. Типи лімфодисекцій, проведених у хворих зі ЗПЯ після НАХТ
| Тип лімфаденектомії | Кількість хворих | |||||||
|---|---|---|---|---|---|---|---|---|
| n | % | Оптимальна | Субоптимальна | Неоптимальна | ||||
| n | % | n | % | n | % | |||
| Тазова | 40 | 54,8 | 29 | 39,8 | 8 | 11,0 | 3 | 4,1 |
| Парааортальна | 4 | 5,4 | 2 | 2,7 | 2 | 2,7 | – | |
| Пахова | 29 | 39,8 | 16 | 21,9 | 10 | 13,7 | 3 | 4,1 |
| Усього | 73 | 100 | 47 | 64,4 | 20 | 27,4 | 6 | 8,2 |
Найчастіше виявляли збільшення клубових та парааортальних лімфатичних вузлів, тому пангістеректомія, оментектомія, клубово-парааортальна лімфаденектомія характеризувалися як умовно радикальна операція більше ніж у 60% хворих зі ЗПЯ.
Наші результати підтверджують дані інших дослідників, які задля досягнення радикалізму хірургічних втручань при розповсюджених формах ЗПЯ наполягають на виконанні комбінованих та розширених операцій [9–10]. Розподіл хворих зі ЗПЯ після ПрЦРО залежно від ступеня циторедукції подано в табл. 9.
Таблиця 9. Розподіл хворих за ступенем циторедукції після ПрЦРО
| Тип операції | Кількість хворих | ||||||
|---|---|---|---|---|---|---|---|
| Оптимальні | Субоптимальні | Неоптимальні | |||||
| n | % | n | % | n | % | ||
| Група хворих після ПрЦРО | Стандартні | 30 | 9,9 | 211 | 69,6 | 62 | 20,5 |
| Комбіновані | 52 | 41,3 | 44 | 34,9 | 30 | 23,8 | |
| Розширені | 16 | 59,3 | 7 | 25,9 | 4 | 14,8 | |
| Інші | 3 | 5,0 | 11 | 18,3 | 46 | 76,7 | |
| Група хворих після ПрЦРО | Стандартні | 91 | 19,2 | 299 | 62,9 | 85 | 17,9 |
| Комбіновані | 121 | 47,6 | 90 | 35,3 | 44 | 17,5 | |
| Розширені | 47 | 64,3 | 20 | 27,4 | 6 | 8,2 | |
| Інші | 3 | 5,5 | 8 | 14,8 | 43 | 79,6 | |
Загальний ефект НАХТ становив 71,6%. Високий показник зумовлений тим, що до даної групи входили пацієнтки і з частковою ремісією <25%. Тобто, якщо після лікування не розвинулися плеврит, асцит, і, за даними ультразвукової томографії, відзначено позитивну динаміку, то хворих оперували. Ефективність платиновмісних схем становила 68,5%, платино- і таксановмісних — 81,8%, а інших схем — 70,5%. Застосування таксанів у передопераційній ХТ пов’язано перш за все з важчим у плані лікування контингентом хворих у цій групі, тому що часто НАХТ таксанами починали тільки при найпоширеніших процесах, тоді як СР/САР вже міцно увійшли до стандартів первинної терапії. Включення таксанів у схеми НАХТ підвищує ефективність хірургічного втручання на 13,3% порівняно лише з платиновмісними схемами (р<0,05). Схеми НАХТ, після яких виконано оптимальні ПрЦРО, подано в табл. 10.
Таблиця 10. Схеми НАХТ, після яких проведено оптимальні ПрЦРО
| Схеми НАХТ | Кількість хворих після оптимальних ПрЦРО | |
|---|---|---|
| n | % | |
| Платиновмісні | 92 | 35,5 |
| Платино- і таксановмісні | 119 | 45,9 |
| Інші схеми | 51 | 18,6 |
| Усього хворих | 262 | 100 |
При аналізі групи хворих, що одержували НАХТ, у яких проведено хірургічні втручання в оптимальному обсязі, 45,9% призначено таксано- і платиновмісні схеми, 35,5% пацієнток — платиновмісні та 18,6% — інші схеми НАХТ (різниця статистично достовірна р<0,05).
Оскільки головним критерієм визначення ефективності методик НАХТ при мікроскопічному дослідженні серозних ЕЗПЯ є наявність структурних незворотних змін пухлини або залишкового, структурно збереженого, пухлинного компонента, то для об’єктивізації результатів оцінки лікувального патоморфозу серозних ЕЗПЯ проведено морфологічне дослідження останнього, тому що виявлення часткового вмісту резидуальної пухлинної паренхіми, на наш погляд, дозволяє більш точно визначати не тільки ступінь безпосереднього антибластомного впливу на пухлину, а й прогнозувати подальший перебіг захворювання. Морфометричну оцінку ефективності НАХТ проведено у 147 хворих із серозною ЕЗПЯ (табл. 11).
Таблиця 11. Морфометричні показники залежно від методики НАХТ у хворих із серозними ЕПЗЯ
| Методика НАХТ | Кількість хворих | Частковий вміст резидуальної пухлинної паренхіми | Коефіцієнт достовірності (Р) | |
|---|---|---|---|---|
| в/в | 41 | 38,8±7,7 | Р1–3<0,05 | |
| е/а | 47 | 27,1±6,9 | Р2–3<0,05 | |
| Комбінована | 59 | Платиновмісна ХТ (n=38) | 19,1±6,4 | Р3–4<0,05 |
| Платино- і таксановмісна ХТ (n=21) | 15,2±6,4 | |||
| Контроль | 35 | 46,5±6,7 | Р1–2>0,05 | |
Виходячи з отриманих результатів морфометричної оцінки лікувального патоморфозу серозних ЕЗПЯ стає очевидним, що в/в застосування ХТ не має статистично вірогідного впливу на серозні пухлини. Можна простежити тільки тенденцію до зменшення в них вмісту резидуальної паренхіми, що залишилася після неоад’ювантного лікування (Р1–2>0,05). Проте ендоабдомінальна (е/а) ХТ із застосуванням аналогічних хіміопрепаратів призводить до вірогідного зменшення вмісту пухлинної паренхіми в серозних ЕЗПЯ порівняно з групою контролю (Р1–3< 0,05) і з групою, у якій проводили в/в ХТ (Р2–3 <0,05).
Підсумовуючи результати проведеного морфологічного дослідження серозних ЕЗПЯ, при неоад’ювантному впливі ХТ слід очікувати на зниження частоти післяопераційного метастазування внаслідок суттєвої втрати пухлинної паренхіми на етапі передопераційного протипухлинного лікування. Ступінь лікувального патоморфозу залежно від методики НАХТ представлено в табл. 12.
Таблиця 12. Лікувальний патоморфоз ЗПЯ залежно від методики проведення НАХТ
| Ступінь лікувального патоморфозу | Кількість досліджених пухлин | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| НАХТ в/в ХТ | НАХТ е/а | НАХТ комбінована | Усього | |||||||
| n | % | n | % | Платиновмісна | Платино- і таксановмісна | n | % | |||
| n | % | n | % | |||||||
| Слабкий або не визначається | 22 | 53,7 | 19 | 40,4 | 9 | 26,5 | 4 | 19,1 | 54 | 37,7 |
| Помірний | 14 | 34,1 | 19 | 40,4 | 14 | 41,2 | 9 | 42,8 | 56 | 39,2 |
| Виражений | 5 | 12,2 | 7 | 14,9 | 10 | 29,4 | 7 | 33,3 | 29 | 20,3 |
| Пухлина не визначається | – | – | 2 | 4,3 | 1 | 2,9 | 1 | 4,8 | 4 | 2,8 |
| Усього | 41 | 100 | 47 | 100 | 38 | 100 | 21 | 100 | 143 | 100 |
Так, у хворих досліджуваних груп в 62,3% випадків виявлено значний лікувальний патоморфоз, що свідчить про високу чутливість пухлин до НАХТ. Найвищі показники зафіксовано в групах, у яких проводили комбіновану НАХТ: 32,3% — при платиновмісних схемах ХТ та 38,1% — при платино- і таксановмісних схемах, — на відміну від в/в та е/а платиновмісних схем (12,2 і 19,1% відповідно; р <0,05).
Дані табл. 12 свідчать про статистично вірогідний ефект неоад’ювантної терапії хворих із серозними ЕЗПЯ при комбінованому введенні цитостатиків. Проведення передопераційної неоад’ювантної комбінованої ХТ значно знижувало темпи накопичення асциту і плевриту, збільшувало резектабельність пухлини за рахунок її редукції, дозволяло частіше виконати оптимальні хірургічні втручання у хворих з ЕЗПЯ.
Досягнення вищих концентрацій цитостатиків у пухлині при поєднанні в/в та е/а введень препаратів сприяли підвищенню абластичності хірургічного втручання. За ступенем елімінації пухлинних осередків визначали індивідуальну чутливість пухлини до цитостатиків.
Післяопераційне ад’ювантне комбіноване введення хіміопрепаратів дозволяє досягти їх високих концентрацій у черевній порожнині, що деструктивно впливає на мікроскопічні залишки осередків пухлини на серозних покривах органів черевної порожнини.
3-річна безрецидивна виживаність хворих із серозними ЕЗПЯ при застосуванні комбінованої передопераційної терапії (табл. 13) в 2 рази вища за показники у контрольній групі та значно краща, ніж в інших групах.
Аналіз виживаності залежно від методики НАХТ переконливо свідчить про переваги комбінованої, що демонструє приклад 3-річної виживаності хворих із розповсюдженими формами ЗПЯ після НАХТ та ПрЦРО — 41,2% порівняно з контрольною групою (10,2%), НАХТ в/в — 15,2%, НАХТ е/а — 26,7%.
Таблиця 13. Безрецидивна виживаність хворих із серозними ЕЗПЯ залежно від методики НАХТ
| Виживаність (міс) | Контроль (без НАХТ) | НАХТ в/в | НАХТ е/а | НАХТ комбінована |
|---|---|---|---|---|
| 12 | 42,1±3,6 | 50,7±3,4 | 68,3±3,7 | 80,1±3,4 |
| 24 | 30,5±5,7 | 42,5±4,7 | 57,8±4,5 | 67,5±5,7 |
| 36 | 10,2±5,4 | 15,2±5,4 | 26,7±5,6 | 41,2±5,4 |
На ефективність терапії істотно впливають такі чинники, як кількість оптимальних і субоптимальних циторедуктивних операцій та ступінь лікувального патоморфозу пухлини, який характеризує ефект первинного лікування. Так, при вираженому лікувальному патоморфозі досягнуто 36,7% 3-річна виживаність хворих із розповсюдженими формами ЗПЯ, при помірному — 17,2%, а при слабкому — лише 12,2%.
Найоб’єктивнішим показником, за яким можна оцінити роль неоад’ювантної терапії в комбінованому лікуванні хворих із дисемінованими формами ЗПЯ, є не загальна, а безрецидивна виживаність, оскільки на загальну виживаність мають безпосередній вплив, разом з іншими прогностичними факторами, і цитостатики, застосовані в другій і третій лініях терапії. Безрецидивна виживаність пацієнток зі ЗПЯ після ПрЦРО у 1-й рік після закінчення спеціального лікування становила 78%, на 2-й — 45,2%, на 3-й — 26,6%, на 4-й — 20,7%, на 5-й — 14,5%, медіана виживаності — 31,9 міс (табл. 14).
З одержаних результатів явно випливає, що хворі з групи НАХТ, незважаючи на гірший прогноз, що був на початку лікування, після закінчення терапії та при відновленні пухлинного росту мали сприятливі перспективи подальшого перебігу хвороби. Аналізуючи вплив різних чинників на виникнення рецидивів або прогресування у хворих із поширеними стадіями ЕЗПЯ, виявили, що для цього процесу істотне значення має характер циторедуктивної операції, ступінь лікувального патоморфозу, ефективність первинного лікування, рівень СА-125 після закінчення терапії.
Таблиця 14. Безрецидивна виживаність хворих зі ЗПЯ після НАХТ
| Інтервал | Безрецидивна виживаність хворих зі ЗПЯ після ПрЦРО | |
|---|---|---|
| n | % | |
| Усього | 516 | 100 |
| 12 | 319 | 61,8±2,7 |
| 24 | 207 | 40,1±3,2 |
| 36 | 113 | 21,9±2,8 |
| 48 | 94 | 18,2±2,6 |
| 60 | 61 | 11,8±2,3 |
| Безрецидивна виживаність хворих після ПрЦРО | ||
| Усього | 857 | 100 |
| 12 | 667 | 78,0±2,7 |
| 24 | 386 | 45,2±3,2 |
| 36 | 227 | 26,6±2,8 |
| 48 | 178 | 20,7±2,6 |
| 60 | 124 | 14,5±2,3 |
При аналізі загальної 5-річної виживаності встановлено, що для всіх хворих після НАХТ вона становила 17,1%. Виявлено значний діапазон віддалених показників лікування пацієнтів цієї групи залежно від стадії захворювання, гістотипу пухлини, радикальності виконаних ПрЦРО.
Так, 5-річна виживаність хворих з ІІВ стадією захворювання становила 57,2% (медіана виживаності — 54,7 міс), з ІІІ стадією — 31,5% (медіана виживаності — 25,6 міс), із IV стадією — всього 17,6% (медіана виживаності —17,3) (р<0,05).
Значно відрізнялися рівні виживаності хворих залежно від обсягу виконаних ПрЦРО: медіана виживаності хворих після стандартних операцій становила 18,7 міс, комбінованих — 23,7 міс, розширених — 27,1 міс, тоді як після паліативних хірургічних втручань тільки — 9,6 міс (р<0,05).
Рівень 5-річної виживаності суттєво залежав і від розмірів залишкової пухлини після ПрЦРО. Так, у пацієнток із ЗПЯ після НАХТ за відсутності макроскопічних ознак резидуальної пухлини загальна 5-річна виживаність становила 36,9%, тоді як за наявності мінімальної залишкової пухлини (<1 см) — 17,1%, а при значній залишковій пухлині (>1 см) — лише 10,2% (р<0,05) (табл. 15).
Таблиця 15. Загальна 5-річна виживаність хворих зі ЗПЯ залежно ПрЦРО
| Інтервал | Загальна 5-річна виживаність хворих | |||||
|---|---|---|---|---|---|---|
| Оптимальна | Субоптимальна | Неоптимальна | ||||
| n | % | n | % | n | % | |
| Вихідні | 361 | 696 | 316 | |||
| 12 | 273 | 75,6±6,7 | 477 | 69,7±3,0 | 201 | 63,6±6,4 |
| 24 | 55 | 63,2±7,6 | 294 | 43,0±3,2 | 109 | 34,7±6,7 |
| 36 | 219 | 48,0±7,9 | 216 | 31,6±3,1 | 67 | 20,4±5,7 |
| 48 | 141 | 40,5±7,8 | 162 | 23,7±2,8 | 45 | 14,3±4,9 |
| 60 | 127 | 36,9±7,6 | 117 | 17,1±2,5 | 32 | 10,2±4,3 |
Ці дані дають позитивну відповідь на головне питання, чи дійсно агресивна хірургічна операція покращує виживаність хворих із ЗПЯ після проміжних комбінованих циторедуктивних втручань.
На основі проведеного аналізу доводиться констатувати невелику кількість парааортальних лімфаденектомій, виконаних у хворих із ЗПЯ. Це пов’язано з технічними проблемами проведення цього втручання та великою кількістю інтраопераційних та післяопераційних ускладнень. Результати розширених операцій вселяють надію, що в майбутньому збільшення кількості показань до регіонарної лімфаденектомії, опанування хірургічної техніки та набуття більшого досвіду виконання таких складних втручань сприятимуть ефективному лікуванню хворих із ЗПЯ, особливо молодшої вікової групи.
Найбільш сприятливий перебіг має захворювання у пацієнтів із герміногенними пухлинами після НАХТ: зальна 5-річна виживаність становила 53,7%, із них у хворих із ІІ стадією — 57,9%, із ІІІ стадією — 46,7%, ІV стадією — 24,6%.
Висновок
Незважаючи на несприятливий прогноз перебігу дисемінованих ЗПЯ, після проведення НАХТ пацієнти з даною патологією отримують обнадійливі перспективи подальшого перебігу захворювання. Загальний ефект НАХТ становить 71,6%, при застосуванні платиновмісних схем — 68,5%, платино- і таксановмісних — 81,8%, інших схем — 70,5%.
Після проведення НАХТ виконували ПрЦРО в оптимальному обсязі у 45,9% хворих, що одержали таксано- і платиновмісні схеми, у 35,5% — платиновмісні та в 18,6% — інші схеми НАХТ (різниця статистично достовірна, р<0,05).
Включення таксанів у схеми НАХТ підвищує ефективність хірургічного втручання порівняно з платиновмісними на 13,3% (р<0,05).
Кращі показники значного лікувального патоморфозу серозних ЕЗПЯ зафіксовано в групах, в яких проводили комбіновану НАХТ: 32,3% — при платиновмісних схемах ХТ та 38,1% — при платино- і таксановмісних схемах порівняно з в/в та е/а платиновмісними схемами — 12,2 та 19,1% відповідно (р<0,05).
Суттєво залежить виживаність хворих від обсягу ПрЦРО: медіана виживаності після стандартних операцій становить 18,7 міс, комбінованих — 23,7 міс, розширених — 27,1 міс, після паліативних хірургічних втручань — лише 9,6 міс (р<0,05).
У пацієнток із ЗПЯ після НАХТ за відсутності макроскопічних ознак резидуальної пухлини в результаті ПрЦРО загальна 5-річна виживаність становила 36,9%, за наявності мінімальної залишкової пухлини (<1 см) — 17,1%, а значної залишкової пухлини (> 1 см) — лише 10,2%(р <0,05).
Проведення НАХТ дозволяє покращати не тільки суб’єктивний статус хворих, але й значно підвищити резектабельність пухлин, частоту виконання оптимальних циторедуктивних операцій, поліпшити віддалені результати лікування пацієнток із ЗПЯ.
Список використаної літератури
1. Бохман Я.В. (2002) Руководство по онкогинекологии, СПб.: Фолиант, 540 с.
2. Блюменберг А.Г. (2002) Диссеминированные формы рака яичников (лечение и факторы прогноза): Дис. … д-ра мед. наук. Москва.
3. Гарин А.М., Горбунова В.А., Бычков М.И. и др. (2000)/Под ред. Н.И. Переводчиковой. Химиотерапия опухолевых заболеваний.
4. Жордания К.И. (2000) Совр. онкол., 2 (2): 51–52.
5. Новикова Е.Г., Корнеева И.А. (2003) Неоадъювантная химиотерапия в лечении распространенного рака яичников. Материалы VII Российской онкологической конференции. М., 27 ноября 2003 г.
6. Bristow R.E., Tomacruz R.S., Armstrong D.K. et al. (2002) Survival effect of maximal cytoreductive surgery for advanced ovarian carcinoma during the platinum era: a meta-analysis. J. Clin. Oncol., 20: 1248–1259.
7. Chambers S.K. (2005) Systematic lymphadenectomy in advanced epithelial ovarian cancer: two decades of uncertainty resolved. J. Nat. Cancer Inst., 97: 548–549.
8. Crawford C.S., Vasey P.A., Paul J. et al. (2005) Does aggressive surgery only benefit patients with less advanced ovarian cancer? Results from an international comparison within the SC0TR0C-1 trial. J. Clin. Oncol., 23: 8802–8811.
9. Gronlund B., Lundvall L., Christensen I.J. et al. (2005) Surgical cytoreduction in recurrent ovarian carcinoma in patients with complete reponse to paclitaxel-platinum. Eur. J. Surgical Oncology; 31: 67–73.
10. Gungor M., Ortac F., Arvas M. et al. (2005) The role of secondary cytoreductive surgery for recurrent ovarian cancer. Gynecol. Oncol., 97: 74–79.
Неоадъювантная химиотерапия у больных со злокачественными опухолями яичника
Резюме. Проведен анализ комплексного лечения 857 больных с запущенными формами злокачественных опухолей яичника (ЗОЯ), которые на первом этапе лечения получили неоадъювантную химиотерапию (НАХТ). Проведение НАХТ позволяет повысить резектабельность опухолей, а также частоту выполнения оптимальных циторедукций, улучшает субъективный статус и качество жизни пациенток со ЗОЯ. Анализ общей 5-летней выживаемости больных со ЗОЯ показал, что для всех пациенток после НАХТ она составляет 17,1%. Размер остаточной опухоли после промежуточной циторедуктивной операции является важнейшим прогностическим фактором, который влияет на выживаемость больных с запущенными ЗОЯ.
Ключевые слова: злокачественные опухоли яичника, неоадъювантная химиотерапия, промежуточная циторедуктивная операция, оптимальная циторедукция.
Neoadjuvant chemotherapy for patients with ovarian malignancies
Summary. The article presents the analysis of complex treatment of 857 patients with advanced ovarian malignancies (OM) who received neoadjuvant chemotherapy (NACT) on first stage of the treatment. NACT allows improving resectability of tumors and increases frequency of cytoreductions, improves objective status and life quality of patients with OM. The analysis of overall 5-year survival of patients with OM was found to be 17,1% after NACT. Residual tumor size after intermediate cytoreductive operation is the most significant predictive factor affecting survival of patients with advanced OM.
Key words: ovarian malignancies, neoadjuvant chemotherapy, intermediate cytoreductive operation, optimal cytoreductive operation.














Leave a comment