Реконструктивно-відновлювальні операції в хірургії місцево-поширених злоякісних пухлин голови та шиї
Процык В.С., Кравец О.В., Трембач А.М., Коробко Е.В., Мосин О.А., Чичула Р.Е.
Резюме. Основна мета даного дослідження — вивчення ефективності застосування різних васкуляризованих комплексів тканин при усуненні дефектів обличчя, шиї, порожнини рота і ротоглотки після комбіновано-розширених хірургічних втручань у 202 хворих місцево-поширеними злоякісними пухлинами голови і шиї. Як пластичний матеріал застосовували різні шкірно-м’язові шматки, комплекси тканин на судинній ніжці, вільну мікрохірургічну трансплантацію тканин. Адаптація до результатів реконструктивно-відновних операцій відзначена у 86,4% хворих з добрими косметичними та функціональними результатами.
Резюме. Основная цель данного исследования — изучение эффективности применения различных васкуляризированных комплексов тканей при устранении дефектов лица, шеи, полости рта и ротоглотки после комбинированно-расширенных хирургических вмешательств у 202 больных местно-распространенными злокачественными опухолями головы и шеи. В качестве пластического материала применяли различные кожно-мышечные лоскуты, комплексы тканей на сосудистой ножке, свободную микрохирургическую трансплантацию тканей. Адаптация к результатам реконструктивно-восстановительных операций отмечена у 86,4% больных с хорошими косметическими и функциональными результатами.

Введение
Злокачественные опухоли головы и шеи в структуре онкологической заболеваемости составляют около 15–20% [1, 2]. У 60—70% больных диагностируют распространенные III—IV стадии заболевания [2, 3].
Основные методы лечения больных местно-распространенным раком головы и шеи — комбинированный и комплексный, которые включают разные комбинации лучевой терапии, химиотерапии и хирургического вмешательства [4–6].
Сложность лечения больных с местно-распространенными опухолями головы и шеи заключается в том, что проведение расширено-комбинированных операций очень часто приводит к образованию больших сложных дефектов, функциональным и эстетическим нарушениям. Поэтому во многих случаях местно-распространенные как первичные, так и рецидивные и/или регионарные метастатические опухоли определяют как неоперабельные вследствие распространенности, сложности или невозможности закрытия послеоперационных дефектов с помощью местных тканей. Это вынуждает хирурга к поиску максимального восстановления анатомических и функциональных нарушений, которые могут возникнуть вследствие радикального хирургического вмешательства [7].
Характер и качество восстановительных операций после удаления злокачественных опухолей определяется многими показателями: размерами и конфигурацией дефектов, дозой ранее проведенного облучения и временем после его окончания, локализацией дефектов, полом, возрастом, соматическим статусом больного, а также выбором пластического материала. Широкий ассортимент пластического материала позволяет выбрать оптимальный вариант реконструкции резецированных тканей в зависимости от локализации дефекта, а также топографо-анатомической и функциональной значимости восстанавливаемого органа. Для восстановления дефектов ткани в области головы и шеи наиболее широко применяют местные лоскуты на питающей ножке, которые формируются из прилежащих к послеоперационному дефекту тканей [8].
Сложные задачи возникают при закрытии дефектов больших размеров у больных, ранее получавших лучевую терапию в радикальных дозах. Успешно восстановить подобные дефекты возможно с помощью кожно-мышечных лоскутов, имеющих большие питающие сосуды, которые обеспечивают жизнедеятельность тканей до возникновения сосудистой связи с ложем дефекта [9]. Для замещения дефектов головы и шеи используют кожно-мышечные лоскуты с сохранением питающей ножки и включением большой грудной мышцы, трапециевидной мышцы, грудинно-ключично-сосцевидной мышцы, височной, подкожной мышцы шеи [10–12].
На протяжении последних десятилетий было создано и исследовано много различных кожно-мышечных лоскутов, большинство из которых полностью удовлетворяют все требования реконструктивных подходов: жизнеспособность, локализацию, удобство, достаточный размер и минимальное повреждение донорской зоны.
Наиболее трудными для замещения считаются дефекты тканей полости рта и ротоглотки вследствие сложного рельефа слизистой оболочки ротовой полости, наличия костных структур, зубов, инфекции в полости рта и ротоглотке, постоянной влажной среды, а также проведенной ранее лучевой терапии [10]. В реконструктивно-восстановительной хирургии дефектов разных отделов полости рта и глотки используют кожно-мышечный лоскут большой грудной мышцы [13, 14]. В случае превалирования объема дефекта со стороны ротоглотки лучше использовать висцеральные трансплантаты — сальниковый или сальниково-кишечный [15, 16]. В связи с технической сложностью микрохирургической аутотрансплантации ее целесообразно применять у больных с относительно благоприятным прогнозом заболевания [17].
Материалы и методы
Проанализированы результаты лечения 202 больных местно-распространенными первичными, рецидивными и метастатическими злокачественными опухолями головы и шеи в возрасте 26–81 года, у которых проведены удаление опухоли и восстановительно-реконструктивные операции.
Для принятия окончательного решения о возможности выполнения радикального хирургического удаления значительного по объему опухолевого поражения всем больным на первом этапе проведено комплексное обследование. Использовали физикальное, ультразвуковое исследование, в том числе и цветную допплерографию, обычную и спиральную компьютерную томографию. Учитывали проведенное ранее лечение, общее состояние и возраст больного. При неполном использовании лучевой терапии, а также при значительном (более 3 мес) интервале после последнего этапа лечения проводили курс полихимиотерапии и лучевой терапии, а операцию — через 3–4 нед. В зависимости от объема хирургического вмешательства, состояния тканей в зоне операции, общего состояния больного планировали наиболее оптимальный метод закрытия послеоперационного дефекта. Особое внимание уделяли правильному выбору донорской зоны, размещению питающей ножки трансплантата. У 156 больных (1-я группа) проведены комбинированные и расширенные операции с пластикой дефектов кожно-жировыми и кожно-мышечными лоскутами на питающей ножке. В этой группе было 129 (82,7%) мужчин и 27 (17,3%) женщин. Средний возраст больных составил 54,8 года. У 46 больных (2-я группа) реконструктивные пластические операции проведены с использованием аутотрансплантации васкуляризированных комплексов тканей (свободная микрохирургическая аутотрансплантация и трансплантация тканей на сосудистой ножке).
Из 46 больных 2-й группы было 40 (87,0%) мужчин и 6 (13,0%) женщин. Средний возраст больных составил 51,4 года. Во всех случаях диагноз был верифицирован гистологически. Результаты микроскопического исследования опухолей свидетельствуют, что плоскоклеточный рак выявлен у 193 (95,5%) больных, меланома кожи — у 4, железистый рак — у 2, хондросаркома нижней челюсти — у 2 и злокачественная амелобластома нижней челюсти — у 1 больного. Наиболее частыми локализациями опухоли у больных в исследованных группах были язык, дно полости рта, альвеолярный отросток нижней челюсти, щека и кожа головы и шеи.
На момент проведения хирургического лечения у больных обеих групп распространенность опухолевого процесса соответствовала III–IV стадиям заболевания. Это требовало выполнения расширенных и комбинированных операций с резекцией 2–3 анатомических областей мягких тканей лица, шеи, лицевого скелета.
У 119 (76,3%) пациентов 1-й группы, пластику послеоперационного дефекта у которых выполняли лоскутами на питающей ножке, диагноз был установлен впервые, 29 (18,6%) поступили на лечение с пролонгацией заболевания после ранее проведенного облучения и хирургического вмешательства. У всех больных выявлены местно-распространенные новообразования. Среди больных 2-й группы с пластикой послеоперационных дефектов свободными аутотрансплантатами и путем транспозиции лоскутов на сосудистой ножке впервые установлен диагноз у 44 (95,6%), местно-распространенный рецидив — у 2 (4,4%) больных.
В зависимости от локализации опухолевого процесса злокачественные новообразования головы и шеи в исследуемых группах представлены в табл. 1. Пациенты с впервые выявленным раком головы и шеи были распределены в соответствии с распространенностью опухолевого процесса согласно Международной классификации злокачественных опухолей TNM-5 (табл. 2). В обеих группах преобладали больные с ІІІ стадией опухолевого процесса. У больных 1-й группы проведены комбинированные, расширенные и реконструктивные пластические операции с использованием кожно-жировых, кожно-мышечных лоскутов и Филатовского стебля. Виды лоскутов, которые использовали для закрытия послеоперационных дефектов у больных 1-й группы представлены в табл. 3.
| Локализация опухоли | 1-я группа | 2-я группа | ||
|---|---|---|---|---|
| n | % | n | % | |
| Язык | 26 | 16,7 | 9 | 19,5 |
| Дно полости рта | 32 | 20,5 | 13 | 28,3 |
| Слизистая оболочка щеки | 13 | 8,3 | 8 | 17,4 |
| Нижняя губа | 19 | 12,2 | 5 | 10,8 |
| Альвеолярный отросток нижней челюсти | 21 | 13,5 | 7 | 15,2 |
| Альвеолярный отросток верхней челюсти | 3 | 1,9 | 1 | 2,2 |
| Передняя небная дужка | 10 | 6,4 | 1 | 2,2 |
| Небная миндалина | 7 | 4,5 | – | – |
| Мягкое небо | – | – | 1 | 2,2 |
| Околоушная железа | 2 | 1,3 | – | – |
| Кожа головы и шеи | 23 | 14,7 | 1 | 2,2 |
| Всего | 156 | 100,0 | 46 | 100,0 |
| Стадия | р TNM | 1-я группа | 2-я группа | ||
|---|---|---|---|---|---|
| n | % | n | % | ||
| ІІІ | T3N0M0, T3N1M0 | 90 | 75,6 | 34 | 77,3 |
| IV | T3N2M0, T4N0M0, T4N1M0, T4N2M0 | 29 | 24,4 | 10 | 22,7 |
| Всего | 119 | 100,0 | 44 | 100,0 | |
| Вид лоскута | Сроки пересадки | |
|---|---|---|
| Одномоментный | Отсроченный | |
| Местные лоскуты | 27 | – |
| Дельто-пекторальный | 27 | – |
| Кожно-мышечный с включением большой грудной мышцы | 15 | – |
| Кожно-мышечный с включением кивательной мышцы | 8 | – |
| Кожно-жировой шейный | 19 | – |
| Кожно-мышечный с включением подкожной мышцы | 17 | – |
| Кожно-мышечный с включением трапециевидной мышцы | 9 | – |
| Комбинация лоскутов | 13 | – |
| Лобно-височный | 12 | – |
| Филатовский стебель | – | 9 |
| Всего (n=156) | 147 | 9 |
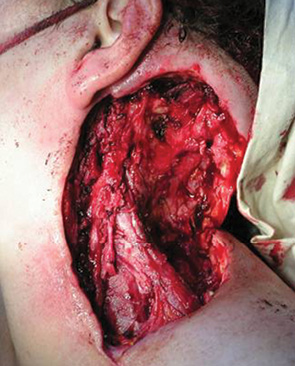
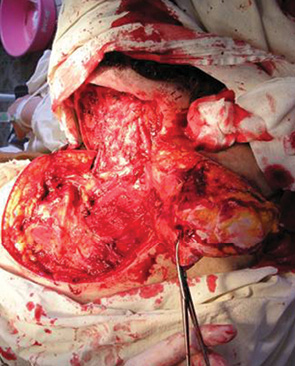
В 27 случаях восстановление мягких тканей дна полости рта и в 6 — мягких тканей лица и шеи проводили с помощью васкуляризированного кожно-мышечного лоскута с включением большой грудной мышцы (рис. 1–3). Этот пластический материал не только прикрывал дефект мягких тканей и кости, но и за счет автономного питания тканей лоскута способствовал хорошему заживлению послеоперационной раны даже у больных, получавших ранее лучевую терапию по радикальной программе. У 22 больных лоскуты сохранили высокую стойкость к инфицированию и зажили первичным натяжением на всем протяжении. У одного больного выявлено расхождение швов на значительном протяжении, которое не повлияло на окончательное заживление раны. Краевой или частичный некроз вследствие нарушения кровоснабжения в питающей ножке трансплантата отмечен у 4 больных.
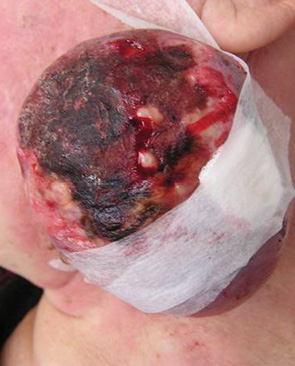
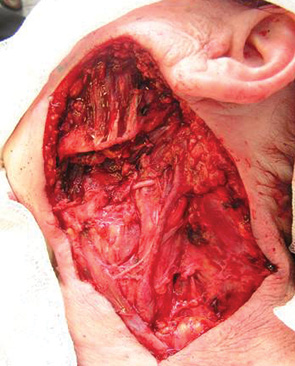
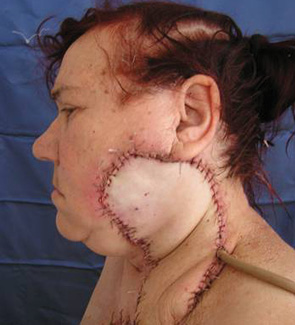
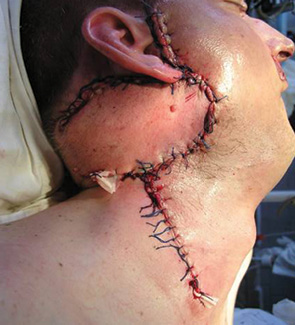
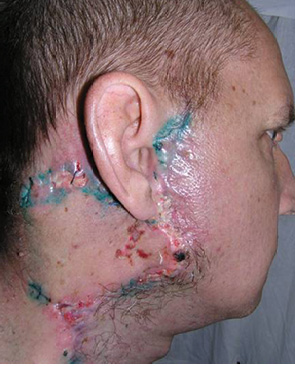
Хорошие косметические и функциональные результаты получены у пациентов с дефектами переднебоковых отделов шеи при использовании лоскута задней части шеи с включением трапециевидной мышцы. У всех 9 больных отмечено полное приживление лоскута (рис. 4–7).
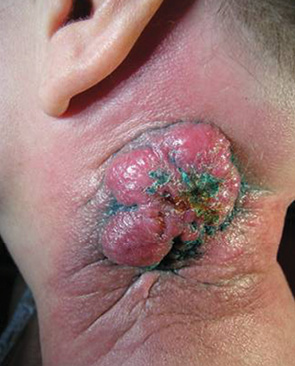
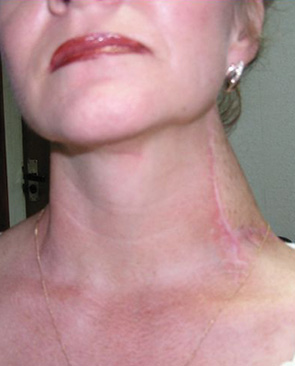
Отмечен хороший эффект при использовании шейного кожно-жирового лоскута и кожно-мышечного лоскута с кивательной мышцей при пластическом восстановлении послеоперационных дефектов как полости рта, так и мягких тканей лица и шеи (рис. 8–10).
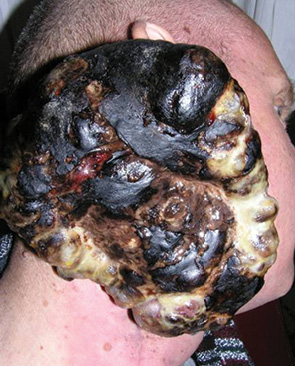
Лобно-височные лоскуты были использованы для замещения послеоперационных дефектов височной, околоушной области и орбиты. У всех больных зафиксировано полное приживление трансплантата.
Реконструкция послеоперационных дефектов свободными аутотрансплантатами и комплексами тканей на сосудистой ножке проведена у 44 больных раком орофарингеальной области и у 2 — с местно-распространенным раком кожи лица (табл. 4). Выбор трансплантата зависел в первую очередь от локализации и объема дефектов тканей. Тонкими пластичными кожно-фасциальными лоскутами проводили реконструкцию частичных дефектов нижней и верхней губы и прилежащих тканей щеки; частичных дефектов боковых отделов языка, дна полости рта, ретромолярной области, прилежащего фрагмента нижней челюсти; субтотальных дефектов языка, дна полости рта при сохранении целостности нижней челюсти; сквозных дефектах щеки, околоушно-жевательной области.
| Вид лоскута | Сроки пересадки | |
|---|---|---|
| Свободная пересадка | Транспозиция на сосудистой ножке | |
| Толстокишечно-сальниковый лоскут | 9 | – |
| Лучевой лоскут предплечья | 11 | – |
| Желудочно-сальниковый лоскут | 3 | – |
| Торакодорзальный лоскут | 4 | – |
| Кожно-мышечный с включением подподъязычной мышцы | – | 10 |
| Кожно-мышечный с включением большой грудной мышцы | – | 5 |
| Щечный лоскут | – | 4 |
| Всего (n=46) | 27 | 19 |
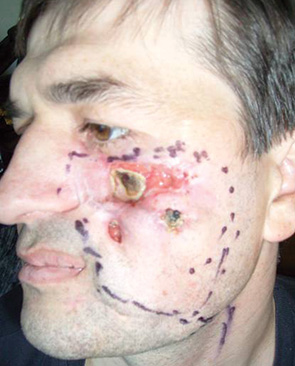
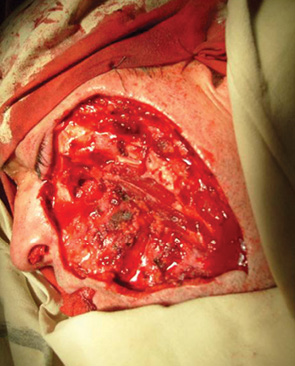
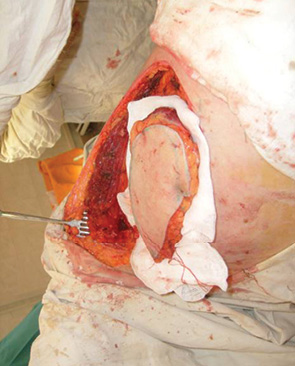
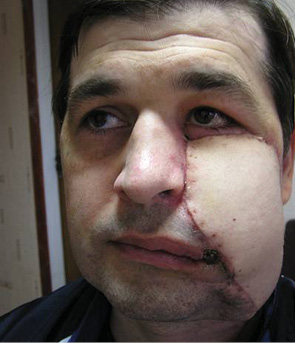
Кожно-мышечными лоскутами, состоящими из дермы и большого массива мышечных структур (большая грудная мышца, широчайшая мышца спины) проводили реконструкцию тотальных дефектов передних отделов языка, дна полости рта, прилежащего фрагмента нижней челюсти и значительных дефектов мягких тканей щеки (рис. 11–14). С помощью висцеральных аутотрансплантатов проводили реконструкцию частичных дефектов корня языка, подвижной части языка, крыло-челюстной складки, боковой стенки глотки, дистальных отделов слизистой оболочки щеки, прилежащего фрагмента нижней челюсти, мягкого неба, небной дужки (рис. 15, 16). В качестве реципиентных артерий при микрохирургической реконструкции тканевых дефектов использовали ветви наружной сонной артерии (лицевую, поверхностную височную, язычную, верхнюю щитовидную артерии), в качестве реципиентных вен — лицевую вену, поперечную вену лица, щитовидную, непосредственно внутреннюю яремную вену. Основной вариант микрососудистых анастомозов — «конец в конец».
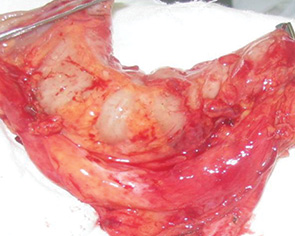
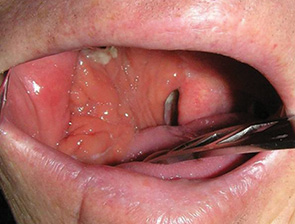
Для изучения эффективности реконструкции послеоперационных дефектов свободными аутотрансплантатами и комплексами тканей на сосудистой ножке была сформирована контрольная группа из 36 больных, которым орофарингопластику проводили с использованием местных лоскутов и кожных лоскутов на питающей ножке. При сравнении основной и контрольной групп по основным прогностическим факторам статистически достоверных отличий не выявлено.
Качество жизни пациентов изучали по трем показателям шкалы функционирования для больных раком головы и шеи PSSHN: нормальность диеты (50–100 баллов), внятность речи (75–100 баллов), питание на людях (75–100 баллов). Оценку качества жизни проводили до начала лечения, через 4 и 8 мес после его окончания.
Для объективной оценки косметического эффекта не использовали балльную систему, а оценивали адаптацию пациента к результату операции: адаптация или ее отсутствие. Основным критерием результативности считали отказ больного от дополнительных приспособлений, маскировочных повязок, косынок после операции. При сравнении пациентов исследуемых групп выявлено, что адаптация к результату операции в 1-й группе больше, чем во 2-й (86,4 ± 5,2% против 63,9 ± 8,0% соответственно, p
Таким образом, установлено, что аутотрансплантация васкуляризированных комплексов тканей при одномоментной реконструкции дефектов орофарингеальной зоны является эффективным методом реабилитации больных местно-распространенным раком полости рта и ротоглотки.
Выводы
Использование кожно-жировых и кожно-мышечных лоскутов позволило выполнить радикальные расширенные и комбинированные операции у больных с III и IV стадией. При обширных дефектах кожи и мягких тканей головы и шеи более эффективным методом их восстановления является одномоментная реконструкция кожно-жировыми или кожно-мышечными лоскутами на питающей ножке.
Разработанные методы реконструкции дефектов орофарингеальной области после комбинированных и расширенных операций свободными трансплантатами и лоскутами на сосудистой ножке обеспечивают высокий функциональный эффект и улучшают качество жизни больных по сравнению с традиционными методами пластики.
Эффективность реконструкции орофарингеальной области свободными трансплантатами и на сосудистой ножке по шкале PSSHN по трем показателям (нормальность диеты, внятность речи, питание на людях) через 8 мес после операции была соответственно на 41,7, 35,0 и 42,5% выше, чем у больных, которым проводили орофарингопластику с использование местных тканей и кожных лоскутов на питающей ножке.
Литература
- 1. Пачес А.И. (2000) Опухоли головы и шеи. Медицина, Москва, 480 с.
- 2. Чиссов В.И., Cтаринский В.В., Петрова Г.В. (2006) Основные показатели онкологической помощи населению России. Состояние онкологической помощи населению России в 2005 г. М., 252 с.
- 3. Щепотін І.Б. (2008) Рак ротової порожнини: організаційні та епідеміологічні аспекти проблеми. Журн. вушних, носових і горлових хвороб, 4: 2–3.
- 4. Любаев В.Л., Пачес А. И., Пустынский И.Н. (2004) Современное состояние проблемы лечения местно-распространенного рака слизистой оболочки полости рта и ротоглотки. Материалы III съезда онкологов и радиологов СНГ. Минск, Т. 1: 75–78.
- 5. Giralt J.L., Gonzalez J. (2000) Preoperative induction chemotherapy followed by concurrent chemoradiotherapy in advanced carcinoma of the oral cavity and oropharynx. Nippon Jibiinkoka Gakkai Kaiho, 103(7): 803–811.
- 6. Machtay M., Rosenthal D.I., Hershock D. (2002) Organ preservation therapy using induction plus concurrent chemoradiation for advanced resectable oropharyngeal carcinoma: a University of Pennsylvania Phase II Trial. Br. J. Oral. Maxillofac. Surg., 40(2): 122–124.
- 7. Матякин Е.Г. (1997) Реконструктивная пластическая хирургия при опухолях головы и шеи. Опухоли головы и шеи: 429–460.
- 8. Пилипюк Н.В., Гобжелянова Т.А., Юрин А.С. (2008) Реконструтивно–восстановительные операции после хирургического лечения злокачественных опухолей головы и шеи. Журн. вушних, носових і горлових хвороб, 4: 91.
- 9. Втюрин Б.М., Цыбырне Г.А., Клим К.И. (1981) Хирургическое лечение рака головы и шеи. Штиинца, Кишинев, с. 48.
- 10. Клочихин А.Л., Кашманов А.Е., Мовергоз С.В. и др. (2003) Пластика дефекта дна полости рта, сектора нижней челюсти и щеки перемещенным кожно-мышечным лоскутом с грудной клетки при операции по поводу местрораспространенного рака. Вопросы онкологии, 6: 768–769.
- 11. Guerrissi J.O., Taborda G.A. (2000) Immediate mandibular reconstruction use of titanium plate reconstructive system and musculocutaneous pectoralis mayor flap. J. Craniomaxillofacial. Surgery., 28(3): 284–285.
- 12. Liu R., Gullane P., Brown D. et al. (2001) Pectoralis major myocutanetous pedicled flap in head and neck reconstruction: retrospective review of indications and results in 244 consecutive cases at the Toronto General Hospital. J. Otolaryngol., 30: 34–40.
- 13. Kimata Y., Uchiyama K., Ebihara S. et al. (2000) Postoperative complications and functional results after total glossectomy with microvascular reconstruction. Plast .Reconstr. Surg., 106(5): 1028–1035.
- 14. Spriano G., Pellini R., Roselli R. (2002) Pectoralis major myocutaneous flap for hypopharyngeal reconstruction. Plast. Reconstr. Surg., 110(6): 1408–1413.
- 15. Кравцов С.А. (2000) Микрохирургическая реконструкция органов орофарингеальной зоны желудочно-сальниковым аутотрансплантатом у онкологических больных: Автореф. дис. … канд. мед. наук: 25 с.
- 16. Ратушный М.В. (2007) Микрохирургическая реконструкция тканей полости рта и глотки толстокишечно-сальниковым лоскутом у онкологических больных: Автореф. дис. … канд. мед. наук.
- 17. Чиссов В.И., Решетов И.В., Кравцов С.А. и др. (2009) 1000 операций микрохирургической аутотрансплантации органов и тканей в онкологии. Рос. онкол. журн., 1: 4–14.














Leave a comment