Гранульозоклітинна пухлина яєчника. Цитоморфологічні та імуноцитохімічні особливості (повідомлення про спостереження та огляд літератури)
Болгова Л.С., Туганова Т.Н., Ярощук Т.М. , Мариненко С.В.
Резюме. За матеріалами зіскрібків із видалених під час операції гранульозоклітинних пухлин яєчника у 4 жінок різного віку представлено особливості їх цитоморфологічних та імуноцитохімічних ознак. За наявності структур, характерних для епітеліальних пухлин, підтверджено їх мезенхімальний генез.
Резюме. По материалам соскобов из удаленных во время операции гранулезоклеточных опухолей яичников у 4 женщин различного возраста представлены особенности их цитоморфологических и иммуноцитохимических признаков. При наличии структур, характерных для эпителиальных опухолей, подтвержден их мезенхимальный генезис.
 Введение
Введение
Гранулезоклеточные опухоли яичников (ГКОЯ) относятся к неэпителиальным новообразованиям полового тяжа яичников и входят в состав группы гранулезо-стромальных опухолей. Наиболее вероятным источником развития данных опухолей является гранулеза примордиальных фолликулов яичника в результате нарушения гормонального равновесия [17]. Опухоли составляют, по данным разных авторов, от 0,6 до 7,5% всех солидных новообразований яичников [2, 15, 16]. Д.И. Головин характеризует ГКОЯ как гормональноактивные опухоли, имеющие мезенхимное происхождение, но эпителиальное строение. ГКОЯ, или фолликуломы (гранулезоклеточный рак, гранулезоэпителиома, фолликулоидный рак, цилиндрома, аденома граафова пузырька, феминизирующая мезенхимома яичника), достаточно редки и в связи с этим малоизучены [12]. В то же время они являются самыми частыми гормонопродуцирующими новообразованиями яичников [16]. Заболевание встречается в любом возрасте, однако большинство случаев выявляется в 40–60 лет [15]. В 1977 г. R.E. Scully выделил 2 варианта ГКОЯ — взрослый и ювенильный [19]. Взрослый вариант составляет около 95% всех ГКОЯ [16]. Микроскопически в гистологических препаратах ГКОЯ взрослого типа выделяют 2 варианта опухоли: макрофолликулярный и лютеинизированный. Первый вариант чаше встречается у молодых женщин. В части наблюдений опухоль достигает больших размеров и содержит крупные полости, иногда с серозной, муцинозной или геморрагической жидкостью. В составе ГКОЯ отмечают солидно-медуллярные, фолликулоидные, трабекулярные, диффузные, цилиндроматозные и псевдоаденоматозные структуры, которые могут переходить друг в друга. Наиболее часто встречается вариант солидной фолликуломы. Наряду с этим в составе ГКОЯ обнаруживают мелкокистозные, крупнокистозные, одно- и многокамерные кисты. Крупнокистозные полости бывают гладкостенными или выстланными псевдопапиллярными структурами. Отмечается, что ГКОЯ являются необычайно полиморными по строению. В одной опухоли можно найти самые разнообразные структуры, расположенные в миксоматозной строме. Встречаются комбинации ее с текомой.
Для гистологического диагноза ГКОЯ характерны отсутствие в препаратах функциональной дифференцировки гранулезных клеток, наличие митозов и васкуляризации гранулезного слоя. При втором лютеинизированном варианте или липидной фолликуломе для опухолевых клеток характерно диффузное расположение или в виде групп, различных по размеру и форме. Клетки в гистологических препаратах чаще расположены в интенсивно васкуляризованной строме. Клетки — обычно с развитой, оптически пустой цитоплазмой с четко очерченной границей, в цитоплазме могут выявляться различного размера капли эозинофильного секрета. Строма гранулезоклеточной опухоли в гистологических препаратах содержит 2 компонента: неспецифический фиброзно-ангиоматозный и специфический, состоящий из функционально активизированных тека-клеток, обладающих иногда выраженной лютеинизацией цитоплазмы. Степень злокачественности гранулезоклеточной опухоли часто установить сложно. Одним из прогностически неблагоприятных параметров является размер опухоли более 5 см и наличие инвазии [4, 9].
Гранулезоклеточная опухоль ювенильного типа встречается чаще в возрасте от 1 года до 30 лет и клинически проявляется ранним половым созреванием, очень редко с сопутствующим андрогенным эффектом. У 10% больных данная опухоль сочетается с асцитом. В 98% случаев опухоль односторонняя, диаметром от 10 до 23 см. Обычно гранулезоклеточная опухоль ювенильного типа отличается более благоприятным клиническим течением, но описаны единичные случаи с выраженной генерализацией процесса. Явные морфологические критерии злокачественности в ней обычно не прослеживаются. Наличие или отсутствие признаков инвазии опухоли является, соответственно, подтверждением или исключением злокачественности роста. Рецидив, если и возникает, то, как правило, в течение первых 3 лет после операции. Микроскопически определяются 2 компонента ГКОЯ ювенильного типа — диффузный и фолликулярный. В последнем встречаются полости разной величины, выстланные либо одним слоем уплощенных или кубических клеток с овальными ядрами, мелкозернистым хроматином и многочисленными фигурами митоза, либо — многослойной выстилкой, в периферических отделах которой в виде частокола располагаются высокие призматические клетки. Фолликулы обычно окружены тека-клетками. Постепенная пролиферация опухолевых клеток приводит к исчезновению полостей в фолликулах, и опухоль приобретает преимущественно солидное строение с присутствием крупных полигональных или веретеновидных тека-клеток. В части препаратов определяются скопления призматических клеток, формирующих трабекулярные и железистые структуры. Цитоплазма опухолевых клеток содержит разное количество липидов, хотя встречаются клетки и с эозинофильной цитоплазмой. Ядра опухолевых клеток овальные, эухроматичные, изредка гиперхромные. По мнению некоторых авторов, почти никогда не выявляются ядра в виде «кофейных зерен». Другие авторы отмечают, что более чем у 60% больных в ядрах опухолевых клеток определяются щели, придающие им своеобразный вид «кофейных зерен» [9].
Гистологическое строение ГКОЯ напоминает одну из стадий развития фолликула. Большинство их обладает способностью продуцировать эстрогены. Это обычно обусловливает клиническую картину с симптомами «омоложения» [3, 8, 10].
ГКОЯ, как правило, считаются новообразованиями «низкой степени злокачественности», видимо, из-за характерной для ГКОЯ взрослого типа склонностью к позднему возникновению рецидивов и метастазов. У 30% пациенток рецидив возникает в срок до 5 лет после оперативного вмешательства, у остальных — позднее [4, 14, 15]. Невзирая на то, что ГКОЯ ювенильного типа отличаются более благоприятным прогнозом, в 5% наблюдений отмечается агрессивное течение, когда быстро развивается рецидив и прогрессирование заболевания в течение 2–3 лет после установления диагноза [7].
Благоприятный прогноз и хорошие отдаленные результаты лечения достигаются при ранней диагностике и своевременном адекватном лечении, как и при всех онкологических заболеваниях. Для выработки оптимальной лечебной тактики необходимы такие данные о ГКОЯ, как установленный гистологический вариант в виде макро-, микрофолликулярной, розетко-, псевдожелезистой, тубулярной и диффузной формы. Также необходимо установить степень дифференцировки опухоли, помня о том, что при взрослом типе выделяются высокая, промежуточная и низкая степени, при ювенильной — признаки степени дифференцировки клеток обычно не выявляются. При исследовании препаратов отмечают слабую, умеренную и выраженную степень ядерной атипии, митотическую активность, выраженность некротических изменений, наличие сосудов. Для выявления прогностического статуса определяют также степень пролиферативной активности гранулезоклеточных элементов. Так, при проведении ДНК-проточной цитометрии установлено, что высокая пролиферативная активность клеток ГКОЯ взрослого типа прогностически более неблагоприятна [6, 13].
Опухолевые клетки могут расти: беспорядочно (диффузный вариант опухоли); в виде длинных тяжей, часто с двухрядным расположением клеток (трабекулярный вариант); в виде ритмичных фигур (гириформный и муаровый варианты); островков (инсулярный вариант). Между опухолевыми клетками формируются небольшие полости, содержащие остатки разрушенных элементов, гиалиновые капли — тельца Колла — Экснера [3, 9]. По периферии комплексов опухолевой паренхимы палисадами располагаются базалоидные элементы. Обычно во всех опухолях обнаруживается сочетание большинства из описанных структур. В редких случаях можно увидеть скопления полиморфных многоядерных клеток, напоминающих клетки саркомы, но, по-видимому, не имеющих прогностического значения. Иногда выявляются тубулярные структуры, не отличимые от таковых в сертолиоме.
Необходимо подчеркнуть, что ГКОЯ при всех своих структурных типах и степенях дифференцировки имеют различный злокачественный потенциал со способностью к экстраовариальному распространению или рецидиву даже после полного удаления опухоли. Отдаленные метастазы встречаются нечасто.
Вариабельность морфологических структур, а нередко и трудности гистологической и клинической диагностики не позволили до настоящего времени прийти к общепринятому мнению о критериях вариантов строения и прогностических факторах, определяющих дальнейшее течение заболевания. В связи с этим особенно актуальными являются поиски путей улучшения клинической и морфологической диагностики ГКОЯ и разработка комплекса факторов, определяющих прогноз новообразований яичников [12, 18].
Цитологическое исследование, являясь современным, доступным и высокоинформативным методом диагностики, позволяет внести свой определенный вклад в повышение эффективности цитологической диагностики злокачественных и доброкачественных опухолей яичников по изучению преимущественно структурных признаков клеток, их компонентов и иммуноцитохимических особенностей [1, 5, 11, 20, 21].
Материал и методы
Изучены цитологические препараты, приготовленные из соскобов удаленных опухолей яичников 4 пациенток в возрасте 13; 14; 54 и 58 лет, которые обследовались и лечились в клинике Национального института рака. Препараты окрашивали по методу Паппенгейма. Для определения генезиса опухоли проведены также иммуноцитохимические реакции с моноклональными антителами (МкАТ) фирмы «Dako»: цитокератин 7, 20 (СК7, СК20), панцитокератин (АЕ1/АЕ3), эпителиальный антиген (Веr-EP4) и виментин.
Результаты исследований
Исследованные цитограммы ГКОЯ нескольких больных отличались многообразием количества клеток небольших размеров, их структурным компонированием, наличием, количеством и окрашиваемостью фонового компонента. Можно наблюдать в препаратах одной и той же опухоли различные места, где выявлялось разное количество оксифильной субстанции и неодинаковое ее окрашивание.
Во всех препаратах отмечалась высокая клеточность. При этом клетки располагались во всех полях зрения в скоплениях, тяжах и разрозненно.
Клетки в соскобах гранулезоклеточных опухолей относительно мелкие, чаще округлые, реже — вытянутые, приближались по форме к призматическим. Большая часть клеток имела истонченную слабооксифильную цитоплазму, которая часто сливалась с таким же фоном препаратов. Ядерно-цитоплазматическое соотношение сдвинуто в сторону ядра (рис. 1).
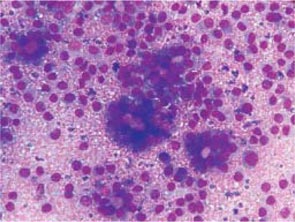
Рис. 1. Розеткоподобные структуры с оксифильной субстанцией и отдельно расположенные опухолевые клетки х 400
Клетки часто формировались в виде небольших розеток, железистоподобных комплексов, фолликул с характерным раположением клеток вокруг округлой оксифильной субстанции или «пустот» (рис. 2). Розеткоподобные группы отличались размерами, ядра в них часто располагались в виде «частокола» вокруг округлой формы оксифильной субстанции различной интенсивности окрашиваемости, названной колл-экснеровскими включениями. Подобное расположение клеток придает цитограммам определенное своеобразие, характерный вид и является одним из важных дифференциально-диагностических признаков. Выявлялись также единичные тубулярные структуры (рис. 3). Часто преобладали солидные скопления, комплексы и тяжи своеобразных клеток призматической или кубической формы. Цитоплазма в них нежной голубоватой или более интенсивной окраски округлой или несколько удлиненной формы. Часть клеток — с вуалевидной вакуолизированной цитоплазмой, содержащей базофильные гранулы. Такие структурные комплексы напоминают эпителиальную опухоль (рис. 4). Часть розеткоподобных структур представлена сохранными клетками, по форме соответствующими призматическим, которые располагались в виде венчика. Ядра в них прилегали непосредственно к центру, в то время как цитоплазма размещалась по периферии комплексов. Данные структуры имели преимущественно округлую форму, значительно реже — удлиненную, вытянутую. Местами клетки располагались скоплениями и в виде однослойных пластов (см. рис. 4). Но и в пластах клетки тяготели к определенной концентрации в виде розеток. В местах скоплений клетки с овальными ядрами тесно прилегали друг к другу, часто наслаивались и представляли собой нагромождения клеток. Цитоплазма данных клеток светло-голубая, неправильно округлая с неровными контурами. В небольшой части клеток содержались крупные или мелкие вакуоли. В клетках, которые по структурным признакам можно было отнести к более зрелым, цитоплазма имела фестончатый, как бы набухший, край. Особенность цитоплазмы ГКОЯ в цитологических препаратах состоит в том, что она тонкая, слабооксифильная, с различной степенью выраженности лизиса и часто сливалась с общим фоном препарата. При этом в части клеток она тонкая с усиленным базофильным характерным фестончатым краем и мелкой вакуолизацией (см. рис. 4).
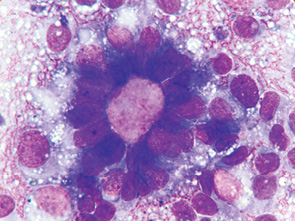
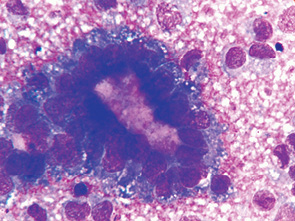
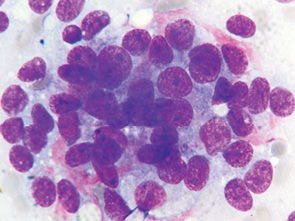
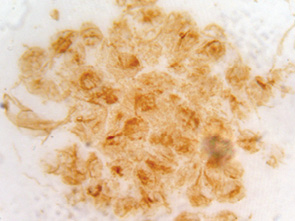
Ядра округлой, овальной, изредка вытянутой формы, в большинстве клеток умеренно гиперхромные несколько варьировали по размеру и форме. В клетках овальной или неправильной формы ядра чаще располагались центрально, в клетках призматической формы — эксцентрично. Ядра клеток частью плотно прилегали, вдавливаясь краями или наслаивались, чаще по центру скоплений и комплексов. В клетках так называемых розеток и фолликул ядра располагались эксцетрично, а в изолированных клетках — примущественно центрально. Контуры ядерной оболочки преимущественно четкие, неровные.
Структура хроматина большинства ядер отличалась неравномерностью, была мелкозернистой, сетчатой или мелкоглыбчатой. В небольшой части ядер выявлялись бороздки. Местами интенсивность гиперхромии ядер варьировала в пределах комплекса или тяжа клеток (рис. 5).
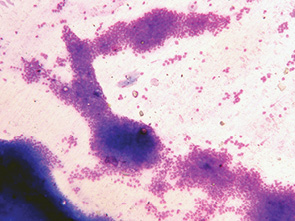
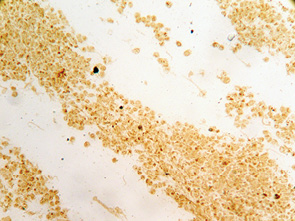
В большинстве ядер определялись от 1 до 3 полиморфныех ядрышек, которые в небольшой части ядер прилегали к ядерной мембране, но чаще располагались центрально (рис. 6).
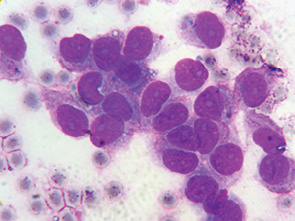
Иногда среди клеток с овальными ядрами встречались вытянутые клетки с сигароподобными гиперхромными ядрами, по структуре напоминающие тека-клетки (рис. 7, 8).
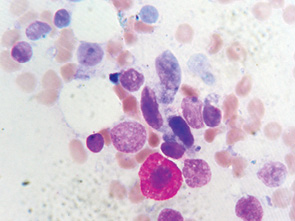
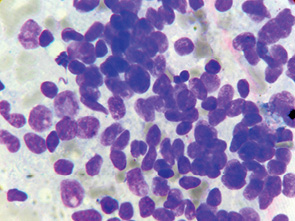
После проведения иммуноцитохимических реакций с МкАТ Ber-EP4, CK7, CK20, панцитокератин установлено, что опухолевые клетки имели отрицательную реакцию. В то же время выявлена положительная экспрессия виментина, что подтверждает мезенхимальную природу опухолевых клеток (см. рис. 4 б, 5 б).
Заключение
Общим для цитограмм ГКОЯ разных больных является наличие большого количества разрозненно расположенных на оксифильном фоне клеток с тонкой слабооксифильной цитоплазмой и своеобразных комплексов в виде розеткоподобных, макро- и микрофолликулоподобных образований, тяжей, в центре которых выявлялась оксифильная субстанция, названная колл-экснеровскими включениями. Определяются отдельные веретенообразные гиперхромные тека-клетки. Ряд выполненных иммуноцитохимических реакций подтвердил мезенхимальную природу ГКОЯ.
Литература
1. Гилязутдинов И.А., Хасанов Р.Ш. (2004) Опухоли гормонозависимых и гормонопродуцирующих органов. М.: МЕДпресс-информ.: 218–246.
2. Григорук О.Г. и др. (2007) Возможности пункционного метода диагностики при злокачественных опухолях яичников. Проблемы клинической медицины, 2: 81–85
3. Елманов А.В., Жаркова О.В., Колесникова Я.М., Вержбицкая Н.Е. (2011) Гранулезоклеточная опухоль яичников с множественными метастазами в кожу (клинический случай). Сибирский онкологический журнал, 5(47): 87–89.
4. Ивинская И.В. (2003) Роль цитологических исследований в диагностике опухолей яичников. Материалы V Всероссийского съезда клинических цитологов. 14–17 июня 2003 г. Новости клинической цитологии России, 7(1–2): 55.
5. Кержковская Н.С., Богатырёв В.Н., Жордания К.И., Паниченко И.В. (2003) Данные ДНК-проточной цитометрии и прогноз гранулезоклеточных опухолей яичников взрослого и ювенильного типа. Материалы V Всероссийского съезда клинических цитологов России (18). Новости клинической цитологии России, 7(1–2): 56.
6. Кержковская Н.С., Жордания К.И., Каллистов В.Е., Анурова О.А. (2004) Послеоперационная химиотерапия гранулезоклеточных опухолй яичника. Акушерство и гинекология, 1: 39–44.
7. Клиническая онкология: Руководство для врачей. Под ред. В.П. Козаченко. (2005) М.: ОАО «Изд-во Медицина»: 341–342.
8. Ковригина А.М., Анурова О.А., Шабанов М.А., Богатырёв В.Н. (1998) Цитоморфологическая диагностика гранулезоклеточной опухоли яичника. Клиническая лабораторная диагностика, 1: 37–39.
9. Краевская И.С. (1978) Рак яичника. М.: Медицина: 119–120.
10. Лагутина Е.Н., Сергеева Т.С. (2003) Значение цитологического метода в интраоперационной диагностике опухолей яичников. Материалы V Всероссийского съезда клинических цитологов. 14–17 июня 2003 г. Новости клинической цитологии России, 7(1–2): 62.
11. Новикова Е.Г., Белоус Т.А., Завалишина Л.Э., Логвинов Ю.И. (2001). Пути улучшения клинико-морфологической диагностики и мониторинга гранулезоклеточных опухолей яичника. Материалы научно-практической конференции «Новые подходы к скринингу, диагностике и лечению опухолей яичников», Великий Новгород, 17–18 мая 2001 г.; Санкт-Петербург, 2001.
12. Паниченко И.В., Богатырёв В.Н., Жорданиа К.И., Паяниди Ю.Г. (2003) Цитометрическое определение содержания ДНК в клетках опухолей яичников и его роль в прогнозе заболевания. Материалы V Всероссийского съезда клинических цитологов. 14–17 июня 2003 г. Новости клинической цитологии России, 7(1–2): 59.
13. Сидорова И.С., Саранцев А.К., Марутян М.Р. (2004) Анализ причин запоздалой диагностики рака яичников. Акушерство и гинекология, 3: 34–37.
14. Соколов И.В., Степанов В.А. (2004) Позднее метастазирование гранулезоклеточной опухоли яичника. Современная онкология, 6(1): 32.
15. Тюляндин С.А., Кержковская Н.С., Стрельцова О.Н. (2009) Герминогенные и гранулезоклеточные опухоли яичников. Практическая онкология, 10(2): 111–116.
16. Шматкова В.В., Порханова Н.В., Кержковская Н.С. и др. (2004) Совершенствование методов ранней диагностики и прогноза рецидивов неэпителиальных опухолей яичников. Вестник московского онкологического общества, 1:54.
17. Яровая Н.Ю., Мельникова Н.В. (2009) Дооперационная цитологическая диагностика новообразований яичника. Новости клинической цитологии России, 13(1–2): 17–19.
18. Scully R.E. (1977) Ovarian tumors. American Journal of Pathology, 87(3): 687–720.
19. Kavuri S., Kulkarni R., Reid-Nicholson M. (2010) Granulosa Cell Tumor of the Ovary: Cytologic Findings. Acta Cytologica, 54 (4), 551–559.
20. Balachandran I., Ju J., Broman J. (2010) Fine Needle Aspiraton of Metastatic Adult Granulosa Cell Tumor of the Ovary: A Case Report. Acta Cytologica, 54 (5), 933–938.
21. Idrovo Mora F., Toldos Gonzales O., Perez Barrioz A. et al. (2010). Fast dagnosis of Liver Metastasis Adult Granulosa Cell Tumor Using Fine Needle Aspiration Cytology. Acta Cytologica, 54 (5), 1080–81.














Leave a comment