Місце неоад’ювантної поліхіміотерапії у комплексному лікуванні хворих на рак грудної залози

Проаналізовано стан захворюваності та смертності на рак грудної залози в Україні та віддалені результати лікування 6001 хворих, які отримували терапію у відділенні пухлин грудної залози та її реконструктивної хірургії Національного інституту раку з 1990 по 2009 р. Доведено доцільність застосування неоад’ювантної протипухлинної терапії та показано еволюцію хірургічних методів лікування у хворих на рак грудної залози за даними Національного інституту раку. Наведено принципи сучасного підходу до планування комплексного лікування хворих на рак грудної залози, спрямовані на підвищення його ефективності та покращання якості життя пацієнток.
Вступ
Рак грудної залози (РГЗ) — найбільш поширене онкологічне захворювання серед жіночого населення. За даними ВООЗ, кожного року у світі реєструють більше 1,2 млн нових випадків РГЗ та помирають від нього понад 400 тис. жінок. Найвищі показники захворюваності відмічені в економічно розвинених країнах Європи, у США, Канаді, Австралії (75,0–120,0 на 100 тис. населення), найнижчі — в країнах Сходу. За даними Національного канцер-реєстру, у 2008 р. в Україні зареєстровано 16 507 нових випадків захворювання, загальна кількість померлих жінок від РГЗ становила 7902 [7]. Постійне зростання показників захворюваності на РГЗ підтверджує актуальність досліджень цієї проблеми. Захворюваність та смертність від РГЗ в Україні за останні роки наведені в табл. 1.
| Показники за роками (абс. числа) | |||||
|---|---|---|---|---|---|
| 2004 | 2005 | 2006 | 2007 | 2008 | |
| Загальна кількість випадків захворювання | 15 183 | 16 346 | 16 042 | 16 195 | 16 507 |
| Звичайний (грубий) показник захворюваності на 100 тис. населення | 59,5 | 64,5 | 63,7 | 64,7 | 65,7 |
| Загальна кількість померлих | 7565 | 7891 | 7826 | 7743 | 7969 |
|
Звичайний (грубий) показник смертності на 100 тис. населення |
29,7 | 31,1 | 31,1 | 30,9 | 31,7 |
Враховуючи кількість осіб, що захворіли у репродуктивному (38,2%) та працездатному віці (39,4%), актуальним на сьогодні є не тільки підвищення ефективності протипухлинної терапії, а й покращання якості життя хворих на РГЗ, тому важливим у сучасному комплексному лікуванні цього захворювання є питання збереження органа. Проте, незважаючи на успіхи в ранній діагностиці РГЗ, майже у 25% хворих на момент встановлення діагнозу реєструються місцево-поширені форми захворювання (МП РГЗ), а саме: пухлини грудної залози розміром >5 см; пухлини менших розмірів, що займають більшу частину залози (при малому її розмірі), або пухлини будь-яких розмірів, що поширюються на шкіру, на грудну стінку, або супроводжуються метастазами в аксилярні, внутрішні грудні та надключичні лімфатичні вузли на боці ураження [1, 2, 3]. Ця категорія хворих потребує довготривалого лікування [2, 6], яке складається із передопераційної (неоад’ювантної) поліхіміотерапії (НПХТ), оперативного втручання та післяопераційної (ад’ювантної) протипухлинної терапії [2, 4–6]. Показники 5-річної виживаності при МП РГЗ коливаються від 27 до 50% та більшою мірою залежать від ступеня первинного розповсюдження пухлинного процесу та адекватності проведеної протипухлинної терапії [1, 2, 4–6].
Зацікавленість проблемою передопераційної системної протипухлинної терапїї постійно зростає, тому що неоад’ювантне лікування при РГЗ дозволяє зменшити обсяг хірургічного втручання та створює сприятливі умови для виконання органозберігаючих або відновлюючих операцій у частини хворих [1–3, 5, 6]. Хірургічний метод лікування ще дотепер залишається самим вагомим компонентом у комплексному лікуванні хворих на РГЗ. За останнє десятиріччя відбулися кардинальні зміни тактики ведення та лікування пацієнток, хворих на РГЗ. Поступово, з розвитком клінічної онкології, хірургічне лікування зменшується за обсягом від радикальних та модифікованих мастектомій до квадрантектомій та туморектомій (лампектомій). Для запобігання генералізації захворювання зменшення обсягу видалених тканин при злоякісних пухлинах грудних залоз повинно доповнюватися адекватними системними та локорегіонарними протипухлинними заходами. Метою проведення неоад’ювантного лікування є саме зменшення розмірів первинної пухлини та її регіонарних метастазів, що дозволяє перевести первинно нерезектабельний РГЗ у резектабельний [1, 3, 5]; підвищення абластики під час операції та зниження ризику розвитку мікрометастазів. Визначення чутливості пухлини до цитостатиків (відповіді пухлини на лікування), виявлення резистентних форм захворювання з метою планування адекватної ад’ювантної ПХТ також є можливими після проведення НПХТ та дозволяє збільшити загальну та безрецидивну виживаність, покращити якість життя хворих на РГЗ [3, 5]. Найчастіше при комплексному лікуванні хворих на РГЗ застосовують схеми НПХТ з використанням антрациклінів — FAC , FEC, AC , CAF [2, 3, 5, 6].
Об’єкт і методи дослідження
У Національному інституті раку з метою вивчення ефективності комплексного лікування проводили аналіз віддалених результатів протипухлинної терапії 6001 хворої на РГЗ, що отримували протипухлинне лікування за період з 1990 по 2009 р. (ретроспективний аналіз). З метою визначення ролі та місця НПХТ при комплексному лікуванні пацієнтів із РГЗ були проаналізовані перебіг захворювання та результати комплексного лікування 589 хворих на РГЗ ІІ—ІІІ стадії (віком від 32 до 65 років), які лікувалися в Національному інституті раку у 2000–2006 рр. Розподіл хворих досліджуваних груп за стадіями представлено в табл. 2.
| Стадія РМЗ | 1-ша група |
2-га група |
Контроль | Всього |
|---|---|---|---|---|
| ІІA | 42 | 38 | 95 | 175 |
| ІІБ | 38 | 85 | 49 | 172 |
| ІІІA | 16 | 93 | 20 | 129 |
| ІІІБ | 22 | 67 | 24 | 113 |
| Всього | 118 | 283 | 188 | 589 |
Всі досліджувані були розподілені на три групи. Дві групи включали в себе пацієнток, у яких комплексне лікування починалося із НПХТ (4 курси з інтервалами у 3 тиж). В третій (контрольній) групі — 188 пацієнток — радикальне лікування починалося з оперативного втручання (радикальна мастектомія або квадрантектомія грудної залози з реґіонарною). Дві основні групи розрізнялися тим, що одним пацієнткам у неоад’ювантному режимі проводили ПХТ за схемою CMF (1-ша група — 118 хворих), іншим (2-га група — 283 хворих) — ПХТ з препаратами антрациклінового ряду (схеми АС, FAC тощо). У хворих всіх груп були проаналізовані обсяги виконаних оперативних втручань та віддалені результати комплексного лікування.
Результати дослідження
Аналізуючи показники виживаності в залежності від стадії та методів неоад’ювантної протипухлинної терапії, було встановлено, що при лікуванні хворих на РГЗ ІІА стадії найкращі результати відмічали у контрольній (без НПХТ) та 1-й групі (НПХТ за схемою CMF) (92,63±5,3% та 90,48±7,9% відповідно), показники 5-річної виживаності практично не відрізнялись. У 2-й групі (НПХТ за схемами з використанням антрациклінів) показники 5-річної виживаності були нижчими — 81,58 ± 6,3 % (p
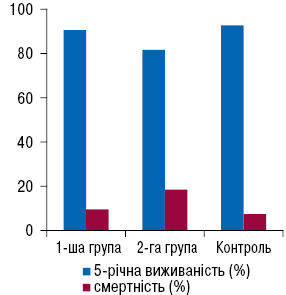
Дещо інша картина спостерігалась у пацієнтів з ІІБ стадією. Найкращі показники 5-річної виживаності були в 1-й групі — 86,84±5,7%. У 2-й групі, де застосовувались препарати антрациклінового ряду, 5-річна виживаність становила 82,35±8,1% (Р1–2?0,05). Показники контрольної групи були найгіршими — 77,55±4,1% (Р1-К?0,05) (див. рис. 2), але різниця показників віддаленої виживаності між дослідними групами не є достовірною. Важливо, що в групах хворих на РГЗ, де застосовували НПХТ, операції із збереженням органа проводили у 17,8% випадків частіше.
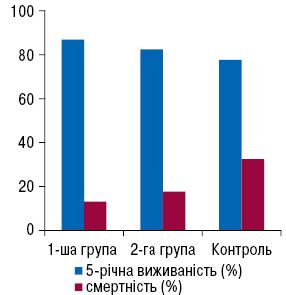
Таким чином, при РГЗ ІІБ стадії доцільно застосовувати НПХТ, схеми якої необхідно корегувати, враховуючи сучасні вимоги до планування протипухлинної терапії РГЗ (St. Gallen — 2009 р.), а саме — шляхом визначення категорій ризику та чутливості до гормонотерапії. НПХТ за схемою CMF може бути ефективною при низькому та проміжному ризику захворювання за необхідності зменшення розміру пухлини перед проведенням заощадливих операцій та зниження ризику кардіотоксичності хіміопрепаратів. Ми вважаємо, що схему CMF доцільно також використовувати при Nx (за неможливості диференціювання стану реґіонарних лімфатичних вузлів). У випадках високого ризику поганого прогнозу захворювання лікування треба починати з НПХТ із використанням препаратів антрациклінового ряду.
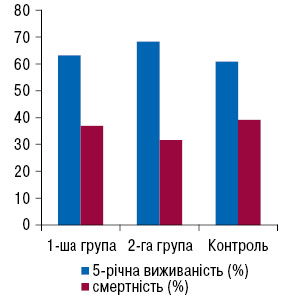
У пацієнток з РГЗ III стадії найкращі результати лікування відмічені в групі з використанням в неоад’ювантному режимі антрациклінів (5-річна виживаність становила 68,33±8,3%). У 1-й групі та в групі контролю виживаність була нижчою (63,16±8,7% та 58,87±6,9% відповідно) (див. рис. 3). Слід відмітити, що при застосуванні схем ПХТ з використанням препаратів антрациклінового ряду частота об’єктивної відповіді пухлини та уражених регіонарних лімфовузлів на лікування була значно вищою, що дозволило пацієнтам 2-ї групи у 12% випадків частіше виконувати ОЗО з досягненням чистих меж резекції.
Таким чином, при РГЗ IІІ стадії доцільно застосовувати НПХТ за схемами з використанням антрациклінів; при поганому прогнозі захворювання та високому ризику прогресування є також необхідність у використанні препаратів таксанового ряду та, за показаннями, таргетної терапії. Обов’язковою умовою при застосуванні НПХТ повинно бути досягнення позитивного об’єктивного результату (відповіді пухлини, наявності у неї чутливості до проведеного лікування) [2, 3, 6]. Відомо, що ПХТ при резистентних пухлинах супроводжується відсутністю лікувального ефекту, а втрата часу на її проведення може бути причиною генералізації та метастазування пухлинного процесу.
При первинно неоперабельному РГЗ (Т4N0–2M0, T0–4N3M0) НПХТ застосовується з метою найбільш ефективної дії на пухлинне вогнище та реґіонарні метастази та сприяє створенню умов для виконання в подальшому радикальної операції. Разом з тим стає можливою оцінка індивідуальної чутливості до проведеного цитостатичного лікування (корекція або подальша інтенсифікація ад’ювантної протипухлинної терапії).
За даними Національного інституту раку, застосування НПХТ не впливає значно на віддалені результати лікування хворих на РГЗ. Відмічено, що при її проведенні різниця показників 5-річної виживаності в залежності від ступеня поширеності пухлинного процесу становить 3–6%, що співпадає з даними світової літератури та результатами рандомізованих досліджень. Але дуже важливою є можливість після застосування НПХТ зменшення розмірів пухлини та її реґіонарних метастазів, що сприяє розширенню показань до заощадливих операцій.
Питання збереження грудної залози завжди залишається актуальним, вважаючи важливість психосоціального фактора у повній реабілітації хворих. Все більша кількість пацієнток, особливо репродуктивного віку відмовляється від повного видалення грудної залози та наполягає на збереженні органа. Проведення НПХТ є суттєвим фактором у вирішенні цієї проблеми. Завдяки широкому впровадженню неоад’ювантної протипухлинної терапії виділена ціла категорія втручань, «альтернативних мастектоміям», які належать до нового етапу радикального лікування РМЗ з одночасною хірургічною реабілітацією хворих.
За нашими даними, застосування НПХТ дало можливість розширити показання до проведення ОЗО, кількість яких збільшилась за останні роки. Характеристика хірургічних видів лікування, які проводилися хворим, та їх еволюція за 20 останніх років представлені в таблиці 3 (див. табл. 3). Звертає на себе увагу той факт, що відсоток радикальних мастектомій поступово знижувався від 96,24% у 1990–1994 рр. до 57,73% — у 2009 р. Хворим на РГЗ І–ІІА ст. за відсутності протипоказань виконувалися переважно органозберігаючі операції, обсяг мастектомій з розширених (з видаленням обох грудних м’язів) скорочувався до функціонально-заощадливих — із збереженням останніх. З 2008 р. в Національному інституті раку почали широко впроваджуватися реконструктивні та відновні операції. Методом вибору для молодих жінок, хворих на РГЗ IIБ та IIIА стадії, зараз вважається шкірозберігаюча мастектомія з одночасним ендопротезуванням або реконструкцією. В цих випадках необхідним компонентом комплексного лікування повинна бути НПХТ, яка дозволяє зменшити розміри пухлини, підвищити абластику під час оперативного втручання та виконати радикальну операцію із збереженням або відновленням органа з урахуванням онкологічних принципів без зниження ефективності протипухлинної терапії в цілому.
| Види операцій | 1990–1994 | 1995–1999 | 2000–2004 | 2005–2008 | 2009 | Всього |
|---|---|---|---|---|---|---|
| абс. (%) | абс. (%) | абс. (%) | абс. (%) | абс. (%) | ||
| Мастектомія | 1255 (96,24) | 1249 (92,18) | 1173 (80,12) | 1035 (68,27) | 209 (57,73) | 4921 |
| Квадрантектомія | 46 (3,53) | 106 (7,82) | 264 (18,03) | 419 (27,64) | 129 (35,64) | 964 |
| Реконструктивні операції |
3 (0,23) | – | 27 (1,85) | 62 (4,09) | 24 (6,63) | 116 |
| Всього | 1304 | 1355 | 1464 | 1516 | 362 | 6001 |
Застосування органозберігаючих та реконструктивних операцій стало можливим за умови виконання наступних принципів сучасного підходу до лікування РГЗ: рання діагностика новоутворення в грудній залозі, бажано на стадії раку in situ; урахування молекулярно-біологічних особливостей пухлини та прогностичних факторів для планування раціональної неоад’ювантної та адекватної ад’ювантної протипухлинної терапії, а саме: індивідуалізований підхід до комплексного лікування хворих на РГЗ; cвоєчасне радикальне хірургічне втручання із диференційованим вибором доступу та обсягу видалених тканин з урахуванням онкологічних принципів та обов’язковим визначенням чистоти меж резекції; оцінка необхідності застосування неоад’ювантної та можливості проведення адекватної ад’ювантної протипухлинної терапії. Комплексна протипухлинна терапія з урахуванням прогностичних молекулярно-біологічних чинників та виконанням онкологічних принципів дає можливість успішно застосовувати органозберігаючі або реконструктивні операції без зниження результатів лікування, що підтверджує аналіз показників виживаності хворих на РГЗ за останні роки (див. табл. 4).
| Стадія РГЗ | 5-річна виживаність (%) | |
|---|---|---|
| 1988–1998* | 1999–2009* | |
| II A | 87,3±0,014 | 93,3±0,008 |
| II B | 78,0±0,017 | 84,34±0,014 |
| III A | 65,3±0,019 | 77,5±0,016 |
| III B | 52,9±0,035 | 64,7±0,027 |
Висновки
При МП РГЗ (ІІБ—ІІІБ стадії) комплексне лікування доцільно розпочинати з НПХТ. При ІІБ стадії РГЗ у хворих категорії низького та проміжного ризику достатньо застосовувати в неоад’ювантному режимі схему CMF, при визначенні поганого прогнозу захворювання бажано застосування схем з препаратами антрациклінового ряду. У пацієнток ІІІА—ІІІБ стадії комплексне лікування доцільно розпочинати з НПХТ із застосуванням схем з препаратами антрациклінового ряду, при визначенні поганого прогнозу захворювання бажано застосування схем з препаратами таксанового ряду та за необхідності — таргетної терапії.
Неоад’ювантне лікування хворих на РГЗ з урахуванням молекулярно-біологічних провісних та прогностичних принципів дозволяє розширити показання до проведення органозберігаючих та реконструктивних операцій без зниження ефективності протипухлинної терапії у первинно операбельних хворих та підвищити кількість радикально оперованих, зменшити частоту виникнення метастазування серед первинно неоперабельних хворих. Проведення НПХТ дозволяє розпочати комплексне лікування із системного протипухлинного впливу на пухлинне вогнище та субклінічні метастази, запобігати їх генералізації, отримувати інформацію про чутливість пухлини до цитостатиків і, таким чином, уникнути неефективної ад’ювантної терапії. Такий підхід створює умови для підвищення якості життя оперованих хворих та покращання результатів їх лікування.
Література
- 1. Возный Э.К., Добровольская Н.Ю. (2006) 15-летний опыт комплексного лечения больных местно-распространенным раком грудной железы с использованием неоадъювантной химиотерапии.Материалы Х Российского онкологического конгресса. Москва, 21–23 ноября 2006 г., с. 64.
- 6. Гарбуков Е.Ю., Слонимская Е.М., Красулина И.А. (2005) Неоадъювантная химиотерапия при раке грудной железы. Сибирский онкол. журн., 2: 14.
- 14. Донских Р.В., Семиглазов В.Ф., Семиглазов В.В. и др. ( 2007) Неоадъювантное лечение рака грудной железы. Маммология, 1: 34–38.
- 22. Думанский Ю.В., Борота А.В., Семикоз Н.Г. и др. (2008 ) Опухоли грудной железы. Учебное пособие. Донецк, 87 с.
- 29. Семиглазов В.Ф. (2008) Неоадъювантное и адъювантное лечение рака грудной железы. Москва, 288 с.
- 34. Татарченко А.С., Великая В.В.(2009) Использование различных схем неоадъювантной полихимиотерапии в комплексном лечении больных местно-распространенным раком грудной железы. Сибирский онкол. журн. Прил. 1, с. 193–194.
- 45. Федоренко З.П., Гайсенко А.В., Гулак Л.О. та ін. (2009) Рак в Україні. Бюл. Нац. канцер-реєстру, Київ, № 10, 70 с.
Место неоадъювантной полихимиотерапии в комплексном лечении больных раком грудной железы
Национальный институт рака, Киев
Резюме. Проанализирована заболеваемость и смертность от рака грудной железы в Украине и отдаленные результаты лечения 6001 больного, получавшего комплексное лечение в отделении опухолей грудной железы и ее реконструктивной хирургии Национального института рака с 1990 по 2009 г. Показана роль и место неоадъювантной противоопухолевой терапии и приведена эволюция хирургических методов лечения больных раком грудной железы по данным Национального института рака. Приведены принципы современного подхода к планированию комплексного лечения больных раком грудной железы, направленные на повышение его эффективности и улучшения качества жизни пациенток.
рак грудной железы, неоадъювантное лечение, сохранение органа, эффективность лечения, качество жизни, результаты лечения.














Leave a comment