Внутриартериальная транстемпоральная химиотерапия в комплексном лечении рака дна полости рта и языка. Новый методический подход
Процык В.С., Югринов О.Г., Коробко Е.В., Руденко Д.Н. , Петренко Л.И.
Резюме. В данной статье представлен новый методический подход к суперселективной катетеризации язычной артерии. Детально описана методика проведения суперселективной внутриартериальной химиотерапии у больных местно-распространенным раком языка и дна полости рта. Показаны основные этапы выполнения катетеризации, особенности проведения химиотерапии. Продемонстрированы преимущества данного метода.

Введение
Сегодня считается доказанным, что комбинация селективной внутриартериальной регионарной химиотерапии и лучевой терапии у больных раком дна полости и языка обеспечивает высокий уровень локорегионарного контроля опухолевого роста на фоне приемлемой системной токсичности. По данным I. Kichinobu, H. Yuichizo, частота ответа опухоли на внутриартериальную химиотерапию цисплатином с последующей лучевой терапией составила 92%, тогда как при системной химиотерапии лишь 56% [1].
Современная технология суперселективной химиотерапии предусматривает многокурсовую инфузию цитостатика через катетер, непосредственно установленный в язычную артерию. Это позволяет увеличить экстракцию цисплатина к опухоли больше, чем в два раза по сравнению с традиционным способом ретроградной внутриартериальной химиотерапии [2–5].
Целью настоящего исследования явилась разработка ангиографического метода суперселективной катетеризации язычной артерии хирургическим транстемпоральным доступом, призванного обеспечить прицельную инфузию химиопрепарата синхронно с проведением сеанса лучевой терапии.
Материалы и методы
Ангиографическая анатомия наружной сонной и язычной артерий.
Наружная сонная артерия кровоснабжает значительную часть лица и шеи и является передне-медиальной ветвью общей сонной артерии. Она начинается в каротидном треугольнике у переднего края грудино-ключично-сосцевидной мышцы и идет к ретромандибулярной ямке, входит в ткань околоушной железы и у ее верхнего края делится на конечные ветви.
На серийных ангиограммах наружной сонной артерии различают ствол, передние, средние, задние и конечные ветви. Длина ствола составляет 7–8 см, диаметр устья — 8–9 мм. На протяжении до угла нижней челюсти она отдает свои передние и медиальные ветви, остальные артерии отходят от ее верхних отрезков. От места возникновения ствол наружной сонной артерии направляется кверху и вперед от внутренней сонной артерии. Можно условно считать, что основные ветви наружной сонной артерии лежат ближе к сагиттальной плоскости, чем к фронтальной. Поэтому для адекватной интерпретации каротидных ангиограмм более пригодны снимки, выполненные в боковой проекции.
Расположение порядковых артерий по ходу наружной сонной артерии остается практически постоянным, в то время как их отжождение может варьировать. Наиболее типичным является самостоятельное начало дистальных разветвлений. Относительным непостоянством отличаются язычная и лицевая артерия. По сводной статистике общий ствол их встречается в 18–20% наблюдений. Длина такого ствола может достигать 1–2 см. При высоком начале общей сонной артерии (на уровне III шейного позвонка) передние артерии наружной сонной артерии могут в 5–7% начинаться близко друг к другу или пересекаться [4].
На ангиограммах, выполненных с закрытым и открытым ртом, в 17% наблюдений язычная и лицевая артерия меняют свое расположение. В случае низкого деления общей сонной артерии язычная артерия начинается на 1,5–2 см выше обычного.
Самостоятельно развитая язычная артерия является первой крупной медиальной ветвью наружной сонной артерии. Она начинается обычно на 2–3 см выше от бифуркации наружной и внутренней сонной артерий, идет по латеральному краю подъязычной мышцы и направляется к языку. Длина ствола язычной артерии составляет 7–8 см, диаметр ее устья равен 3–4 мм, а в случае опухолевого поражения языка диаметр язычной артерии может увеличиться. На уровне больших рожков подъязычной кости язычная артерия разделяется на свои конечные ветви. Она имеет тесное сообщение с одноименной артерией на контралатеральной стороне. Внутриорганные дорсальные ветви язычной артерии идут к задней части спинки языка. Иногда правая и левая дорсальные артерии в корне языка сливаются в одну, носящую название средней язычной артерии.
Дорсальные язычные артерии могут брать начало от восходящей небной артерии.
Глубокая артерия языка — самая крупная артерия, идущая по направлению к уздечке языка, пересекая тело нижней челюсти. Она тесно анастомозирует с одноименными артериями противоположной стороны.
Добавочные язычные артерии встречаются редко. При чрезбедренном доступе антеградная катетеризация язычной артерии считается довольно эффективным исследованием. Катетер «Кобра» в боковой проекции свободно располагается в начальном отделе ее ствола.
При транстемпоральном доступе для идентификации язычной артерии требуется выполнить более трудоемкие внутрисосудистые манипуляции.
Результаты
Ангиографическая методика катетеризации наружной сонной и язычной артерии хирургическим доступом. Селективная внутриартериальная химиотерапия.
В рентгенооперационной под местной анестезией производили разрез кожи по переднему краю ушной раковины на уровне козелка длинной около 3 см и выделяли поверхностную височную артерию. В просвет сосуда вводили проводник и по нему армированный рентгеноконтрасный катетер F-4 или F-5 типа «Кобра» 2 или 3 с двумя боковыми отверстиями в концевом отделе (рис. 1). В начальный период освоения методики использовали катетеры фирм «Кордис», «Кук». В настоящее время в нашем распоряжении имеются подобные катетеры фирмы «Terumo».
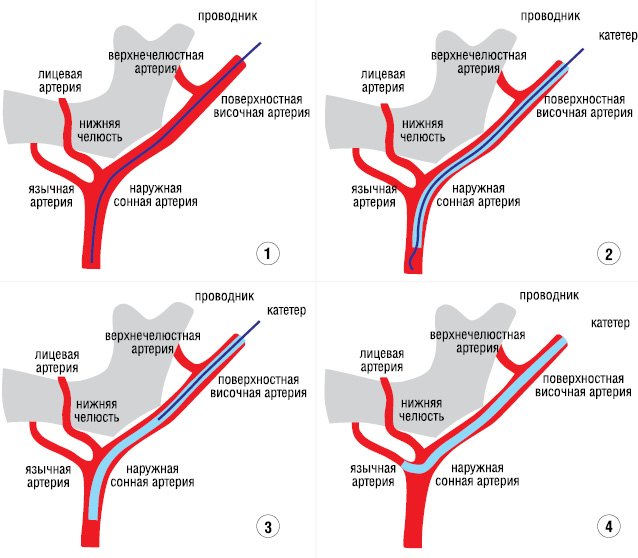
Под рентгенконтролем выбранный катетер низводили вглубь сосуда и устанавливали в стволе наружной сонной артерии на уровне расположения больших рожков подъязычной кости.
Производили ретроградную дигитальную субтракционную ангиографию и идентифицировали артерию, непосредственно кровоснабжающую опухоль (рис. 2). Суперселективную ангиографию язычной артерии проводили для уточнения ангиоархитектоники опухоли с использованием программы «сосудистая карта».
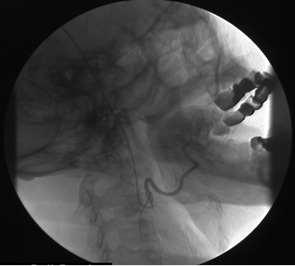
Фиксированные изгибы в верхушке катетеров были подробно описаны в специальных руководствах. Следует различать анатомическую и адаптационную кривизну катетера. Практика показывает, что успех катетеризации язычной артерии зависит от умения специалиста точно подобрать диагностический катетер соответственно диаметру устья и направление оси внеорганной порции язычной артерии. Для этого в распоряжении ангиолога должен быть набор катетеров с анатомической кривизной, образованной на расстоянии 1,5–2,5 см от кончика катетера под углом 45–90°. Адаптационный проксимальный изгиб должен быть смоделирован на расстоянии 6–8 см от анатомической вершины под углом 90–120°. В некоторых случаях бывают необходимы катетеры с верхушкой в форме полукольца. Такими универсальными катетерами лучше управлять, и они надежно фиксируются в устье язычной артерии.
Мы применили выбранные универсальные катетеры UK II Catheter 16 Unica Hyogo, Japan у 19 больных. Нами отмечен ряд преимуществ в применении последних при резкой извилистости хода, малом калибре язычной артерии, опухолевом тромбозе и облитерации просвета искомой артерии. Благодаря универсальной адаптационной кривизне управляемый катетер внедрялся в устья язычной артерии, отходящей от наружной сонной артерии под углом 90–120°.
Проникновение катетера в устье язычной артерии определяли по легкому кивку его кончика и усилению амортизирующего сопротивления катетера. Истинное положение катетера подтверждает пробное контрастирование с помощью 2 мл контрастного вещества.
При выявлении сосуда, кровоснабжающего опухоль, выполняли мероприятия, направленные на надежную фиксацию кончика катетера в устье язычной артерии, и проводили прокаиновую блокаду. Для этого в просвет сосуда через катетер вводили 5 мл 2% раствора прокаина. Следует отметить, что ни в одном случае при применении прокаиновой блокады не обнаружили признаков ангиоспазма. Кроме того, при предварительном введении прокаина в артериальное русло у больных значительно уменьшились неприятные ощущения, связанные с последующим введением контрастного вещества. После выполнения проб на устойчивость катетера (форсированный вдох, кашлевой толчок, гидравлический тест) вводили основную дозу контрастного вещества для проведения ангиографии. Количество и скорость введения иопромида зависело от калибра артерии, размеров опухолевого очага, наличия межартериальных анастомозов. Обычно вводили 10–12 мл иопромида со скоростью 2,5 мл/с. В редких случаях дозу увеличивали до 15 мл. Съемку начинали после введения 2 мл контрастного препарата и продолжали в течение 3–4 с. Как правило, ангиографию производили на высоте небольшого вдоха с частотой 1 кадр в секунду. В некоторых случаях съемку в стандартной боковой проекции дополняли ангиографией в косых проекциях.
Рентгеноморфологические признаки опухоли языка, отражающие структурные изменения язычной артерии, разделяли на прямые и косвенные. Прямые признаки деструкции сосудистой стенки, обусловленные опухолевой инвазией, проявлялись в виде локальной экстравазации рентгеноконтрастного вещества, возникновения культи сосуда.
Косвенные признаки опухолевого поражения заключались в увеличении диаметра, атипии хода афферентных сосудов, регистрации рентгенофункциональных нарушений. Они были обусловлены формированием патологического кровотока в виде контрастирования межартериальных анастомозов и соединений со смежными артериями, перетока крови на контралатеральную сторону языка.
По нашим данным, комплекс достоверных рентгеноморфологических и рентгенофункциональных признаков опухолевого поражения языка встретился у 96% больных.
Режим сочетания селективной внутриартериальной химиотерапии и лучевой терапии.
После подтверждения нахождения катетера в язычной артерии проводили инфузии цисплатина по 20 мг/м² в течение 5 дней синхронно с лучевой терапией. Затем лучевую терапию продолжали до суммарной дозы 60 Гр. Соблюдение постельного режима во время сеансов сочетанной химиолучевой терапии не требовалось.
Осложнения, возникшие при катетеризации и проведении селективной внутриартериальной химиотерапии.
Ангиоспазм при катетеризации поверхностной височной артерии наблюдался у 3 больных и пришелся на период освоения методики. Применение прокаина, введенного внутриартериально, постепенно купировало явления локального спазма.
Болевой синдром при введении рентгеноконтрастного вещества в наружную сонную артерию отмечен у 3 больных.
Дислокация катетера из язычной артерии во время инфузии цисплатина была в одном и окклюзия катетера также в одном наблюдении.
Местная реакция на внутриартериальную инфузию цисплатина в виде гиперемии, отека кожи и слизистых оболочек зоны опухолевого поражения не была выраженной и не препятствовала своевременному проведению лучевой терапии.
Дискуссия
Химиотерапевтические агенты, в частности цисплатин, карбоплатин, 5-фторурацил при системном применении показали высокие уровни опухолевого ответа в зависимости от дозы. Однако такие побочные эффекты препаратов, как нефротоксичность, ототоксичность и воспаление слизистой оболочки полости рта ограничивают использование высоких доз химиопрепаратов [6].
Нежелательные побочные эффекты системной химиотерапии можно компенсировать использованием техники внутриартериальной химиотерапии. Ранние попытки внутриопухолевой инъекции химиопрепарата были недостаточно эффективны из-за низкой диффузии лекарства в ткань опухоли, что требовало дополнительной инъекции вазоактивного средства для улучшения местной проницаемости [7–10].
В последствии ряд авторов сообщили об успешном использовании внутриартериальной химиотерапии, но уровни опухолевого ответа оставляли желать лучшего. Основная доля критики приходилась на методику ретроградной внутриартериальной регионарной химиотерапии, при которой имело место непредсказуемое распределение цитостатика в бассейне наружной сонной артерии и увеличение местной токсичности из-за нецелевого поступления химиопрепарата [11–14].
T. Robbins и соавторами [15] было предложено проводить адресную инфузию цисплатина путем суперселективной катетеризации артерии, ответственной исключительно за автономное кровоснабжение опухоли. Эта методика, названная «RADPLАТ», включает 4 цикла суперселективной внутриартериальной инфузии цисплатина с одновременным проведением лучевой терапии. Параллельно с каждой дозой цисплатина внутриартериально в системное русло вводили нейтрализирующий агент — тиосульфат натрия, который связывается ковалентно с цисплатином, формируя растворимое нетоксическое соединение. Такая нейтрализация цисплатина увеличивает плазменный клиренс лекарства, обеспечивая максимальную его конценртацию в опухолевой ткани, одновременно снижая системную токсичность. При использовании методики «RADPLАТ» возможно увеличить стандартную дозу цисплатина в 10 раз.
Сегодня доказан эффект радиосенсибилизации при комбинации инфузии 5-фторурацила, цисплатина и лучевой терапии. Вместе с тем известно, что цитотоксические эффекты наиболее полно потенцируются тогда, когда химиопрепарат вводится одновременно с лучевой терапией. Отсюда понятно стремление специалистов к синхронизации методик интервенционной лучевой терапии. При этом на передний план выступает методика внутриартериальной химиотерапии, предусматривающая транстемпоральный доступ катетеризации сосудов опухоли, не ограничивающий больного в передвижении и не препятствующий синхронному приему сеанса лучевой и химиотерапии [16].
Недавние достижения ученых в области разработки и совершенствования коаксиальных микрокатетерных систем позволили достичь очевидных успехов в технологии суперселективной внутриартериальной химиотерапии опухолей головы и шеи. Технический успех при применении суперселективной катетеризации и химиотерапии у больных раком дна полости рта, языка составляет 75–85%.
Несмотря на сложность транстемпоральной катетеризации язычной артерии, преимущество данной методики в том, что она позволяет проводить повторные курсы суперселективной внутриартериальной химиотерапии на протяжении длительного времени у больных местно-распространенным раком языка и дна полости рта.
Литература
1. Kichinobu I., Yuichiro H. (2000) Simultaneous intra-arterial chemotherapy and radiotherapy for carcinoma of oropharynx without neck metastasis. Otologia Fu-kuoka, 2 (46): 943–948.
2. Fuwa N., Kodaira T., Furutani K. et al. (2008) Arterial сhemoradiotherapy for locally advanced tongue cancer. Analysis of retrospective study of therapeutic results 88 Patients. International Journal of Radiation Oncology, 4 (72): 1090–1100.
3. Fuwa N., Kodira T., Furutani K. et al. (2008) A new method of selective inra-arterial infusion therapy via superficial temporal artery for head and neck cancer. Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology and Endodontplogy, 6 (105): 783–789.
4. Nakasato T., Katoh K., Sone M. et al. (2000) Superselective Continuous Arterial Infusion Chemotherapy through the Superficial Temporal Artery for Oral Cavity Tumors. American Journal of Neuroradiology, Vol. 21: 1917–1922.
5. Rohde S., Turowski B., Berkefeld I. et al. (2007) CT-Based evaluation of tumor volume after Intra-Arterial Chemotherapy of Locally Advanced Carcinoma of the Oral Cavity: Comparison with Clinical Remission Rates. Cardio Vascular and Interventional Radiology, 30: 86–91.
6. Luur C.L., Simis Y.I., Lansdaal P.E. et al. (2007) Ototoxicity in a randomized phase III Trial of Intra-Arterial Compared Witch Intravenous Cisplatin chemoradiation in Patients Witch Locally Advanced Head and Neck Cance. J. Clinical. Oncol., 24 (25): 3759–3765.
7. Korogi, Hikai I., Nishimura R. et al. (1995) Superselective intra-arterial Infusion cisplatin for squmous Cell Carcinoma of the mouth: preliminary Clinical Experience. Am. J. Rentgenol., 165: 1269–1272.
8. Tohnai I., Fuma N., Hayaschi Y. et al. (1998) New superselective intra-arterial infusion via superficial temporalis for cancer of the tongue and tumor tissere platinum concentration alter carboplatin (CBDCA) infusion. Oral Oncology, 5 (34): 387–390.
9. Hirai T., Korogi Y., Hamatare S. et al. (1999) Stages III and IV Squamous Cell. Carcinoma of the Mouth: Three-Year Experience with Superselective Chemotherapy Using Cisplatin. Prior to Definitive Treatment. Cardiovase Intervent Radiol., 22: 201–205.
10. Furutani K., Fuwa N., Kodaira T. et al. (2002) Continuous select intra-arterial chemotherapy in combination with irradiation for locally advanced cancer of the tongue and oral. Oncol., 38: 145–152.
11. Tsurumary D., Kuroiwa I., Yabuuchi H. et al. (2007) Efficacy of intra-arterial infusion chemotherapy for head and neck cancers using coaxial catheter technique: Initial Experience. Cardie Vascular and Interventional Radiology, 30: 207–211.
12. Ikushima I., Korogi Y., Isehi A. et al. (2007) Superselective intra-arterial infusion chemotherapy for stage III/IV Squamous cell carcinomas of the oral cavity: Midterm results. Eur J. Radiol., 29: 43–49.
13. Salins P.C., Venkatraman B. (2008) Retrograde externale carotid angiography: Technique for operative and emergency assessment of craniomaxillofacial haemorrhage. Brit. J. of Oral and Maxillofacial Surgery, 3 (46): 253–254.
14. Mitsudo R., Shigetomi T., Fujimoto Y. et al. (2011)Organ Preservation With Daily Concurrent Chemoradiotherapy V-sign superselective Intra-Arterial Infusion via a Superficial Temporal artery for T3 and T4 Head and Neck Cancer. Int. J. of Radiation Oncology, 5 (79): 1428–1435.
15. Robbins T., Kumar P., Harris I. et al. (2005) Supradose intra-arterial cisplatin and concurrent radiation therapy for the treatment of stage IV head and neck squamous cell carcinoma is feasible and efficacious in a multiinstitutional setting: Results of Radiation Therapy Oncology Group Trial 9615. J. Clin. Oncol., 7 (23): 1447–1454.
16. Bertino I., Occhini A., Falco C.E. et al. (2009) Concurrent Intra-Arterial carboplatin and ministration and radiation therapy for the treatment of advanced head and neck squamous cell carcinoma: short term results. Cancer, 9: 313–328.
Внутрішньоартеріальна транстемпоральна хіміотерапія в комплексному лікуванні раку дна ротової порожнини та язика. Новий методичний підхід
Резюме. У даній статті представлений новий методичний підхід до суперселективної катетеризації язичної артерії. Детально описана методика проведення суперселективної внутрішньоартеріальної хіміотерапії у хворих на місцево-поширений рак язика і дна ротової порожнини. Показані основні етапи виконання катетеризації, особливості проведення хіміотерапії. Продемонстровані переваги даного методу.
Ключові слова: рак дна порожнини рота, язика, селективна внутрішньоартеріальна хіміотерапія, транстемпоральний доступ.
Intra-arterial transtemporal chemotherapy in complex treatment of the mouth floor and tongue cancer. A new methodology approach
Summary. This article presents a new methodological approach to superselective catheterization of the lingual artery, the technique of superselective intra-arterial chemotherapy in patients with locally advanced cancer of the tongue and floor of the mouth was described in details. Main stages of the catheterization execution, features of chemotherapy were showed. The advantages of this method are demonstrated.
Key words: cancer of floor of the mouth, tongue, selective intra-arterial chemotherapy, transtemporal access.














Leave a comment