АЛГОРИТМ КОМПЛЕКСНОЇ ПРОМЕНЕВОЇ ДІАГНОСТИКИ ДИФУЗНИХ МАСТОПАТІЙ
Головко Т.С.1, Францевич К.А.2, Скляр С.Ю.1, Озеран Н.В.3
- 1Національний інститут раку, Київ
- 2Главный военно-медицинский клинический ордена Красной Звезды центр «Главный военный клинический госпиталь», Киев
- 3Киевская городская клиническая больница №18, Киев
Резюме. У статті розглянуто актуальність променевої діагностики дифузних мастопатій у жінок різного віку. Проаналізовано результати мамографічного обстеження 242 амбулаторних пацієнтів. Розроблений алгоритм комплексної променевої діагностики захворювань грудної залози надасть можливість підвищити ефективність діагностики та своєчасного лікування дифузних мастопатій.

ВСТУП
Протягом останнього десятиріччя відзначають збільшення кількості доброякісних захворювань грудних залоз (ГЗ), в тому числі дифузної фіброзно-кістозної мастопатії (ДФКМ), яку діагностують у 60–80% жінок репродуктивного віку [1, 2]. Подібність клінічної симптоматики, засад та механізмів розвитку мастопатій та ранніх стадій раку грудної залози (РГЗ), а також вірогідність розвитку РГЗ на фоні мастопатій — суттєвий привід для посилення уваги до даної патології [3]. У зв’язку з тим, що дифузна мастопатія може бути початковою фазою в ланцюгу розвитку новоутворень ГЗ [2], першочерговим завданням лікарів є профілактика, своєчасна діагностика та лікування ДФКМ. Спираючись на багаторічний досвід рентгенологічних досліджень ГЗ, сучасні радіологи концентрують свої зусилля на впровадженні у клінічну практику нових технологій та методик променевої діагностики. Але, незважаючи на високу інформативність сучасних променевих методів візуалізації, відсутність єдиного комплексного алгоритму променевої діагностики захворювань ГЗ віддаляє початок комплексного лікування, а також сприяє збільшенню показників занедбаності захворювань та смертності жінок від патології ГЗ.
Метою даної роботи є розробка алгоритму комплексної променевої діагностики захворювань ГЗ з метою своєчасного виявлення та лікування дифузних мастопатій як засобу раннього виявлення новоутворень ГЗ.
ОБ’ЄКТ І МЕТОДИ ДОСЛІДЖЕННЯ
Ретроспективно проаналізовано результати променевого дослідження пацієнток кабінету мамографії клініки променевої діагностики та терапії Головного військово-медичного клінічного ордена Червоної Зірки центру «Головного військового клінічного госпіталю» та відділення променевої діагностики Національного інституту раку. У дослідженні беруть участь 242 жінки віком від 26 до 66 (45±21) років, яких направили спеціалісти районних поліклінік та лікарень, з патологічними змінами в ГЗ. Усі знахідки, виявлені при обстеженні, згідно з системою опису зображень ГЗ Breast Imaging Reporting and Data System (BIRADS) Американської радіологічної колегії (American College of Radiology — ACR) були класифіковані за 6 категоріями:
- BIRADS 1 — немає змін (ризик раку — 0%);
- BIRADS 2 — доброякісні зміни (ризик раку — 0%);
- BIRADS 3 — вірогідні доброякісні зміни (ризик раку —
- BIRADS 4 — вірогідні злоякісні зміни (ризик раку — ~ 30%);
- BIRADS 5 — зміни високого рівня підозрілості (ризик раку — ~ 95%);
- BIRADS 6 — гістологічно верифікований рак.
Обстежених нами пацієнтів за класифікацією BIRADS розподілили наступним чином (табл. 1). Статистичну обробку даних проводили за допомогою програми MSExcel.
Таблиця 1 Розподіл пацієнтів за патологією ГЗ згідно з категорією BIRADS
| Категорія BIRADS | Характеристика патології ГЗ згідно з категорією BIRADS | Всього | Збережена репродуктивна функція | Менопауза |
|---|---|---|---|---|
| 1 | Без патології ГЗ | 53 (22%) | 45 (18,59%) | 8 (3,31%) |
| 2 | ДФКМ без вузлових утворень | 92 (38%) | 82 (33,88%) | 10 (4,13%) |
| 3 | З вузловими доброякіснимиутвореннями на фоні ДФКМ | 75 (31%) | 33 (13,64%) | 42 (17,35%) |
| 4 | З вірогідно злоякісними утвореннями на фоні ДФКМ | 15 (6%) | 5 (2,07%) | 10 (4,13%) |
| 5—6 | З гістологічно верифікованимизлоякісними новоутвореннями на фоні ДФКМ | 7 (3%) | 5 (2,07%) | 2 (0,83%) |
| Всього | 242 (100%) | 170 (70,25%) | 72 (29,75%) |
Отримані дані (див. табл. 1) свідчать, що з 242 обстежених пацієнток, направлених на прицільне дослідження, патологія ГЗ була виявлена у 189 (78%). У великої кількості пацієнток було відзначено ДФКМ без вузлових утворень при збереженій репродуктивній функції — 82 (33,88%). Вузлові доброякісні утворення на фоні ДФКМ переважали у пацієнток в менопаузі — 42 (17,35%), вірогідно злоякісні утворення на фоні ДФКМ також переважали у пацієнток в менопаузі — 10 (4,13%), гістологічно верифіковані злоякісні новоутворення на фоні ДФКМ у більшості випадків зустрічалися у пацієнток зі збереженою репродуктивною функцією.
При обстеженні пацієнток зареєстровано також супутні захворювання. Слід зазначити, що у 189 (78,09%) пацієнток в анамнезі була діагностована гінекологічна патологія (а саме — фіброміома матки, ендометріоз, міома матки, аденоміоз, полікістоз яєчників, цистоаденома яєчника, аднексит). У 133 (54,95%) пацієнток гінекологічна патологія в анамнезі поєднувалася з ендокринологічною патологією (гіпотиреоз, гіпертиреоз, гіперплазія щитоподібної залози, дифузний багатовузловий зоб, рак щитоподібної залози, тиреотоксикоз, аутоімунний тиреоїдит, цукровий діабет).
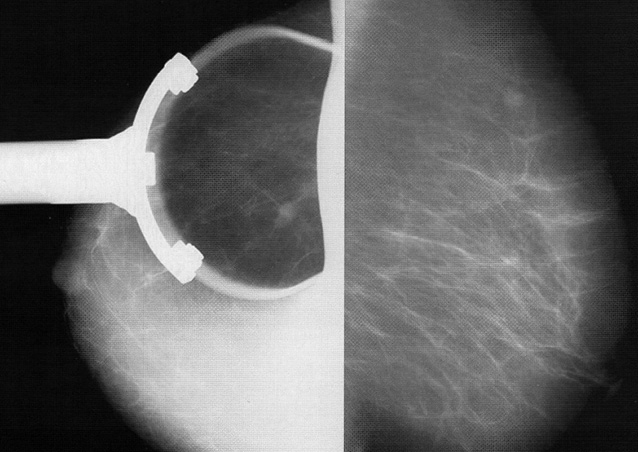
При обстеженні пацієнток із захворюваннями ГЗ комплексна променева діагностика включала: комплексну рентгенівську мамографію (КРМ) та комплексну ультразвукову мамографію (КУМ). КРМ виконували усім пацієнткам на сучасній рентгенівській мамографічній системі DIAMOND (General Electric, Фінляндія, 2007) (рис. 1) за стандартною методикою в прямих та косих проекціях, а також при необхідності доповнювали боковими проекціями та прицільними знімками патологічних утворень з локальною компресією (рис. 2), що дозволяло отримати достатньо повну інформацію про стан структури ГЗ: шкіри, підшкірної клітковини, залозистої, жирової та сполучної тканини, судин, звапнень, тканин в підзалозистому просторі та соску, про наявність новоутворень [2, 6, 7, 10, 11].
КУМ проводили для диференційної діагностики кіст та солідних утворень, які виявляли при пальпації та при КРМ, при оцінці ущільнень незрозумілої природи, та для виявлення змін в лімфатичних вузлах, а також у жінок із щільною паренхімою ГЗ та при вираженому больовому синдромі ГЗ [4, 5, 6]. Такі дослідження було виконано у 72 (29,75%) пацієнток.
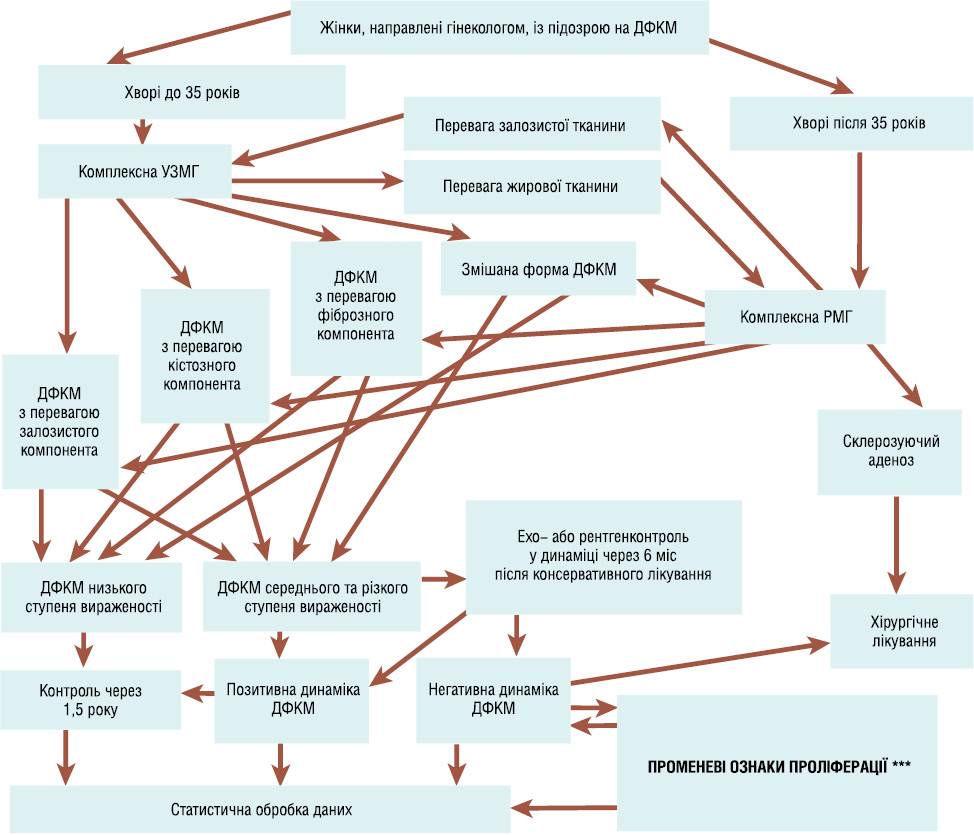
Виходячи з того, що КРМ є базою в діагностиці доклінічної (прихованої) форми РГЗ, детально досліджували рентгенологічну семіотику різних форм ДФКМ, що й було відображено в розробленому нами алгоритмі променевої діагностики ДФКМ (рис. 3). Усім пацієнткам, незалежно від віку, з перевагою в структурі ГЗ жирової тканини, а це видно на стандартній обзорній мамограмі в прямій та косій проєкціях, детально оцінювали рентгенологічні ознаки різних форм ДФКМ. В окремих випадках ділянки ущільнень документували прицільними знімками, навіть із збільшенням в 1,8 раза, під зручним кутом падіння рентгенівських променів (0°–180°) і в подальшому спостерігали через 3–6 міс (термін протизапальної терапії) позитивну або негативну динаміку зміни структури залозистого матриксу. При цьому оцінювали: вираженість патологічного процесу за об’ємом патологічної перебудови залозистого матриксу відносно нормального об’єму паренхіми (залозистих структур) ГЗ (до 25% — низький ступінь вираженості; 25% — середній ступінь вираженості; понад 25% — різкий ступінь вираженості); підвищення або зниження щільності залозистих структур; чіткість або розмитість контурів залозистих часточок та протоків; наявність мікрокальцинатів або збільшення їх кількості з оцінкою їхньої форми та розмірів, а також розповсюдженості (дифузної або локальної (регіонарної)); збільшення кількості вен, симетричність та несиметричність їх діаметрів; наявність або збільшення кількості ущільнених підпахвинних лімфатичних вузлів з оцінкою їх розмірів та структури; зміну діаметрів кістозного та солідного утворення — що дало змогу правильно сформулювати заключення для подальшої лікувальної тактики.
У випадках з вираженим больовим синдромом та різким ступенем вираженості патологічного процесу ДФКМ при природно щільній паренхімі ГЗ, що часто зустрічається у жінок до 30 років, виконували дообстеження на УЗД-апараті мультичастотним лінійним датчиком на частоті 7,5–13 МГц з метою оцінки розмірів і форми залозистих протоків та часточок, структури кістоподібних або солідних утворень, а також для виключення вузлових злоякісних новоутворень на фоні щільного залозистого матриксу.
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
У результаті проведеного дослідження хворих на різні форми дифузної мастопатіі без вузлових утворень розподілили за віковими групами згідно з морфорентгенологічною класифікацією (Н.І. Рожкова, 993) [1] наступним чином (табл. 2).
Таблиця 2 Розподіл дифузних мастопатій за віковими групами
| Кількість пацієнтів | ДФКМ з перевагою ЗК | ДФКМ з перевагою КК | ДФКМ з перевагою ФК | ДФКМ | |
|---|---|---|---|---|---|
| 26–35 | 10 (10,88%) | 4 (40%) | 3 (30%) | 2 (20%) | 1 (10%) |
| 36–45 | 43 (46,74%) | 3 (6,98%) | 10 (23,25%) | 25 (58,14%) | 5 (11,63%) |
| 46–55 | 32 (34,78%) | 1 (3,125%) | 7 (21,87%) | 18 (56,25%) | 6 (18,75%) |
| 56–66 | 7 (7,6%) | – | – | 4 (57,14%) | 3 (42,86%) |
| Всього | 92 (100%) | 8 (9%) | 20 (22%) | 49 (53%) | 15 (16%) |
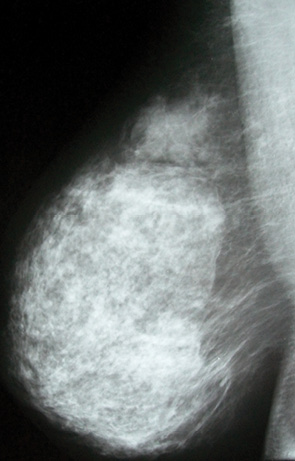
Рентгенологічно діагностували ДФКМ з перевагою залозистого компонента (ЗК) (рис. 4) як наявність симетричної тіні ГЗ — інтенсивної, неоднорідної, на фоні якої ділянки гіперплазії залозистої тканини візуалізувалися як велика кількість нашарувань округлих тіней розмірами від 0,3–0,4 до 1,0–1,5 см, неправильної форми, з нерівними контурами, що утворювали зони нерівномірної щільності. Ділянки аденозу виглядали як «пухнасті» або розмиті ущільнення, крізь які простежувався трабекулярний малюнок. Підшкірний жировий шар нерівномірно був звужений за рахунок випинання залозистих часточок. Картину інколи доповнювали фіброаденоми. При вираженому аденозі тіні часточок зливалися з зображенням навколочасточкової сполучної тканини, іноді тінь ГЗ ставала практично однорідною. При вираженому жировому компоненті ділянки гіперплазії утворювали дрібнокаліберний мереживоподібний малюнок з вогнищами, кожне з яких відповідає ділянці часточкової гіперплазії. У більшості випадків ДФКМ з перевагою ЗК діагностували у віковій групі 26–35 років, що практично збігалося з даними літератури (у віці 25–30 років) [8, 9].
ДФКМ з перевагою кістозного компонента (КК) (рис. 5) ренгенологічно діагностували за наявності порушення нормальної структури ГЗ, на фоні якої спостерігали велику кількість округлих та витягнутих розмитих тіней гіперплазованих часточок, що чергувалися з ділянками однорідного затемнення. Все перекреслювалося потовщеними тяжами з розмитими контурами в результаті набряку сполучної тканини (великопетлистої деформації строми). При збереженні острівців жирової тканини затемнення чергувалися з просвітленнями, що створювало картину в вигляді «місячного рельєфу». Дрібні кісти на мамограмах не розпізнавалися. Винятком були випадки з наявністю вапняного вмісту в кісті. Великі кісти давали округлі або овальні тіні різного розміру (від 0,5 до 4–5 см та більше). Тінь кісти була однорідною, контури її рівні та чітки. Навколо великої кісти інколи візуалізувалося вузьке та рівномірне кільце просвітлення. У випадках, коли в конгломераті щільної тканини не простежувалася кіста, допомагала КУМ. У більшості випадків ДФКМ з перевагою КК діагностували у віковій групі 36–45 років.
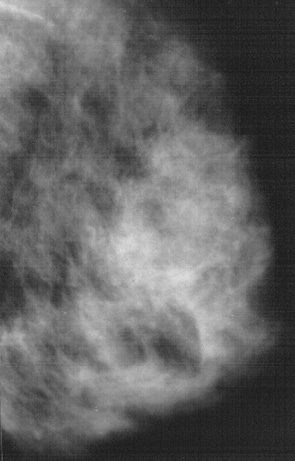
ДФКМ з перевагою фіброзного компонента (ФК) (рис. 6) ренгенологічно діагностували за наявності групи розширених деформованих протоків, що візуалізувалися як фіброзні нашарування, чітко контуровані щільні тяжі, які залежно від вираженості займали всю ГЗ або окремі ділянки (часто преареолярну зону, передній відділ, зовнішні квадранти). Зовнішній контур залозистого трикутника був нерівний, зубчастий, за рахунок фіброзування зв’язок Купера. У більшості випадків ДФКМ з перевагою ФК реєстрували в віковій групі 46–55 років.
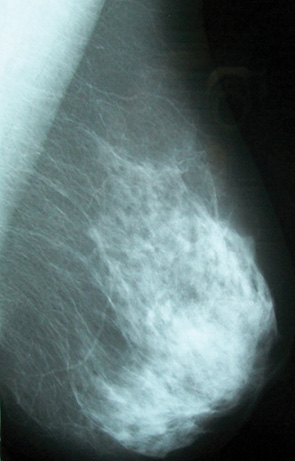
Змішана форма ДФКМ (рис. 7) рентгенологічно була представлена як хаотичний, мозаїчний малюнок з наявністю щільних тяжів, з розмитими ділянками ущільнень. У більшості випадків цю патологію діагностували в віковій групі 46–55 років.
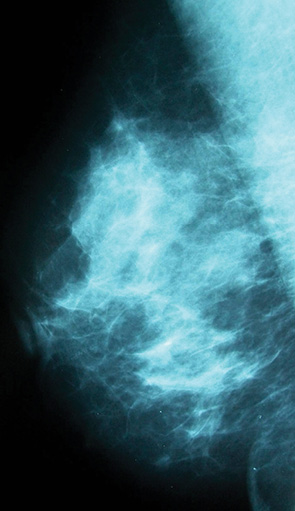
З табл. 2 видно, що дифузні мастопатії без вузлових утворень розподілилися таким чином: ДФКМ з перевагою ФК — 49 (53%) пацієнток, ДФКМ з перевагою КК — 20 (22%), ДФКМ з перевагою ЗК — 8 (9%), змішана форма ДФКМ — 15 (16%) пацієнток. У найбільшої кількості жінок в нашому досліджені, що страждали дифузними мастопатіями в віковій групі 36–45 років, діагностували ДФКМ з перевагою ФК. Наочну динаміку розподілу різних форм дифузних мастопатій за віковими групами жінок представлено на графічній діаграмі (рис. 8).
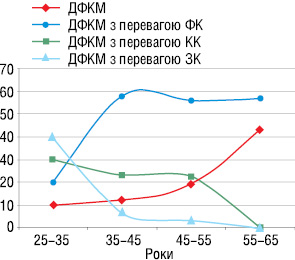
При зіставленні різних вікових груп пацієнток з діагностованими різними формами ДФКМ, як видно на рис. 8, виявилося, що кількість випадків змішаної форми ДФКМ із віком поступово збільшується, набирає обертів у віковій групі 55–65 років, а кількість випадків ДФКМ з перевагою КК — поступово зменшується; кількість випадків ДФКМ з перевагою ЗК у пацієнток зі збільшенням віку значно зменшується, пік спостерігається у віковій групі пацієнток 26–35 років, а кількість випадків ДФКМ з перевагою ФК зростає у віковій групі 30–45 років, а далі залишається практично на сталому рівні.
Слід зазначити, що в процесі рентгенологічного дослідження пацієнтка потрапляє під дію рентгенівського опромінення. Це потребує постійного контролю і можливого зниження дозових навантажень, оскільки порівняно малі дози випромінювання можуть призвести до негативних наслідків у майбутньому (погіршення стану здоров’я, прогресування існуючих захворювань, розвиток пухлин у віддаленні строки). Дозу контролюють за допомогою визначення ефективної дози (Е): Е=2,5 q (мкЗв) при 25 кВ, де q — експозиція (мАс) при виконанні мамограми; мкЗв — одиниця виміру ефективної дози. Ефективна доза на одну мамограму дорівнює 0,15 мЗв [10]. Ефективна доза при рентгенівській комп’ютерній томограмі ГЗ становить 0,4–0,5 мЗв [10].
При виконанні рентгеномамографічних досліджень бажано не перевищувати величини ефективних доз:
- профілактичне дослідження — 1000 мкЗв/рік;
- диференціальне діагностичне дослідження — 10 000 мкЗв/рік;
- дослідження та динамічний контроль у процесі лікування онкологічного захворювання — 1000 000 мкЗв/рік [10].
Використання розробленого нами алгоритму променевої мамографії ДФКМ (див. рис. 3) дало можливість не перевищувати величини ефективних доз, точно встановлювати діагноз, спостерігати за динамікою лікування.
ВИСНОВКИ
Враховуючи дані власного спостереження, ми дійшли висновку, що будь-які доброякісні або злоякісні утворення ГЗ завжди виникають на фоні ДФКМ. Раннє виявлення ДФКМ, динамічне спостереження за її розвитком, своєчасне її лікування є засобом раннього виявлення новоутворень ГЗ.
Спираючись на багаторічний досвід використання рентгенівської мамографії, велику розповсюдженість та постійне вдосконалення рентгенодіагностичного обладнання для діагностики ГЗ, розробки методик інтерпретації променевих сканів ГЗ, накопичення досвіду зіставлення клінічних, інструментально-лабораторних даних патології ГЗ у різних вікових групах, можна стверджувати, що на сьогоднішній день КРМ залишається основою променевої діагностики захворювань ГЗ.
Розроблений алгоритм променевої мамографії ДФКМ дає змогу не перевищувати величини ефективних доз, точно встановлювати діагноз, спостерігати за динамікою лікування, скоротити термін встановлення діагнозу ДФКМ, прискорити початок своєчасного лікування ДФКМ, отримати покращення стану пацієнтів у динаміці (через 6–12 міс) та запобігти виникненню РГЗ.
У близький перспективі розроблений алгоритм променевої мамографії ДФКМ стане основою організаційної моделі комплексної променевої діагностики ГЗ для своєчасного діагностування та лікування ДФКМ, а також надасть змогу програмувати процес діагностики захворювань ГЗ, що призведе до усунення операторозалежного тлумачення діагнозу.
ЛІТЕРАТУРА
- Рожкова Н.І. (1993) Рентгенодиагностика заболеваний молочной железы /Под ред. акад. А.С. Павлова/ М.: Медицина, 224 с.
- Татарчук Т.Ф., Ефименко О.А., Рось Н.В. (2003)Дисгормональные заболевания молочных желез в практике гинеколога-эндокринолога.Эндокринная гинекология, К.:147–181.
- Смоланка И.И., Досенко И.В. (2007) Дисгормональные гиперплазии молочных желез: этиология, клинические формы, принципы терапии. Медицинские аспекты здоровья женщины, №3 (6).
- Харченко В.П. и др. (2001) Лучевая диагностика заболеваний молочной железы, лечение и реабилитация (Лечение, профилактика и реабилитация заболеваний молочной железы): практ. руководство. Рос. науч. Центр рентгенорадиологии, Вып.4, М.: Фирма СТРОМ, 151 с.
- Харченко В.П., Рожкова Н.И. (2005) Клиническая маммология, М.: СТРОМ, 232 с.
- Клиническая маммология. Современное состояние проблемы/Под ред. Е.Б. Камповой-Полевой, С.С. Чистякова / М.: Гэотар-медиа, 2006: 511 c.
- Труфанов Г.Е., Рязанов В.В., Иванова Л.И. (2008) УЗИ в маммологии: руков. для врачей / Под ред. Г.Е. Труфанова / Воен.-мед. акад.СПб.: Элби-СПб, 186с.
- Головко Т.С. и др. (2009) Лучевая диагностика опухолевых заболеваний грудной железы: учеб.пособ., Харьков: Нове слово, 112с.
- Абдуллаев Р.Я. и др. (2009) Лучевая диагностика неопухолевых заболеваний грудной железы: учеб.пособ., Харьков: Нове слово, 96 с.
- Маммология: национальное руководство /под ред. В.П. Харченко, Н.И. Рожковой. / М.: ГЭОТАР-Медиа, 2009, 328 c.
- Bick U., Diekmann F. (2007) Digital mammography: what do we and what don’t we know? Eur. Radiology. Ibid., 8 (17): 1931–1942Алгоритм комплексной лучевой диагностики диффузных мастопатий
Алгоритм комплексной лучевой диагностики диффузных мастопатий
Главный военно-медицинский клинический ордена Красной Звезды центр «Главный военный клинический госпиталь», Киев
Киевская городская клиническая больница № 18, Киев
Резюме. В статье рассмотрена актуальность комплексной лучевой диагностики диффузных мастопатий у женщин разного возраста. Проанализировано маммографическое обследование 242 амбулаторных пациенток. Представлен алгоритм комплексной лучевой диагностики диффузных мастопатий. Разработанный алгоритм лучевой маммографии диффузной фиброзно-кистозной мастопатии создает возможность эффективной диагностики и своевременного лечения диффузных мастопатий.
алгоритм комплексной лучевой маммографии (АКЛМ), диффузная фиброзно-кистозная мастопатия (ДФКМ).














Leave a comment