KEYNOTE-006: результати 10-річного спостереження застосування пембролізумабу порівняно з іпілімумабом при поширеній меланомі
Резюме. Вступ. У дослідженні KEYNOTE-006 (NCT01866319) наводяться дані 10-річного спостереження порівняння пембролізумабу з іпілімумабом при неоперабельній поширеній меланомі. Матеріали та методи дослідження. Пацієнтів з неоперабельною меланомою III або IV стадії рандомізовано (1:1:1) у групу прийому пембролізумабу в дозі 10 мг/кг маси тіла внутрішньовенно (в/в) кожні 2–3 тиж протягом менше ніж 2 років або у групу отримання іпілімумабу в дозі 3 мг/кг маси тіла в/в кожні 3 тиж протягом 4 циклів. Після завершення KEYNOTE-006 хворі могли залучитися в дослідження KEYNOTE-587 (NCT03486873) для довгострокового спостереження. Пацієнти, що відповідали критеріям, могли отримати 2-й курс пембролізумабу. Первинною кінцевою точкою дослідження була загальна виживаність (ЗВ), при цьому модифікована виживаність без прогресування (ВБП), модифікована ВБП на 2-му курсі пембролізумабу та меланомоспецифічна виживаність були додатковими точками дослідження. Результати. З 834 пацієнтів, рандомізованих у дослідження KEYNOTE-006 (пембролізумаб отримували 556 учасників; іпілімумаб — 278 учасників), 333 хворі (39,9%) відповідали вимогам для залучення в дослідження KEYNOTE-587, проте в дослідження KEYNOTE-587 перейшли 211 з 333 (25,3%) пацієнтів (159 хворих отримували пембролізумаб, а 52 — іпілімумаб). Для пацієнтів, які перейшли в дослідження KEYNOTE-587 (n=211), медіана часу від рандомізації в дослідження KEYNOTE-006 до завершення збору даних для дослідження KEYNOTE-587 (1 травня 2024 р.) становила 123,7 міс (діапазон від 122,0 до 127,3 міс). Медіана ЗВ у групі отримання пембролізумабу становила 32,7 міс (95% довірчий інтервал (ДІ) 24,5–41,6 міс) та у групі іпілімумабу — 15,9 міс (95% ДІ 13,3–22,0 міс) (коефіцієнт ризику (КР) 0,71 (95% ДІ 0,60–0,85)). Рівень 10-річної ЗВ становив 34,0 і 23,6% в обох групах відповідно. Серед пацієнтів, які завершили лікування пембролізумабом протягом періоду більше ніж 94 тиж, медіани ЗВ з 94-го тиж не досягнуто (НД) (НД; 95% ДІ НД–НД), при цьому рівень 8-річної ЗВ становив 80,8%. Медіана модифікованої ВБП становила 9,4 міс (95% ДІ 6,7–11,6 міс) у групі пембролізумабу та 3,8 міс (2,9–4,3 міс) у групі іпілімумабу (КР 0,64 (95% ДІ 0,54–0,75)). Серед пацієнтів, які отримували 2-й курс пембролізумабу, медіана модифікованої ВБП з моменту початку 2-го курсу лікування становила 51,8 міс (95% ДІ 11,0 міс — НД), а рівень 6-річної модифікованої ВБП становив 49,2%. Медіана ВБП становила 51,9 міс (95% ДІ 30,0–114,7 міс) у групі пембролізумабу та 17,2 міс (95% ДІ 13,9–25,9 міс) у групі іпілімумабу (КР 0,66 (95% ДІ 0,55–0,81)). Висновки. Отримані результати свідчать про те, що пембролізумаб забезпечує довгострокові переваги виживаності при поширеній меланомі, що підтверджує його роль як стандарту лікування.
DOI: 10.32471/clinicaloncology.2663-466X.56-4.33755
Вступ
 Іпілімумаб, інгібітор цитотоксичного білка 4, асоційованого з Т-лімфоцитами (Cytotoxic T-lymphocyte associated protein 4 — CTLA-4), став першим інгібітором імунних контрольних точок, схваленим для лікування поширеної меланоми, який був стандартом терапії цього захворювання до появи інгібіторів білка програмованої клітинної смерті 1 (Programmed cell death 1 — PD-1) [1]. У 2014 р. Управлінням з контролю за харчовими продуктами і лікарськими засобами (Food and Drug Administration — FDA), США, уперше схвалено застосування пембролізумабу для лікування неоперабельної або метастатичної меланоми у пацієнтів, в яких спостерігали прогресування захворювання при використанні іпілімумабу [2]. З того часу пембролізумаб став стандартом лікування поширеної меланоми у 1-й та наступних лініях терапії, а також використовується в неоад’ювантному та ад’ювантному лікуванні резектабельної меланоми III стадії та ад’ювантному лікуванні резектабельної меланоми IIB або IIC стадії підвищеного ризику [3, 4]. Дослідження III фази KEYNOTE-006 розроблене для порівняння ефективності та безпеки пембролізумабу з іпілімумабом у осіб із поширеною меланомою, які раніше не отримували іпілімумаб [5]. У результатах первинного аналізу встановлено, що пембролізумаб суттєво підвищив ЗВ і ВБП порівняно з іпілімумабом у пацієнтів із поширеною меланомою, які раніше не приймали іпілімумаб, зокрема у тих, хто раніше проходив лікування інгібіторами BRAF (білка, залученого до передачі сигналів усередині клітин) або MEK (білка в сигнальному шляху RAS-RAF-MEK-ERK), а також у хворих із метастазами в головний мозок [5]. Цей висновок підтверджено в наступних аналізах дослідження KEYNOTE-006, в яких доведено, що пембролізумаб продовжує забезпечувати вищі показники виживаності протягом 5 років спостереження порівняно з іпілімумабом [6, 7].
Іпілімумаб, інгібітор цитотоксичного білка 4, асоційованого з Т-лімфоцитами (Cytotoxic T-lymphocyte associated protein 4 — CTLA-4), став першим інгібітором імунних контрольних точок, схваленим для лікування поширеної меланоми, який був стандартом терапії цього захворювання до появи інгібіторів білка програмованої клітинної смерті 1 (Programmed cell death 1 — PD-1) [1]. У 2014 р. Управлінням з контролю за харчовими продуктами і лікарськими засобами (Food and Drug Administration — FDA), США, уперше схвалено застосування пембролізумабу для лікування неоперабельної або метастатичної меланоми у пацієнтів, в яких спостерігали прогресування захворювання при використанні іпілімумабу [2]. З того часу пембролізумаб став стандартом лікування поширеної меланоми у 1-й та наступних лініях терапії, а також використовується в неоад’ювантному та ад’ювантному лікуванні резектабельної меланоми III стадії та ад’ювантному лікуванні резектабельної меланоми IIB або IIC стадії підвищеного ризику [3, 4]. Дослідження III фази KEYNOTE-006 розроблене для порівняння ефективності та безпеки пембролізумабу з іпілімумабом у осіб із поширеною меланомою, які раніше не отримували іпілімумаб [5]. У результатах первинного аналізу встановлено, що пембролізумаб суттєво підвищив ЗВ і ВБП порівняно з іпілімумабом у пацієнтів із поширеною меланомою, які раніше не приймали іпілімумаб, зокрема у тих, хто раніше проходив лікування інгібіторами BRAF (білка, залученого до передачі сигналів усередині клітин) або MEK (білка в сигнальному шляху RAS-RAF-MEK-ERK), а також у хворих із метастазами в головний мозок [5]. Цей висновок підтверджено в наступних аналізах дослідження KEYNOTE-006, в яких доведено, що пембролізумаб продовжує забезпечувати вищі показники виживаності протягом 5 років спостереження порівняно з іпілімумабом [6, 7].
У цьому дослідженні наведено аналіз ефективності пембролізумабу та іпілімумабу після 10 років спостереження пацієнтів з поширеною меланомою, які раніше не отримували іпілімумаб, зокрема додано дані досліджень KEYNOTE-006 і KEYNOTE-587, включно з пацієнтами, які пройшли 2-й курс терапії пембролізумабом.
Методи
Дизайн дослідження
Багатоцентрове відкрите рандомізоване дослідження III фази KEYNOTE-006 (NCT01866319) проведене у 87 центрах у 16 країнах і спрямоване на оцінку ефективності та безпеки пембролізумабу порівняно з іпілімумабом у пацієнтів із неоперабельною або поширеною меланомою. Детальні методи дослідження KEYNOTE-006 опубліковані раніше [5–7]. Після завершення дослідження KEYNOTE-006 (3 червня 2019 р.) хворі, які відповідали критеріям, могли перейти до відкритого розширеного дослідження фази III KEYNOTE-587 (NCT03486873), яке розроблено для продовження збору довготривалих даних про ефективність лікування у осіб із солідними пухлинами, які раніше отримували пембролізумаб у межах клінічного дослідження.
Протоколи дослідження та поправки до них схвалені відповідними інституційними наглядовими радами та комітетами з етики в кожній установі. Дослідження проводилося відповідно до протоколу, керівництв із належної клінічної практики (Good Clinical Practice — GCP) та Гельсінської декларації. Усі пацієнти надали письмову інформовану згоду.
Пацієнти
Особи, які відповідали критеріям залучення в дослідження KEYNOTE-006, були віком від 18 років, мали неоперабельну меланому III або IV стадії з функціональним статусом 0 чи 1 за шкалою Східної кооперативної онкологічної групи (Eastern Cooperative Oncology Group — ECOG), а також щонайменше 1 вимірюване ураження відповідно до критеріїв RECIST 1.1 (Критерії оцінки відповіді при солідних пухлинах, версія 1.1) і відомий статус мутації BRAF. Пацієнти могли пройти не більше 1 системної терапії за умови, що ця терапія не передбачала застосування анти-CTLA-4, анти-PD-1, анти-PD-L1 або анти-PD-L2 препарати. Пацієнтів з увеальною або очною меланомою, а також тих, у кого діагностовано активні метастази в центральну нервову систему, виключено з дослідження. Хворі з раніше лікованими метастазами в головний мозок мали право на залучення в дослідження, якщо їх стан залишався стабільним і не виявлено нових метастазів або прогресування вже наявних метастазів у головний мозок. Будь-які пацієнти, зареєстровані в KEYNOTE-006, які отримували лікування або знаходилися на етапі спостереження, мали право перейти в дослідження KEYNOTE-587.
Досліджуване лікування
У дослідженні KEYNOTE-006 хворих випадковим чином розподілено (1:1:1) на 3 групи для отримання різних схем лікування: пембролізумабу в дозі 10 мг/кг маси тіла в/в кожні 2 тиж протягом 2 років, пембролізумабу в дозі 10 мг/кг маси тіла в/в кожні 3 тиж протягом 2 років або іпілімумабу в дозі 3 мг/кг маси тіла в/в кожні 3 тиж протягом 4 циклів. Лікування тривало до завершення призначеного курсу, прогресування хвороби, розвитку ознак неприйнятної токсичності, рішення пацієнта або лікаря про припинення участі в дослідженні чи до появи інших критеріїв припинення лікування. Пацієнти, які досягли повної відповіді (ПВ), підтвердженої двома скануваннями з інтервалом щонайменше 4 тиж, могли припинити лікування за умови, що вони отримували пембролізумаб щонайменше 6 місяців і отримали принаймні 2 дози пембролізумабу після підтвердження ПВ. Пацієнти, які досягли стабілізації хвороби (СХ) або кращих результатів під час 1-го курсу лікування пембролізумабом, могли отримати 2-й курс пембролізумабу в дозі 200 мг кожні 3 тиж протягом періоду до 1 року (близько 17 циклів) у межах дослідження KEYNOTE-006 або KEYNOTE-587, якщо у них виявлено прогресування хвороби після припинення терапії.
Оцінки та кінцеві точки
У дослідженні KEYNOTE-006 оцінку відповіді пухлини проводили за допомогою комп’ютерної або магнітно-резонансної томографії на 12-му тиж, потім кожні 6 тиж до 48-го тиж і далі — кожні 12 тиж. Після припинення лікування пацієнтів спостерігали кожні 12 тиж для оцінки виживаності до закінчення дослідження (3 червня 2019 р.). Пацієнти, які перейшли в дослідження KEYNOTE-587, знаходилися під наглядом для оцінки тривалості виживаності, прогресування хвороби та початку нової протиракової терапії. Хворі, які отримували 2-й курс пембролізумабу в межах дослідження KEYNOTE-587, проходили радіографічне обстеження відповідно до протоколу KEYNOTE-006. Особи, яких спостерігали в дослідженні KEYNOTE-587, проходили обстеження відповідно до місцевих стандартів медичної допомоги.
Основною кінцевою точкою дослідження KEYNOTE-587 була ЗВ, а ВБП та ВБП під час 2-го курсу пембролізумабу були додатковими кінцевими точками. Post hoc аналізи включали меланомоспецифічну виживаність серед усіх учасників, ЗВ у підгрупах пацієнтів, ЗВ та модифіковану ВБП з 94-го тиж серед хворих, які отримували пембролізумаб протягом >94 тиж. Оцінювали також ЗВ, модифіковану ВБП та меланомоспецифічну виживаність з моменту оцінки дослідником найкращої загальної відповіді на основі ПВ, часткової відповіді (ЧВ) або СХ на пембролізумабі в дослідженні KEYNOTE-006. Оцінювали також ЗВ та модифіковану ВБП у пацієнтів, які отримували пембролізумаб або іпілімумаб як терапію першої лінії. Відповідь оцінювалася дослідником згідно з критеріями RECIST 1.1. Дані 2 схем дозування пембролізумабу були об’єднані. ЗВ, модифіковану ВБП та меланомоспецифічну виживаність оцінювали за методом Каплана — Меєра. Для аналізу ЗВ та модифікованої ВБП пацієнтів у KEYNOTE-006, які не перейшли до KEYNOTE-587, цензуровано на дату останнього відомого моменту, коли вони були живі в дослідженні KEYNOTE-006. У дослідженні KEYNOTE-587 хворих, яких спостерігали після завершення збору даних, цензуровано на момент завершення збору або на дату останнього відомого моменту, коли вони були живі.
Події ВБП зареєстровано на момент їх виникнення, при цьому пацієнти без подій були цензуровані на дату останнього спостереження в дослідженні KEYNOTE-587 (модифікований аналіз ВБП). Для оцінки меланомоспецифічної виживаності хворих, у яких не відмічалося прогресування меланоми або смерті від неї, цензуровано на момент завершення збору даних або на останню відому дату життя в KEYNOTE-587. Пацієнтів, які не перейшли в KEYNOTE-006, цензуровано на момент завершення цього дослідження (31 липня 2019 р.) або на останню відому дату їх життя [9]. КР та 95% ДІ розраховані на основі моделі регресії Кокса за методом Ефрона для обробки зв’язків із включенням лікування як коваріату.
Результати
Пацієнти
У період з 18 вересня 2013 р. до 3 березня 2014 р. 834 осіб зареєстровано в дослідженні KEYNOTE-006, яких випадковим чином розподілили в групу отримання пембролізумабу (n=556) або іпілімумабу (n=278). Середній вік хворих становив 62,0 року (діапазон 18–89 років); серед яких 497 пацієнтів (59,6%) — чоловічої статі, у 270 (32,4%) осіб відмічався підвищений рівень лактатдегідрогенази (ЛДГ), у 302 (36,2%) осіб виявлено мутацію BRAF при меланомі, у 186 (22,3%) хворих розмір пухлини на момент початкового обстеження зафіксовано на рівні >10 см, у 80 (9,6%) пацієнтів виявлено метастази в головний мозок, а 549 (65,8%) осіб отримали досліджуване лікування як терапію першої лінії. На момент завершення дослідження KEYNOTE-006 (31 липня 2019 р.) 333 з 834 хворих (39,9%) мали право на залучення в дослідження KEYNOTE-587 (комбінована група пембролізумабу, n=228; група іпілімумабу, n=105), з яких 211 (25,3%) зареєструвалися в дослідженні (комбінована група пембролізумабу, n=159; група іпілімумабу, n=52), а 122 (14,6%) не зареєструвалися. У 211 пацієнтів, які перейшли в дослідження KEYNOTE-587, медіана тривалості спостереження (час від рандомізації в KEYNOTE-006 до 1 травня 2024 р. — дати завершення дослідження KEYNOTE-587) становила 123,7 міс (діапазон 122,0–127,3 міс). Подальшу протипухлинну терапію отримували близько половини хворих, залучених до KEYNOTE-006. 16 пацієнтів розпочали 2-й курс пембролізумабу в дослідженні KEYNOTE-006 (n=15) або KEYNOTE-587 (n=1).
Ефективність
Станом на дату завершення збору даних 533 з 834 пацієнтів (63,9%) померли, з яких у 438 (52,5%) зафіксовано летальні випадки через прогресування меланоми або причини, пов’язані з нею, а у 95 (11,4%) — через інші або невідомі причини. У групі хворих, які отримували пембролізумаб, померли 348 з 556 (62,6%), тоді як у групі, що отримувала іпілімумаб, померли 185 з 278 (66,5%). Медіана ЗВ становила 32,7 міс (95% ДІ 24,5–41,6 міс) у групі пембролізумабу та 15,9 міс (95% ДІ 13,3–22,0 міс) — у групі іпілімумабу (КР 0,71 (95% ДІ 0,60–0,85)) (рис. 1а). 8-річний рівень ЗВ становив 36,9% у групі пембролізумабу та 24,8% у групі іпілімумабу, а 10-річний рівень ЗВ — 34,0 та 23,6% відповідно. Загалом зареєстровано 643 події, з них 423 (76,1%) у групі пембролізумабу та 220 (79,1%) у групі іпілімумабу. Медіана модифікованої ВБП становила 9,4 міс (95% ДІ 6,7–11,6 міс) у групі пембролізумабу та 3,8 міс (95% ДІ 2,9–4,3 міс) у групі іпілімумабу (КР 0,64 (95% ДІ 0,54 0,75)) (рис. 1в). 8-річний рівень ВБП становив 23,4% у групі пембролізумабу та 12,8% у групі іпілімумабу, а 10-річний рівень ВБП — 22,0 та 12,8% відповідно. Усього сталося 438 подій, пов’язаних з меланомоспецифічною виживаністю, а саме 278 (50,0%) у групі пембролізумабу та 160 (57,6%) у групі іпілімумабу. Медіана меланомоспецифічної виживаності становила 51,9 міс (95% ДІ 30,0–114,7 міс) у групі пембролізумабу та 17,2 міс (95% ДІ 13,9–25,9 міс) у групі іпілімумабу (КР 0,66 (95% ДІ 0,55–0,81)) (рис. 1c). 8-річний рівень меланомоспецифічної виживаності становив 46,5% у групі пембролізумабу та 32,1% у групі іпілімумабу, а 10-річний рівень меланомоспецифічної виживаності — 45,2 та 31,3% відповідно.
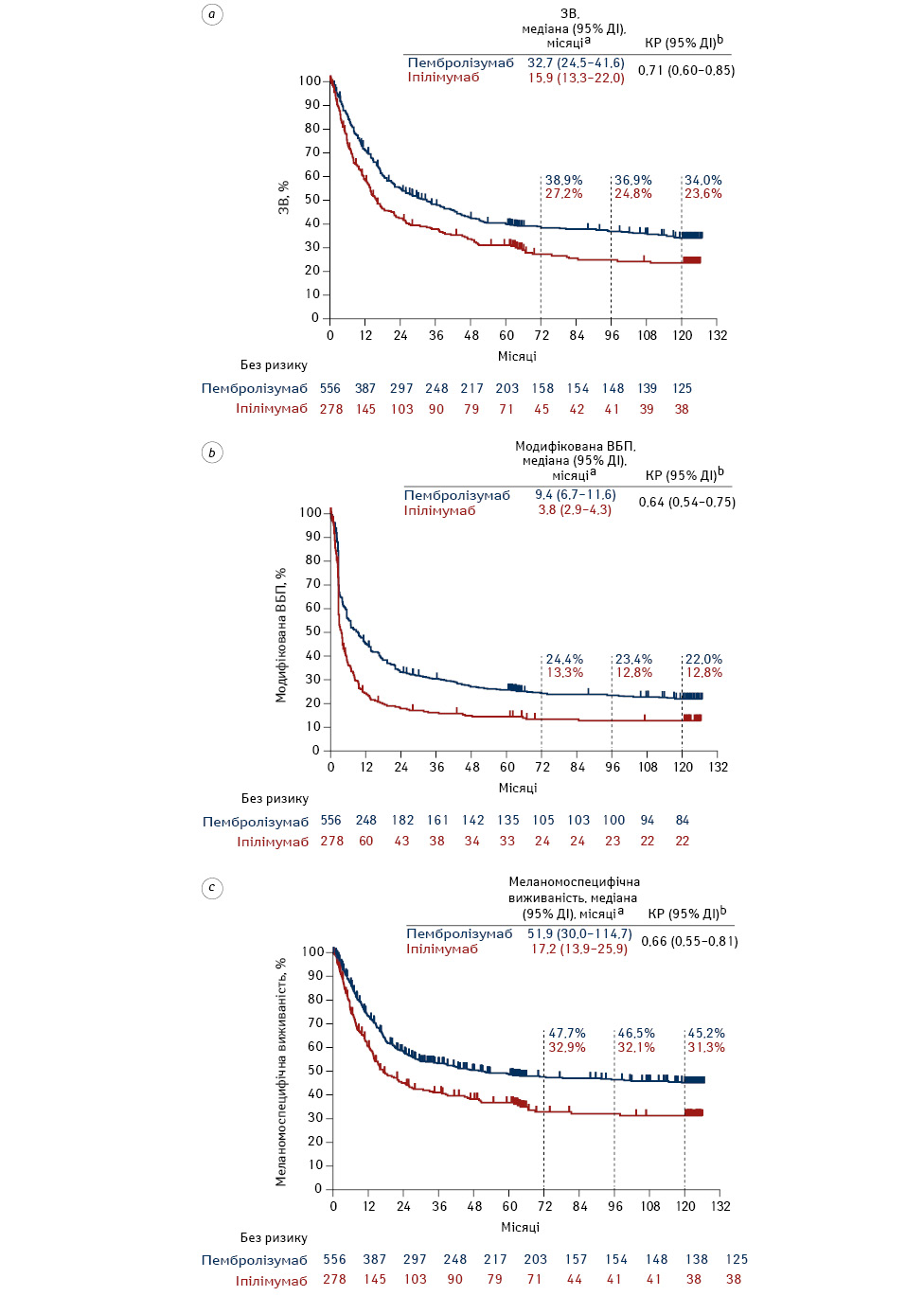
a) За методом Каплана — Меєра для цензурованих даних; b) на основі регресійної моделі Кокса за методом Ефрона
Серед пацієнтів, які завершили 94-тижневе лікування пембролізумабом (n=103), медіана тривалості спостереження становила 122,9 міс (діапазон 65,2–127,2 міс). Медіани ЗВ після 94-го тиж не досягнуто (НД; 95% ДІ НД–НД), 6-річний рівень ЗВ після 94-го тиж становив 91,8%, а 8-річний рівень — 80,8% (рис. 2a). Медіани модифікованої ВБП серед хворих, які завершили 94-тижневе лікування пембролізумабом, після 94-го тиж не досягнуто (НД; 95%ДІ НД–НД), 6-річний рівень модифікованої ВБП після 94-го тиж становив 73,2%, а 8-річний рівень модифікованої ВБП — 64,8% відповідно (рис. 2b).
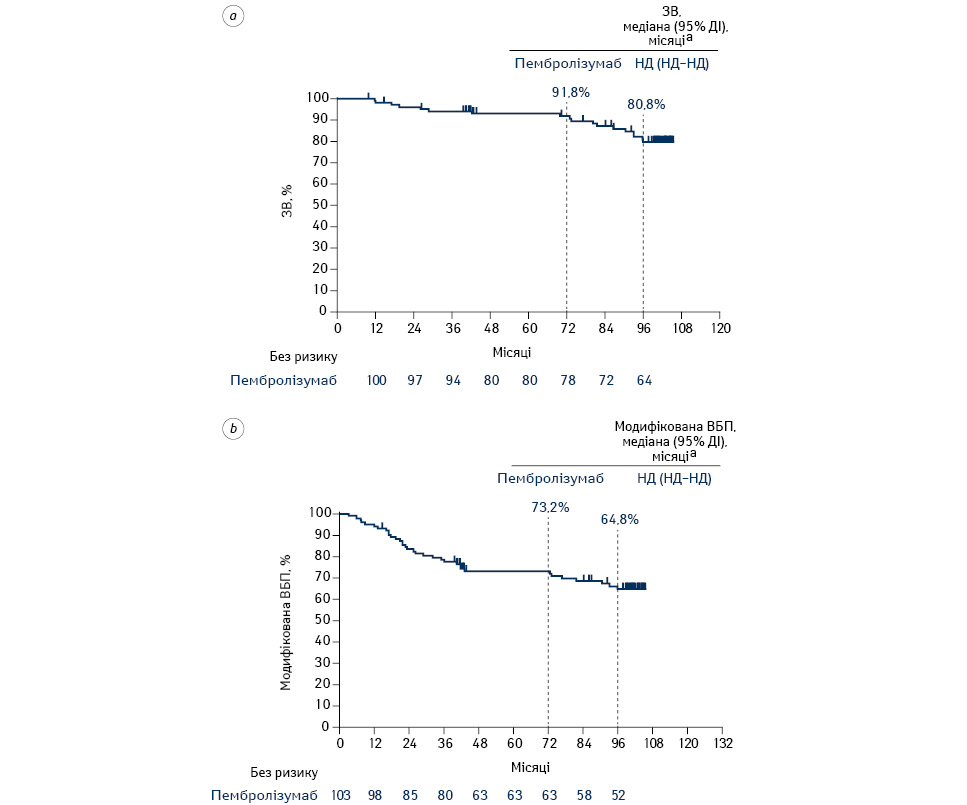
a) Метод Каплана — Меєра для цензурованих даних; b) на основі регресійної моделі Кокса за методом Ефрона
У загальній популяції пацієнтів, які отримували пембролізумаб, у 83 пацієнтів (14,9%) зафіксовано ПВ на лікування, 172 (30,9%) — ЧВ та 97 (17,4%) — СХ. Медіани ЗВ з моменту найкращої відповіді не досягнуто у осіб з ПВ (95% ДІ НД–НД), у пацієнтів з ЧВ (95% ДІ 99,2 міс — НД), тоді як для хворих із СХ вона становила 23,7 міс (95% ДІ 18,7–30,9 міс) (рис. 3a). 6-річний рівень ЗВ з моменту найкращої відповіді становив 81,9% у пацієнтів з ПВ, 59,5% у осіб з ЧВ і 25,2% у хворих із СХ; 8-річний рівень ЗВ становив 78,1, 58,7 та 21,8% відповідно. Медіани модифікованої ВБП з моменту найкращої відповіді не досягнуто у пацієнтів з ПВ (95% ДІ НД–НД) та становила 24,9 міс (95% ДІ 17,7–44,4 міс) у осіб з ЧВ і 4,2 міс (95% ДІ 2,8–7,2 міс) у хворих з СХ (рис. 3b). 6-річний рівень модифікованої ВБП з моменту найкращої відповіді становив 66,4% у пацієнтів з ПВ, 39,1% у осіб з ЧВ і 7,4% у хворих із СХ; 8-річний рівень модифікованої ВБП становив 62,7, 38,3 та 6,4% відповідно. Медіани меланомоспецифічної виживаності з моменту найкращої відповіді не досягнуто (95% ДІ НД–НД) у пацієнтів з ПВ та ЧВ, вона становила 27,0 міс (95% ДІ 19,1–56,6 міс) у осіб із СХ (рис. 3c). 6-річний рівень меланомоспецифічної виживаності з моменту найкращої відповіді становив 91,8% у хворих з ПВ, 68,3% у пацієнтів з ЧВ і 37,5% у осіб із СХ; 8-річний рівень меланомоспецифічної виживаності становив 87,5, 68,3 та 35,7% відповідно.
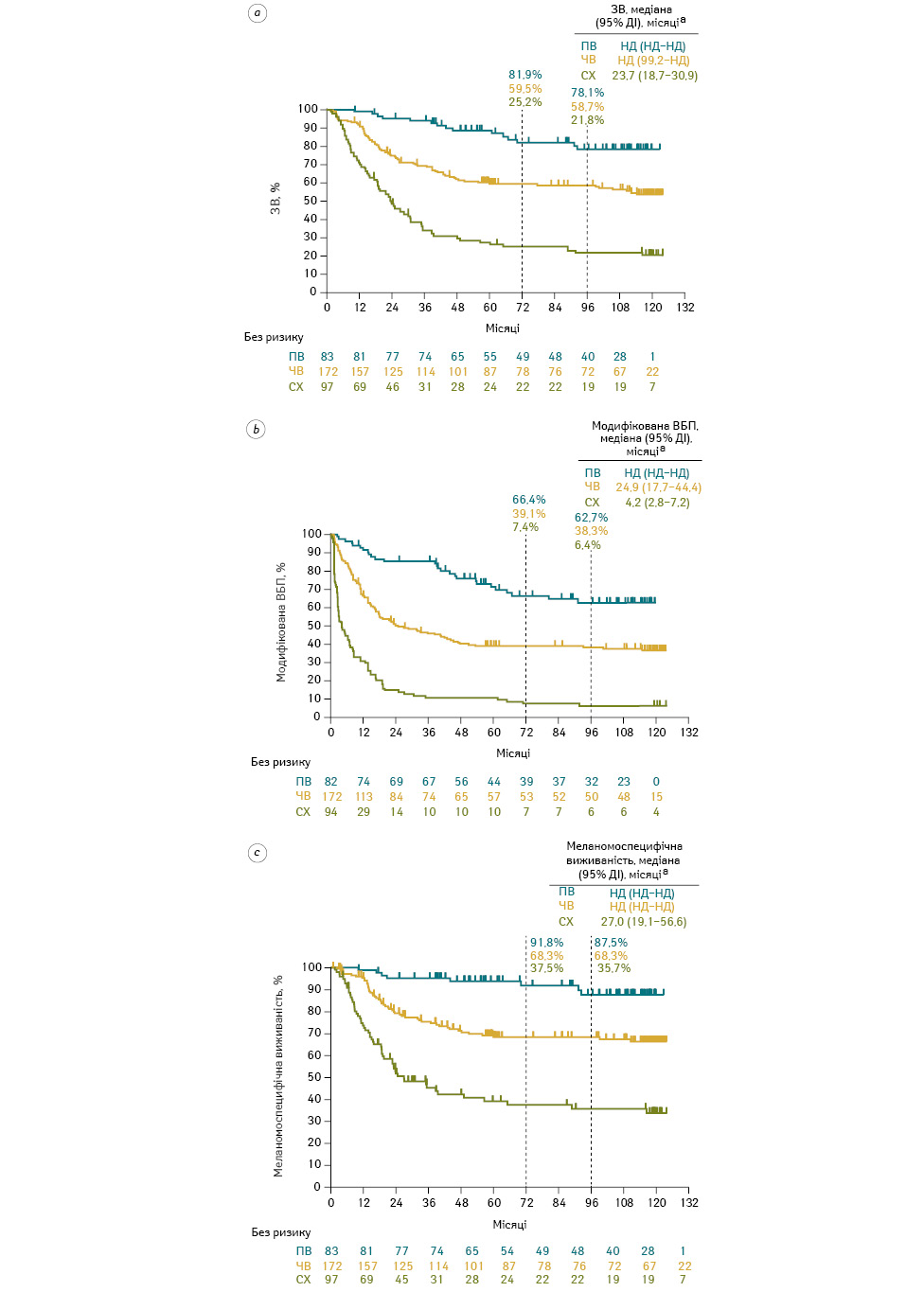
a) Метод Каплана — Меєра для цензурованих даних; b) на основі регресійної моделі Кокса за методом Ефрона
У підгрупових аналізах ЗВ КР був на користь пембролізумабу порівняно з іпілімумабом незалежно від статусу BRAF-мутації, попереднього лікування інгібіторами BRAF або MEK, рівня ЛДГ, розміру пухлини або наявності метастазів у головному мозку (рис. 4). 10-річний рівень ЗВ був вищим у групі пембролізумабу порівняно з групою іпілімумабу у всіх підгрупах, включно з пацієнтами із підвищеним рівнем ЛДГ (27,3 проти 14,7%), загальним розміром новоутворення 10 см (25,2 проти 13,6%) та метастазами в головний мозок (40,0 проти 27,6%).
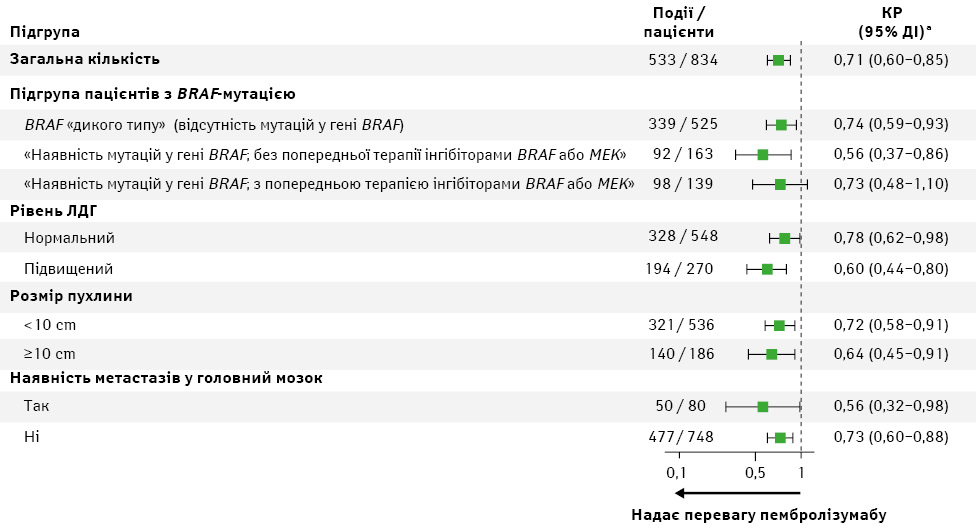
aНа основі моделі регресії Кокса за методом Ефрона
У загальній популяції 368 з 556 хворих (66,2%) у групі пембролізумабу та 181 з 278 пацієнтів (65,1%) у групі іпілімумабу отримали досліджуване лікування як першу лінію терапії. Серед цих осіб медіана ЗВ становила 38,7 міс (95% ДІ 27,3–50,9 міс) у групі пембролізумабу та 17,2 міс (95% ДІ 13,8–26,2 міс) у групі іпілімумабу (КР 0,68 (95% ДІ 0,55–0,86))(рис. 5a). 8-річний рівень ЗВ становив 40,1% у групі пембролізумабу та 27,0% у групі іпілімумабу; 10-річний рівень ЗВ становив 36,9 та 25,0% відповідно. Медіана модифікованої ВБП серед пацієнтів, які отримували досліджувану терапію як першу лінію терапії, становила 12,0 міс (95% ДІ 8,3–16,6 міс) у групі пембролізумабу та 4,1 міс (95% ДІ 2,9–5,2 міс) у групі іпілімумабу (КР 0,62 (95% ДІ 0,50–0,76)) (рис. 5b). 8-річний рівень модифікованої ВБП становив 27,0% у групі пембролізумабу та 15,1% у групі іпілімумабу; 10-річний рівень ЗВ становив 25,5 та 15,1% відповідно.
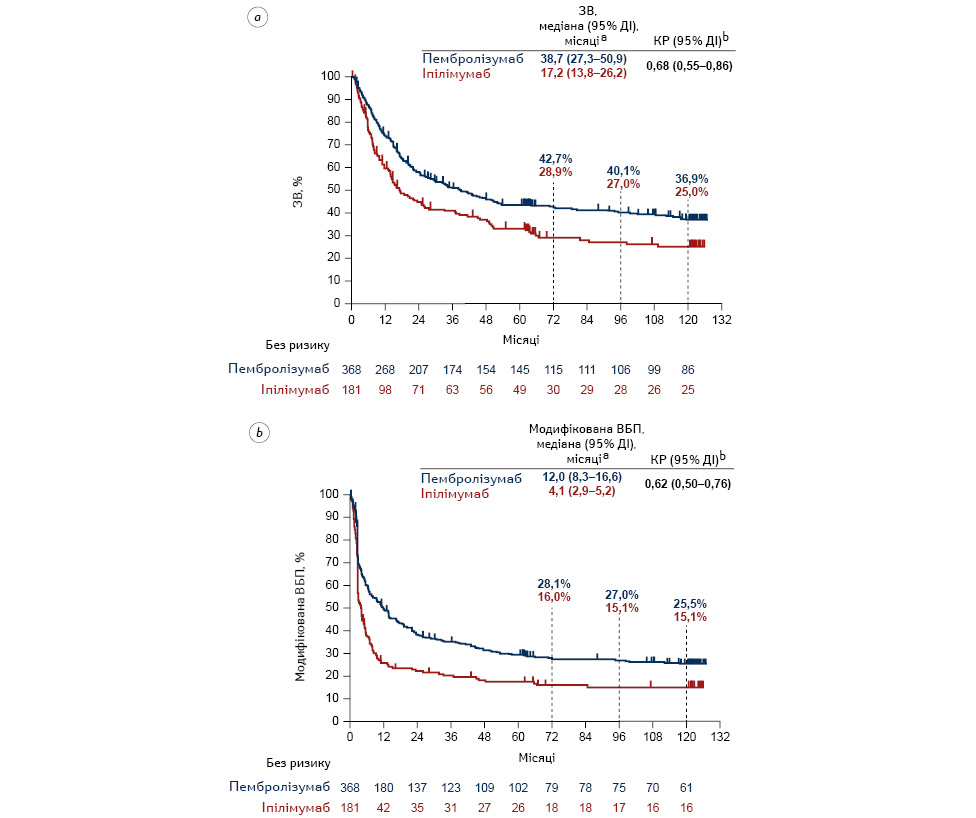
a) Метод Каплана — Меєра для цензурованих даних; b) на основі регресійної моделі Кокса за методом Ефрона
Серед пацієнтів, які отримали 2-й курс пембролізумабу за протоколом досліджень KEYNOTE-006 або KEYNOTE-587 (n=16), у 4 пацієнтів досягнуто ПВ, у 5 хворих досягнуто ЧВ, у 5 — спостерігали СХ і у 2 — прогресування захворювання. Медіана модифікованої ВБП з початку 2-го курсу лікування становила 51,8 міс (95% ДІ 11,0–НД) (рис. 6). 4-річний рівень модифікованої ВБП з початку 2-го курсу пембролізумабу становив 56,3%, а 6-річний рівень модифікованої ВБП — 49,2%.
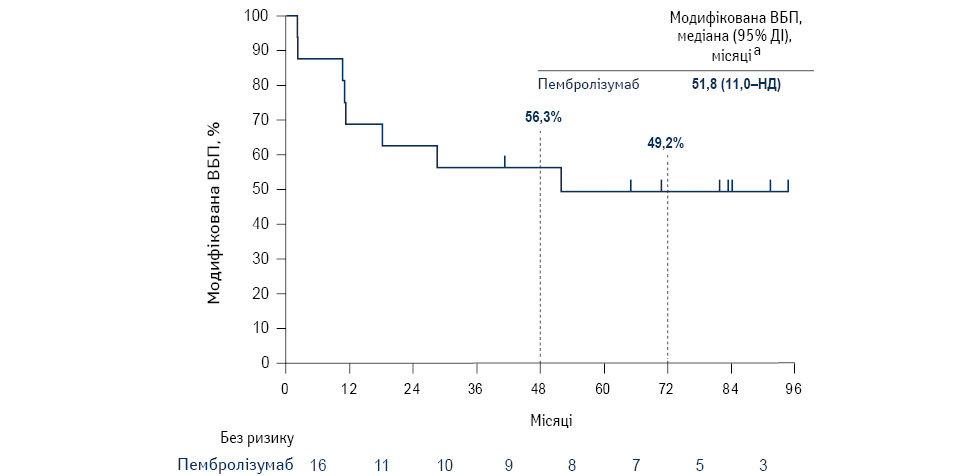
aЗа методом Каплана — Меєра для виключених даних.
Обговорення
У цьому 10-річному спостереженні дослідження KEYNOTE-006 застосування пембролізумабу продовжувало зумовлювати підвищення ЗВ та ВБП порівняно з іпілімумабом у пацієнтів із нерезектабельною або метастатичною меланомою, які раніше не отримували іпілімумаб. Тенденції щодо показників виживаності відповідали тим, що зафіксовані під час 7-річного спостереження [8]. Медіана ЗВ була підвищена у групі пембролізумабу в загальній популяції і, за оцінками, через 10 років 34,0% усіх хворих у групі пембролізумабу залишалися живими порівняно з 23,6% у групі іпілімумабу. ЗВ була особливо високою серед пацієнтів, які проходили лікування пембролізумабом довше 94 тиж, причому медіани ЗВ з 94-го тиж не досягнуто, а 8-річний рівень ЗВ становив 80,8%. Це можна пояснити тим, що пацієнти, у яких не відмічали прогресування хвороби або які продовжували терапію для отримання додаткової клінічної користі після прогресування, мають вищу ймовірність тривалої виживаності.
В оцінці КР для ЗВ також встановлено перевагу пембролізумабу у всіх підгрупах незалежно від наявності BRAF-мутації, попереднього лікування інгібіторами BRAF або MEK, а також від несприятливих прогностичних факторів, таких як підвищений рівень ЛДГ, розмір пухлини >10 см та метастази в головний мозок.
10-річний рівень ЗВ у пацієнтів із попередньо лікованими та стабільними метастазами в головний мозок становив 40,0% у групі пембролізумабу проти 27,6% у групі іпілімумабу, при цьому медіана ЗВ становила 53,4 міс проти 10,8 міс (КР 0,56 (95% ДІ 0,32–0,98)) відповідно, що може мати клінічне значення для цієї підгрупи пацієнтів з несприятливим прогнозом. Модифікована ВБП також була вищою у групі пембролізумабу в загальній популяції і, за оцінками, у 22,0% хворих не зафіксовано прогресування хвороби через 10 років порівняно з 12,8% у групі іпілімумабу. У першому аналізі меланомоспецифічної виживаності показники були вищими у групі пембролізумабу: медіана меланомоспецифічної виживаності становила 4,3 року проти 1,4 року у групі іпілімумабу. Пацієнти з ПВ або ЧВ мали вищі показники ЗВ, модифікованої ВБП і меланомоспецифічної виживаності порівняно з хворими із СХ. Важливим відкриттям стало те, що під час 2-го курсу пембролізумабу виявлено додаткову протипухлинну активність. [8]. Адже як і під час 7-річного спостереження, деякі пацієнти, які отримали 2-й курс пембролізумабу після припинення терапії та подальшого прогресування захворювання, продовжували отримувати користь від повторного застосування пембролізумабу.
Цей аналіз є найдовшим спостереженням у проспективному дослідженні, яке вивчає ефективність інгібітора PD-1 у пацієнтів із поширеною меланомою. Результати відповідали тим, що фіксували під час 7-річного спостереження дослідження KEYNOTE-006 [8]. Хоча прямі порівняння між дослідженнями мають певні обмеження, поточні результати пембролізумабу є сприятливими порівняно з результатами пацієнтів, які отримували іпілімумаб в інших дослідженнях, в яких медіана ЗВ становила 11,4 міс, а рівень 3-річної ЗВ становив 22% [10]. Відомо, що в метааналізі іпілімумабу крива ЗВ стабілізувалася через близько 3 роки спостереження з періодом до 10 років.
Єдині інші довгострокові дані про інгібітори PD-1 у цьому контексті походять з 7,5-річного спостереження в дослідженні CheckMate 067 фази III. У ньому встановлено, що комбінація ніволумабу з іпілімумабом, а також монотерапія ніволумабом зумовлюють стійку відповідь і стабільну криву виживаності у осіб із поширеною меланомою. Крім того, монотерапія ніволумабом виявилася ефективнішою за монотерапію іпілімумабом щодо показників ЗВ і меланомоспецифічної виживаності [11]. У дослідженні фази II/III RELATIVITY-047 застосування ніволумабу поєднано з анти-LAG-3 антитілом релатлімабом у пацієнтів з раніше не лікованою нерезектабельною або метастатичною меланомою сприяло значному підвищенню ВБП порівняно з монотерапією ніволумабом, хоча ця комбінація не досягла статистично значущих показників для ЗВ [12, 13].
Незважаючи на значне підвищення виживаності, яке забезпечують інгібітори PD-1, близько 60% усіх хворих із поширеною меланомою все ще помирають протягом 5 років після лікування пембролізумабом, тому залишається необхідність розв’язання питань первинної та набутої резистентності та оптимізації комбінацій імунотерапії. Основне обмеження цього аналізу полягає в тому, що не всі пацієнти, які мали право на перехід у дослідження KEYNOTE-587, погодилися на подальше спостереження. Однак вихідні характеристики хворих, які перейшли до KEYNOTE-587, були подібними до тих, що були у всіх пацієнтів, залучених до KEYNOTE-006.
Результати цього 10-річного спостереження пацієнтів в KEYNOTE-006 підтверджують, що пембролізумаб забезпечує довгострокові переваги у виживаності щодо осіб з нерезектабельною меланомою, які раніше не отримували іпілімумаб. Крім того, у результатах встановлено, що деякі хворі отримують користь від повторного лікування пембролізумабом. Ці дані підтверджують доцільність застосування пембролізумабу в таких випадках і підкреслюють його здатність перетворити меланому з гострої, смертельної хвороби на хронічне, тривале захворювання у значної частини пацієнтів.
Адаптований переклад за Long, G. V., Carlino, M. S., McNeil, C., Ribas, A., Gaudy-Marqueste, C., Schachter, J., … Robert, C. (2024). Pembrolizumab versus ipilimumab for advanced melanoma: 10-year follow-up of the phase III KEYNOTE-006 study. Ann. Oncol. doi.org/10.1016/j.annonc.2024.08.2330.
Стаття друкується у скороченому вигляді.
Список використаної літератури знаходиться в редакції.
Ірина Неміш














Leave a comment