Переваги та ризики застосування інгібіторів CDK4/6, зокрема палбоциклібу, у першій лінії терапії HR+ метаcтатичного раку молочної залози
Резюме. Рак молочної залози (РМЗ) є найбільш поширеним онкологічним захворюванням у жінок і провідною причиною смертності, а гормон-рецептор-позитивний (HR+) РМЗ є одним із найпоширеніших підтипів. Ендокринна терапія (ЕТ), зокрема на основі інгібіторів ароматази (ІА), є стандартом лікування HR+ РМЗ, але її ефективність обмежується розвитком резистентності до терапії. Інгібітори циклінзалежних кіназ (CDK) 4/6, такі як палбоцикліб, значно розширили можливості лікування HR+ РМЗ, зупиняючи клітинний цикл пухлинних клітин на фазі G1. Палбоцикліб у комбінації з ІА або фулвестрантом зумовлює значне підвищення виживаності без прогресування (ВБП), перевищуючи ефективність монотерапії ЕТ у постменопаузальних і пременопаузальних жінок. Проте комбінована терапія асоціюється з підвищеним ризиком токсичності, зокрема нейтропенії III–IV ступенів, що потребує ретельного моніторингу та корекції дози. Серії досліджень PALOMA підтверджують ефективність палбоциклібу для різних груп пацієнтів із HR+/HER2−− метастатичним РМЗ, а його застосування рекомендоване в міжнародних клінічних протоколах (Національної мережі багатопрофільних онкологічних закладів США (National Comprehensive Cancer Network — NCCN), Європейського товариства медичної онкології (European Society for Medical Oncology — ESMO), Американської спільноти клінічних онкологів (American Society of Clinical Oncology — ASCO)). Палбоцикліб у першій лінії терапії є ефективним вибором для довготривалого контролю за захворюванням, підвищення якості життя та управління ендокринною резистентністю. Водночас персоналізований підхід до терапії є ключовим для забезпечення балансу між клінічною ефективністю та безпекою лікування.
DOI: 10.32471/clinicaloncology.2663-466X.56-4.33705
 РМЗ є найбільш часто діагностованим новоутворенням у всьому світі та основною причиною смертності жінок від онкологічних захворювань [1]. Статус рецепторів РМЗ впливає на лікування та прогноз онкопатології, а також на експресію певних генів, що пов’язано з прогнозом різних підтипів РМЗ, серед яких одним із найпоширеніших є HR+ РМЗ. Стандартним методом лікування HR+ РМЗ є ЕТ на основі ІА, проте внаслідок прогресування хвороби через розвиток резистентності до терапії фіксуються труднощі в подальшому лікуванні. Значним проривом у терапії HR+ РМЗ стала поява CDK 4/6, які зумовлюють протипухлинну активність, сприяючи зупинці клітин у фазі G1. Останніми роками кілька інгібіторів CDK схвалено для лікування жінок із метастатичним HR+ РМЗ. До рекомендованих препаратів належать палбоцикліб, рибоцикліб, абемацикліб. У китайських настановах зазначається про те, що на ранніх етапах HR+ прогресуючого РМЗ рекомендовано поєднувати CDK4/6-інгібітори з ІА. Дані мережевого метааналізу (NMA) також підтверджують ефективність додавання інгібіторів CDK4/6 до ЕТ [2]. Проте необхідно чітко оцінити переваги та ризики комбінованого застосування інгібіторів CDK 4/6 з ET при HR+ РМЗ.
РМЗ є найбільш часто діагностованим новоутворенням у всьому світі та основною причиною смертності жінок від онкологічних захворювань [1]. Статус рецепторів РМЗ впливає на лікування та прогноз онкопатології, а також на експресію певних генів, що пов’язано з прогнозом різних підтипів РМЗ, серед яких одним із найпоширеніших є HR+ РМЗ. Стандартним методом лікування HR+ РМЗ є ЕТ на основі ІА, проте внаслідок прогресування хвороби через розвиток резистентності до терапії фіксуються труднощі в подальшому лікуванні. Значним проривом у терапії HR+ РМЗ стала поява CDK 4/6, які зумовлюють протипухлинну активність, сприяючи зупинці клітин у фазі G1. Останніми роками кілька інгібіторів CDK схвалено для лікування жінок із метастатичним HR+ РМЗ. До рекомендованих препаратів належать палбоцикліб, рибоцикліб, абемацикліб. У китайських настановах зазначається про те, що на ранніх етапах HR+ прогресуючого РМЗ рекомендовано поєднувати CDK4/6-інгібітори з ІА. Дані мережевого метааналізу (NMA) також підтверджують ефективність додавання інгібіторів CDK4/6 до ЕТ [2]. Проте необхідно чітко оцінити переваги та ризики комбінованого застосування інгібіторів CDK 4/6 з ET при HR+ РМЗ.
Оцінка ефективності та безпеки комбінованого застосування інгібіторів CDK4/6 та ET порівняно з монотерапією ET у пацієнток із HR+ РМЗ
У систематичному огляді та метааналізі C. Messina та співавт. (2018) проведено оцінку ефективності комбінованого застосування інгібіторів CDK4/6 та ET порівняно з монотерапією ET у осіб із HR+ РМЗ. Встановлено, що додавання інгібіторів CDK4/6 до ЕТ у хворих, чутливих до ЕТ (коефіцієнт ризику (КР) = 0,55; 95% довірчий інтервал (ДІ) 0,50–0,62), або у пацієнтів, резистентних до ЕТ (КР=0,51; 95% ДІ 0,43–0,61), супроводжувалося значним підвищенням ВБП при метастатичному HR+ РМЗ незалежно від менопаузального статусу та місця метастазування. Крім того, застосування інгібіторів CDK4/6 поєднано з ЕТ суттєво підвищило частоту об’єктивної відповіді (ЧОВ) у осіб, чутливих до ЕТ (ЧОВ=0,62; 95% ДІ 0,52–0,73), або хворих, резистентних до ЕТ (ЧОВ=0,33; 95% ДІ 0,24–0,47). Проте лікування інгібіторами CDK4/6 поєднано з ЕТ асоціювалося з вищим ризиком розвитку побічних ефектів (ПЕ) III–IV ступенів, які відмічалися у 71,2% усіх пацієнток з комбінованим застосуванням інгібіторів CDK4/6 з ЕТ та у 23,3% групи прийому тільки ET. Найбільш поширеним ускладненням була нейтропенія. Тобто в результатах дослідження підтверджено ефективність інгібіторів CDK4/6 поєднано з ET у осіб із HR+ РМЗ, хоча ризик токсичності залишається суттєвим фактором при виборі цієї терапії [1]. У метааналізі F. Schettini та співавт. (2020) зафіксовано, що комбінації інгібіторів CDK4/6 та ЕТ порівняно з використанням тільки ЕТ забезпечують підвищення загальної виживаності (ЗВ) незалежно від віку, менопаузального статусу, ендокринної чутливості та вісцерального ураження, тому їм слід віддавати перевагу як початковій терапії замість ендокринної монотерапії [3].
Порівняльна оцінка ефективності і безпеки 3 інгібіторів CDK4/6 (палбоциклібу, рибоциклібу, абемациклібу) у комбінації з ЕТ у пацієнтів з HR+/HER2− метастатичним або прогресуючим РМЗ
Y. Liu та співавт. (2023) описують дані мережевого метааналізу порівняльної оцінки ефективності та безпеки комбінацій, що включають 3 інгібітори CDK4/6 (палбоцикліб, рибоцикліб, абемацикліб), і ЕТ у пацієнтів з HR+/HER2− метастатичним або прогресуючим РМЗ. Встановлено, що усі комбінації значно підвищували ВБП порівняно з монотерапією ІА або фулвестрантом. Проте застосування палбоциклібу із фулвестрантом порівняно з іншими інгібіторами CDK4/6 (рибоциклібу, абемациклібу) супроводжувалося найвищою ймовірністю отримання переваг щодо показника ВБП (37,65%), тоді як застосування палбоциклібу з IА поступалося іншим комбінаціям щодо підвищення показника ЗВ. Крім того, застосування палбоциклібу в комбінації з IА або фулвестрантом асоціювалося з найвищим ризиком ПЕ III–IV ступенів, включно з нейтропенією. Однак у цьому дослідженні незрозуміло, чи отримували пацієнти лікування першої лінії, що певною мірою вплине на результати у хворих, які раніше не отримували терапії [4]. У дослідженні X. Guan та співавт. (2023) наводяться дані систематичного огляду та метааналізу ефективності та безпеки інгібіторів CDK4/6 у лікуванні першої лінії HR+ поширеного РМЗ. Зафіксовано, що застосування абемациклібу супроводжувалося найбільшою користю (показник років без прогресування (Progression-free life years — PFLYs) становив 3,059), при цьому рибоцикліб і палбоцикліб зумовили дещо гірші результати (показник PFLYs становив 2,636 та 2,302 відповідно), ніж в абемациклібу, але значно кращі, ніж при монотерапії ІА (показник PFLYs становив 2,047). Найкращі результати ЗВ відмічалися при застосуванні рибоциклібу (показник років життя (life years — LYs) становив 6,543), при цьому палбоцикліб посідав 2-ге місце (показник LYs становив 6,351), випереджаючи результати застосування абемациклібу (показник LYs становив 6,275) і ІА (показник LYs становив 6,016). При оцінці безпеки застосування інгібіторів CDK4/6 встановлено, що загальний ризик для всіх інгібіторів CDK4/6 був підвищений (КР=9,84; 95% ДІ 8,13–11,95), особливо при застосуванні палбоциклібу (КР=14,04; 95% ДІ 10,52–18,90), при цьому гематологічна токсичність була найбільш виражена при застосуванні палбоциклібу і рибоциклібу. Серед ПЕ найчастіше траплялися нейтропенія (КР=105,53; 95% ДІ 65,24–183,09) і лейкопенія (КР=46,25; 95% ДІ 23,20–110,94). Тобто палбоцикліб залишається ефективним варіантом для пацієнтів із HR+/HER2− РМЗ, особливо у комбінаціях з фулвестрантом. Однак підвищений ризик ПЕ потребує індивідуального підходу до вибору терапії [2].
Ефективність та безпека палбоциклібу в серії клінічних досліджень
Палбоцикліб, перший у своєму класі інгібітор CDK4/6, схвалений для лікування HR+/HER2− метастатичного РМЗ у комбінації з ІА або фулвестрантом. Схвалення палбоциклібу в США Управлінням з контролю за якістю харчових продуктів і лікарських засобів (Food and Drug Administration — FDA) (ґрунтувалося на результатах 3 основних клінічних досліджень: PALOMA-1, PALOMA-2, в яких оцінювали застосування палбоциклібу в комбінації з летрозолом порівняно з монотерапією летрозолом або плацебо поєднано з летрозолом як початкове лікування для жінок у період постменопаузи на пізніх стадіях, та PALOMA-3, в якому оцінювали ефективність комбінованого лікування палбоциклібом з фулвестрантом порівняно з монотерапією фулвестрантом у жінок у період пре- чи постменопаузи, у яких відмічалося прогресування хвороби після ЕТ. Крім того, сучасні дані наукової літературні наводять результати порівняльної ефективності палбоциклібу поєднано з летрозолом порівняно з монотерапією летрозолом при HR+/HER2− метастатичному РМЗ в умовах реальної клінічної практики. У реальному клінічному аналізі застосування палбоциклібу в комбінації з ІА зумовлювало значно вищу медіану ВБП (20 міс) порівняно з монотерапією ІА (11,9 міс, КР=0,58; 95% ДІ 0,49–0,69; p <0,0001) (рис. 1). Це свідчить про значне зниження ризику прогресування захворювання у пацієнток з HR+/HER2− метастатичним РМЗ при застосуванні палбоциклібу в комбінації з ІА. Медіани ЗВ не досягнуто в групі палбоциклібу поєднано з летрозолом, вона становила 43,1 міс у групі застосування тільки летрозолу (КР=0,66; 95% ДІ 0,53–0,82; p =0,0002) (рис. 2). Незважаючи на те що результати досліджень PALOMA демонструють ефективність палбоциклібу серед пацієнтів, які відповідали критеріям включення та виключення з дослідження, реальні докази ефективності палбоциклібу надають додаткову підтримку для ухвалення клінічних рішень у хворих, які виявляються в рутинній клінічній практиці [5].
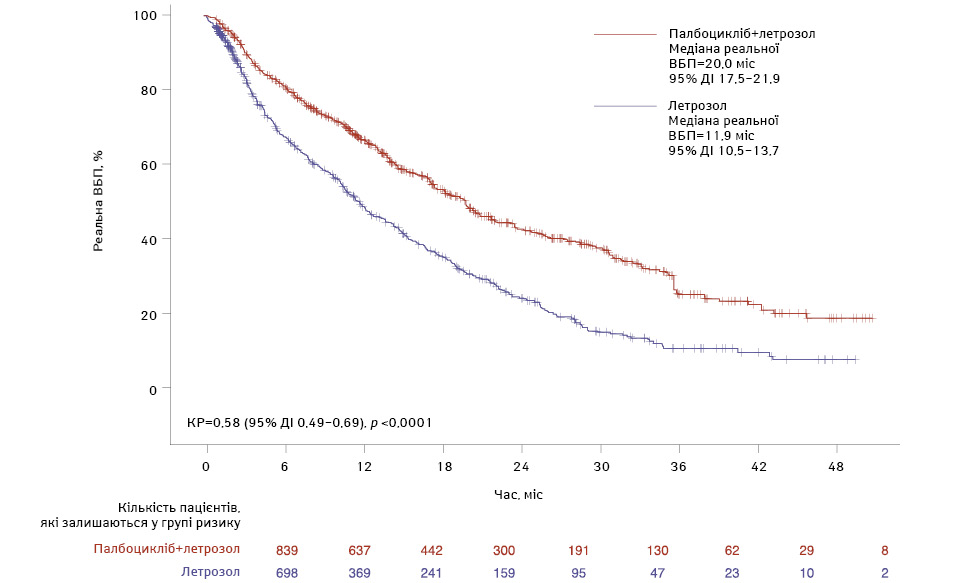
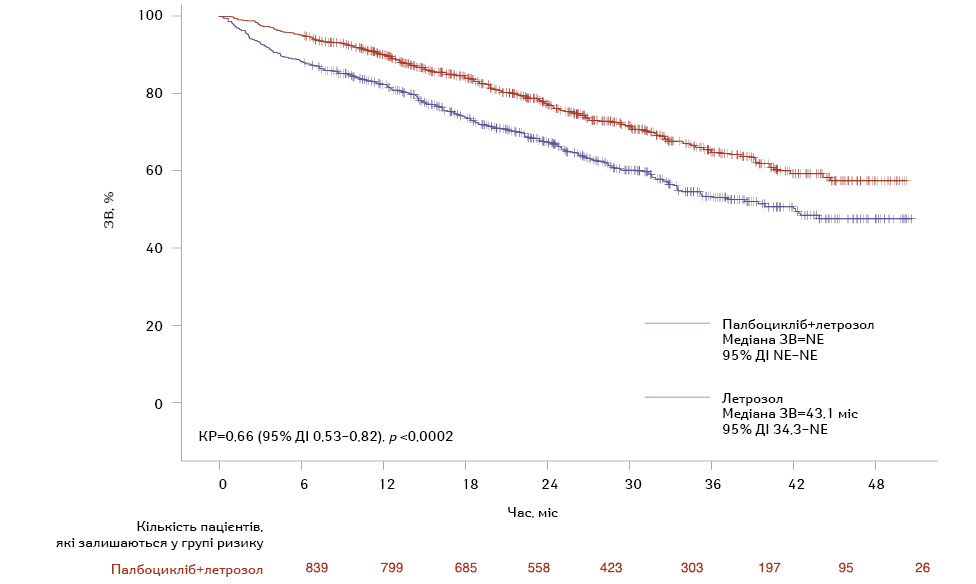
Примітка: NE — не піддається оцінці.
Палбоцикліб у світлі сучасних рекомендацій
У клінічних практичних рекомендаціях ESMO щодо діагностики, визначення стадії та лікування пацієнтів з метастатичним РМЗ 2021 р. зазначається про те, що інгібітори CDK4/6 у комбінації з ЕТ є стандартом терапії першої лінії HR-позитивного, HER2-негативного метастатичного РМЗ, оскільки застосування такої комбінації препаратів супроводжувалося підвищенням ВБП, ЗВ та характеризувалося сприятливим профілем безпеки. Ця комбінація рекомендована як альтернатива хімієтерапії через більш низьку токсичність та аналогічну або вищу ефективність. Для пацієнтів, які не рецидивували на ІА або упродовж 12 міс після завершення ад’ювантної терапії ІА, рекомендовано призначати комбінацію інгібітора CDK4/6 з ІА. Для пацієнтів, в яких відмічався рецидив на ІА або протягом 12 міс після завершення ад’ювантної терапії, рекомендовано застосовувати комбінацію інгібітора CDK4/6 з фулвестрантом. Інгібітори CDK4/6 ефективні у випадках первинної чи вторинної ендокринної резистентності, при рецидивах або de novo метастатичному РМЗ у жінок у період пре-та постменопаузи. ЕТ без інгібіторів CDK4/6 слід розглядати лише для пацієнтів із серйозними супутніми захворюваннями або низьким показником працездатності, який унеможливлює проведення комбінованої терапії [6].
У 5-му міжнародному узгодженому керівництві Європейська школа онкології (European School of Oncology — ESO) — ESMO для поширеного РМЗ 2020 р. зазначається, що використання інгібітора CDK4/6 поєднано з ET для хворих з поширеним РМЗ, а саме палбоциклібу з фулвестрантом у другій лінії супроводжувалося підвищенням якості життя пацієнтів (оцінка ESMO — величини шкали клінічної користі (Magnitude of Clinical Benefit Scale — MCBS) v1.1: 4) [7]. Згідно з Клінічними практичними настановами NCCN (версія 4.2024), рекомендованою схемою системної терапії HR+ рецидивного нерезектабельного (локального чи регіонарного) або IV стадії РМЗ у фазі постменопаузи є палбоцикліб у комбінації з ІА [8]. У настановах ASCO 2024 р. зазначається про те, що ІА поєднано з інгібітором CDK4/6 рекомендований для осіб із HR-позитивним РМЗ із прогресуванням захворювання, які знаходяться в періоді постменопаузи [9]. У настановах Німецької програми рекомендацій в онкології щодо раннього виявлення, діагностики, лікування та спостереження хворих на РМЗ 2021 р. зазначається, що ЕТ поєднано з таргетною терапією (наприклад палбоцикліб + ІА) рекомендована для пацієнток у період постменопаузи з HR+, HER2− статусом. При цьому комбінація палбоциклібу та ІА рекомендована, якщо раніше ці препарати не застосовували [10]. Отже, палбоцикліб у комбінації з ІА є стандартом терапії першої лінії для HR+, HER2− метастатичного РМЗ у пацієнток у період постменопаузи. Терапія спрямована на ефективний контроль захворювання із мінімальною токсичністю.
Проте на шляху застосування інгібіторів CDK4/6 лікарі неодноразово стикаються з розвитком ПЕ. Одним з найпоширеніших ПЕ III–IV ступенів є нейтропенія. У дослідженні W. Wang та співавт. (2024) зазначається про те, що одним зі шляхів зменшення вираженості ПЕ є коригування дози, що є особливо актуальним при розвитку нейтропенії. Крім того, часто для того, щоб зменшити вираженість ПЕ, рекомендовано доповнювати системну терапію місцевим лікуванням, яке включає хірургічне втручання, променеву терапію, радіочастотну абляцію та інтервенційну терапію. Оскільки відповідне місцеве лікування має потенціал для зменшення вираженості болю у пацієнтів, ефективного лікування потенційно небезпечних для життя ускладнень і надає хворим можливість пройти додаткові цикли системної терапії. Крім того, важливим у контролі розвитку ПЕ є постійний моніторинг показників крові, що дозволить визначити зміни на ранньому етапі та вжити відповідних заходів з його корекції [11].
Тобто палбоцикліб у комбінації з ІА або фулвестрантом є універсальним і ефективним підходом у терапії метастатичного РМЗ. Персоналізація лікування базується на характеристиках пацієнток, таких як чутливість до ЕТ, менопаузальний статус, супутні захворювання та переносимість лікування. Цей підхід дозволяє оптимізувати баланс між ефективністю терапії та ризиком ПЕ, забезпечуючи найкращі результати для кожної категорії хворих.
Так, серії клінічних досліджень свідчать про те, що палбоцикліб у комбінації з ІА або фулвестрантом є ефективним стандартом терапії першої лінії для HR+/HER2− метастатичного РМЗ, забезпечуючи тривалий контроль захворювання і підвищення якості життя. Проте підвищений ризик токсичності потребує ретельного моніторингу стану пацієнток і індивідуального підходу до вибору схеми лікування.
Список використаної літератури
1. Messina, C., Cattrini, C., Buzzatti, G., Cerbone, L., Zanardi, E., Messina, M., & Boccardo, F. (2018). CDK4/6 inhibitors in advanced hormone receptor-positive/HER2-negative breast cancer: a systematic review and meta-analysis of randomized trials. Breast Cancer Research and Treatment, 172(1), 9–21. doi: 10.1007/s10549-018-4901-0.
2. Guan, X., Li, M., Ji, X., Wang, Y., & Tian, L. (2024). Confirming the efficacy and safety of CDK4/6 inhibitors in the first-line treatment of HR+ advanced breast cancer: a systematic review and meta-analysis. Frontiers in Pharmacology, 15, 1369420. doi: 10.3389/fphar.2024.1369420.
3. Schettini, F., Giudici, F., Giuliano, M., Cristofanilli, M., Arpino, G., Del Mastro, L., … Generali, D. (2020). Overall Survival of CDK4/6-Inhibitor-Based Treatments in Clinically Relevant Subgroups of Metastatic Breast Cancer: Systematic Review and Meta-Analysis. Journal of the National Cancer Institute, 1, 112(11), 1089–1097. doi: 10.1093/jnci/djaa071.
4. Liu, Y., Wu, J., Ji, Z., Chen, L., Zou, J., Zheng, J., … Li, Z. (2023). Comparative efficacy and safety of different combinations of three CDK4/6 inhibitors with endocrine therapies in HR+/HER-2 − metastatic or advanced breast cancer patients: a network meta-analysis. BMC Cancer, 23, 816. doi: 10.1186/s12885-023-11322-2.
5. DeMichele, A., Cristofanilli, M., Brufsky, A., Liu, X., Mardekian, J., McRoy, L., …Finn, R. S. (2021). Comparative effectiveness of first-line palbociclib plus letrozole versus letrozole alone for HR+/HER2− metastatic breast cancer in US real-world clinical practice. Breast Cancer Research, 23, 37. doi: 10.1186/s13058-021-01409-8.
6. Gennari, A., André, F., Barrios, C. H., Cortés, J., de Azambuja, E., DeMichele A., … ESMO Guidelines Committee (2021). ESMO Clinical Practice Guideline for the diagnosis, staging and treatment of patients with metastatic breast cancer. Annals of oncology, 32(12), 1475–1495. doi: 10.1016/j.annonc.2021.09.019.
7. Cardoso, F., Paluch-Shimon, S., Senkus, E., Curigliano, G., Aapro, M. S., André, F., … Winer, E. P. (2020). 5th ESO–ESMO international consensus guidelines for advanced breast cancer (ABC 5). Annals of Oncology, 31(12), 1623–1649. doi: 10.1016/j.annonc.2020.09.010.
8. Gradishar, W. J., Moran, M. S., Abraham, J., Abramson, V., Aft, R., Agnese, D., … Kumar, R. (2024). Breast Cancer, Version 3.2024, NCCN Clinical Practice Guidelines in Oncology. Journal of the National Comprehensive Cancer Network, 22(5), 331–357. doi: 10.6004/jnccn.2024.0035.
9. Al Sukhun, S., Temin, S., Barrios, C. H., Antone, N. Z., Guerra, Y. C., Chavez-MacGregor, M., … Arun, B. K. (2024). Systemic Treatment of Patients With Metastatic Breast Cancer: ASCO Resource-Stratified Guideline. JCO Global Oncology, 10, e2300285. doi: 10.1200/GO.23.00285.
10. German Guideline Program in Oncology (GGPO). Evidence-based Guideline for the Early Detection, Diagnosis, Treatment and Follow-up of Breast Cancer (2021). Retrieved from http://www.leitlinienprogramm- onkologie.de/fileadmin/user_upload/S3_Guideline_Breast_Cancer.pdf.
11. Wang, W., Lei, W., Fang, Z., Jiang, R., & Wang, X. (2024). Efficacy, safety, and predictive model of Palbociclib in the treatment of HR-positive and HER2-negative metastatic breast cancer. BMC Cancer, 24, 1. doi: 10.1186/s12885-023-11764-8.














Leave a comment