Одномоментна тромбектомія з гілок легеневої артерії та нижньої порожнистої вени при ускладненому адренокортикальному раку лівого наднирника
Скумс А.В., Габрієлян А.В., Гурін П.В., Симонов О.М., Кропельницький В.О., Скумс А.А.
Резюме. Представляємо клінічний випадок успішного симультанного хірургічного лікування пацієнта з адренокортикальним раком (АКР) лівого наднирника, ускладненим пухлинним тромбозом нижньої порожнистої вени (НПВ) та масивною тромбоемболією легеневої артерії (ТЕЛА). Пацієнт, 52 роки, з діагнозом АКР лівого наднирника, тромбозом НПВ та клінічними проявами ТЕЛА. За даними магнітно-резонансної томографії (МРТ) та мультиспіральної комп’ютерної томографії (МСКТ), виявлено пухлину лівого наднирника діаметром 20 см з пухлинним тромбозом лівої ниркової вени та НПВ, а також тромби в обох гілках легеневої артерії. За шкалою індексу тяжкості ТЕЛА (Pulmonary Embolism Severity Index — PESI), ризик смерті протягом 30 днів був дуже високий (162 бали). Проведено симультанну операцію: тромбектомію з гілок легеневої артерії, лівобічну адреналектомію, тромбектомію з лівої ниркової вени та НПВ. Післяопераційний період пройшов без ускладнень. На 14-ту добу хворий виписаний зі стаціонару в задовільному стані. Патогістологічно підтверджено АКР наднирника з пухлинним тромбом. Наведений клінічний випадок демонструє можливість успішного виконання симультанної операції при поєднанні АКР з венозною інвазією та ТЕЛА за умови своєчасної діагностики та наявності мультидисциплінарної команди. Висновки. Пацієнти з місцево-поширеними пухлинами наднирників з висхідними пухлинними тромбозами НПВ представляють складну групу хворих з підвищеним периопераційним ризиком, лікування яких має проводитися в умовах багатопрофільних спеціалізованих центрів.
Одержано 12.06.2024
Прийнято до друку 25.06.2024
DOI: 10.32471/clinicaloncology.2663-466X.55-3.32938
Вступ
АКР — рідкісна злоякісна пухлина надниркових залоз з частотою виникнення 0,5–2 випадки на 1 млн населення щороку [1]. Характерною особливістю АКР є здатність до венозної інвазії з формуванням пухлинних тромбів, які можуть поширюватися просвітом вен і призводити до тромбозу НПВ. Така ситуація відмічається у третини пацієнтів з АКР, причому при лівобічній локалізації пухлини тромбоз НПВ розвивається рідше — у близько 20% усіх випадків [2, 3].
Іншим грізним ускладненням злоякісних пухлин, зокрема АКР, є ТЕЛА. У хворих з АКР вона може розвиватися як унаслідок фрагментації пухлинного тромбу НПВ, так і через гіперкоагуляцію та венозний стаз. На жаль, статистичних даних щодо частоти розвитку ТЕЛА при АКР наразі недостатньо через рідкісність цієї патології [4, 5].
Лікування АКР, ускладненого пухлинною венозною інвазією, полягає в радикальному хірургічному видаленні пухлини разом з тромбом з НПВ. Однак при супутній ТЕЛА тактика лікування досі чітко не встановлена через відсутність стандартів і рекомендацій. У медичній літературі описані поодинокі випадки успішного лікування таких пацієнтів з використанням різних підходів — від антикоагулянтної терапії з відтермінуванням операції до симультанного видалення тромбів з легеневої артерії та НПВ [6–8].
У цій статті ми представляємо власне клінічне спостереження успішного симультанного хірургічного лікування пацієнта з АКР лівого наднирника, ускладненого масивною ТЕЛА та пухлинним тромбозом НПВ.
Клінічний випадок
Пацієнт С., 52 роки, госпіталізований 18.04.2022 р. у відділ хірургії поєднаної патології та захворювань заочеревинного простору Національного наукового центру хірургії та трансплантології (ННЦХТ) ім. О.О.Шалімова НАМН України з діагнозом АКР лівого наднирника, тромбоз НПВ. Хворий скаржився на виражену задишку як при ходьбі, так і в стані спокою, загальну слабкість, помірний біль у лівій поперековій зоні.
Розвиток болю відмітив 9.04.2022 р. У лікарні за місцем проживання, за результатами МРТ, виявлено гіповаскулярне об’ємне утворення в проєкції лівого наднирника розміром 15×12 см з ділянками некрозу, розцінене як АКР з пухлинним тромбозом лівої ниркової вени та НПВ (рис. 1).
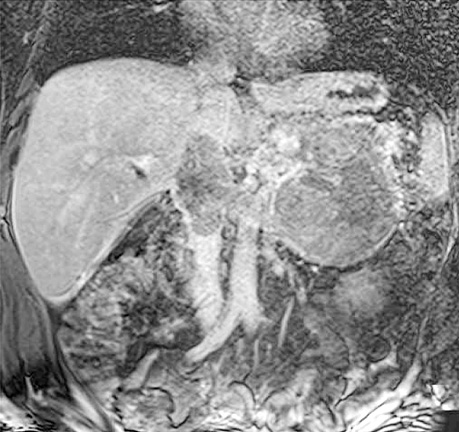
Там же під час проведення МСКТ 14.04.2022 р. у пацієнта виникли задишка, загальна слабкість із втратою свідомості, що було розцінено як анафілактичний шок на введення контрастної речовини.
При огляді у відділенні: стан хворого тяжкий. Скарги на задишку, відчуття нестачі повітря, страху смерті, виражену загальну слабкість. Артеріальний тиск (АТ) = 130–150/100 мм рт.ст.; частота дихання (ЧД) = 28–30 уд./хв; рівень насичення крові киснем (SpO2) = 92–89%. Зріст — 192,0 см, маса тіла — 105,0 кг.
При ехокардіографічному дослідженні (18.04.2022 р.) виявлено розширення правих відділів серця та легеневу гіпертензію (61 мм рт.ст.).
За результатами МСКТ (18.04.2022 р.), у проєкції лівого наднирника зафіксоване об’ємне гетерогенне утворення діаметром 20 см, пухлинний тромбоз лівої ниркової вени та НПВ нижче рівня печінкових вен. У лівій та правій гілках легеневої артерії виявлені тромботичні маси, що на 80–90% перекривають їх просвіт та поширюються на сегментарні та субсегментарні гілки (рис. 2).
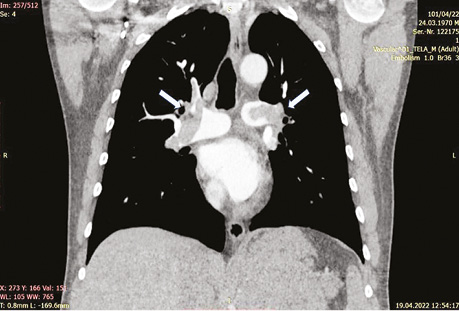
Для встановлення тактики лікування пацієнта проведений консиліум хірургів-онкологів, кардіохірургів та анестезіологів. Розглядали 3 можливі шляхи лікування: 1) медикаментозна терапія ТЕЛА з наступною операцією з приводу пухлини (тромболітична терапія, терапія антикоагулянтами, терапія правошлуночкової дисфункції); 2) першим етапом — тромбектомія з легеневої артерії, другим етапом — видалення пухлини; 3) симультанне втручання (тромбектомія з гілок легеневої артерії + видалення пухлини наднирника з тромбектомією з НПВ).
З урахуванням тяжкого стану хворого, дуже високого ризику смерті протягом 30 днів за шкалою PESI = 162 бали (клас V), ризику рецидиву тромбоемболії та втрати часу до хірургічного лікування пухлинного процесу — ухвалене рішення про необхідність одночасного послідовного виконання тромбектомії із легеневих артерій та адреналектомії з тромбектомією із НПВ та лівої ниркової вени.
21.04.2022 р. — проведено операцію. Загальна анестезія здійснювалася за допомогою севофлурану з керованим диханням за стандартною методикою. Інтраопераційний моніторинг передбачав реєстрацію артеріального тиску інвазивним методом, електрокардіограми в стандартних та грудних відведеннях, моніторинг температури тіла, центрального венозного тиску та пульсоксиметрію, встановлення концентрації севофлурану на вдиху та видиху, а також його мінімальну альвеолярну концентрацію (МАК). Перед виконанням основного етапу кардіохірургічної операції проводилася гепаринізація в дозі 300 ОД/кг маси тіла.
Після виконання серединної стернотомії розсічено перикард, підключено апарат штучного кровообігу (АШК). Штучна фібриляція. Виконано артеріотомію стовбура легеневої артерії. У ділянці її біфуркації і в гирлах дольових артерій виявлені множинні частково організовані тромби, місцями щільно фіксовані до стінки судин. Тромби вилучені. Додаткова ревізія із застосуванням катетера Фогарті — тромбів не виявлено (рис. 3). Отвір стовбура легеневої артерії зашито. Розсічена права гілка легеневої артерії. Також на біфуркації та в гирлах дольових артерій видалені множинні, частково організовані тромби. Проведено додаткову ревізію судин з використанням катетера Фогарті. Гілка легеневої артерії ушита.
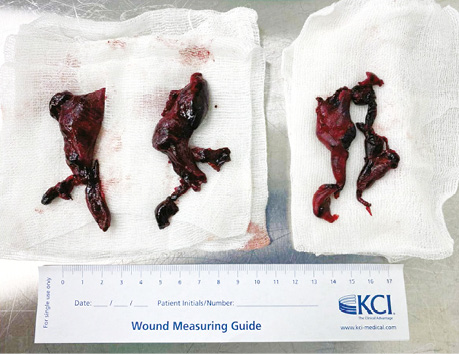
Дефібриляція. Підшиті 4 електроди. Проведена нейтралізація гепарину розчином протаміну сульфату в співвідношенні 1:1. Гемостаз. Післяопераційну рану зашито.
Виконано лапаротомію доступом Mercedes. У ділянці лівого наднирника виявляється пухлина діаметром близько 20,0 см. Запечінковий сегмент НПВ тромбований, починаючи з рівня впадіння лівої ниркової вени. Печінка мобілізована з перетином правої та лівої триангулярної, коронарної та серпоподібної зв’язок. Виділений запечінковий сегмент НПВ до рівня впадіння печінкових вен з прошиванням та пересіченням коротких вен. Виділені НПВ нижче зони тромбозу та права ниркова вена. Послідовно накладені судинні зажими на НПВ вище та нижче тромбованої ділянки, а також на праву ниркову вену. Через венотомію видалено пухлинний тромб НПВ та частково лівої ниркової вени, на яку накладений судинний затискач. У просвіт НПВ введено розчин гепарину. Розріз НПВ ушито однорядним атравматичним швом, відновлено кровотік. Далі мобілізовано ліву половину товстої кишки. Виділені тромбовані центральна вена наднирника та ліва ниркова вена. Центральна вена наднирника пересічена в місці впадіння з нирковою. Виконана венотомія лівої ниркової вени дистальніше тромбу. Після його видалення виконано пластику судин. Знято затискач, кровотік у нирковій вені відновлено. Лівобічна адреналектомія (рис. 4). Дренування заочеревинного простору справа та зліва.
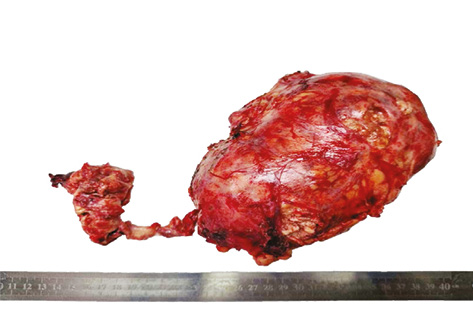
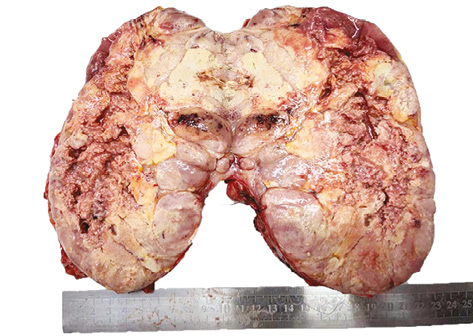
Тривалість оперативного втручання — 9 год 10 хв. Загальна крововтрата становила 1500 мл. Введено 1908 мл еритроцитарної маси, 1370 свіжозамороженої плазми крові та 250 мл тромбоцитарної маси. На наступну добу хворого екстубували. Протягом 3 діб потребував кисневої підтримки. У подальшому післяопераційний період проходив без ускладнень. Дренажі плевральної порожнини видалені на 7-му добу, заочеревинного простору — на 12-ту добу через значну лімфорею. Виписаний зі стаціонару на 14-ту добу після операції в задовільному стані. SpO2 у день виписки — 97%. За даними ультразвукової діагностики (УЗД) серця, артеріальний тиск у легеневій артерії становив 24 мм рт.ст.
Патогістологічний висновок: адренокортикальна карцинома наднирника з пухлинним тромбом у вені наднирника та НПВ. У легеневій артерії — змішаний тромб. pT4. ICD-O 8370/3 (рис. 5).
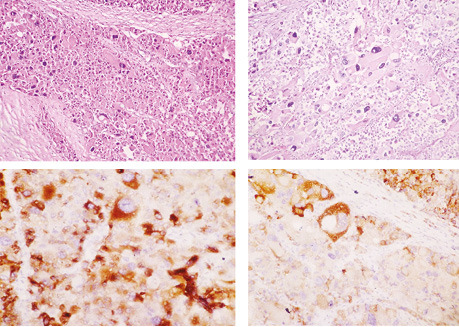
Дискусія
Карцинома кори надниркових залоз є рідкісною пухлиною з унікальною здатністю до розширення венозного пухлинного тромбу [1]. Хоча перший зареєстрований випадок ураження тромбом новоутворення порожнистої вени виявлений під час розтину в 1963 р. [9], лише в 1972 р. він був описаний інтраопераційно В. Castleman та співавт. [10]. Ураження пухлинним тромбом НПВ може відбуватися як шляхом прямого вторгнення, так і, частіше, внутрішньопросвітного розширення пухлинного тромбу через надниркову або ниркову вену. Найчастіше (80%) тромбоз НПВ виникає при ураженні правого наднирника, що може бути пов’язано з коротшою веною правого наднирника [2].
ТЕЛА є важливою проблемою громадського здоров’я. У серпні 2019 р. Європейським товариством кардіологів (European Society of Cardiology — ESC) у співпраці з Європейським респіраторним товариством (European Respiratory Society — ERS) опублікувало нові рекомендації щодо діагностики та лікування ТЕЛА [11]. Для оцінки прогнозу осіб з гострою ТЕЛА розроблено низку алгоритмів, що ґрунтуються на клінічних показниках, використання яких вважається досить обґрунтованим. Серед них — шкала PESI, яка є найбільш визнаною [11, 12]. Оцінка PESI допомагає встановити клінічний ступінь тяжкості і може впливати на вибір лікування для пацієнтів з ТЕЛА. Якщо індекс PESI >125 балів (клас ризику V), ризик вважається дуже високим і асоціюється з підвищеним ризиком настання смерті протягом 30 днів. За даними регістрів та когортних досліджень, ризик летального наслідку у цих хворих за PESI становив 24,5%. Пацієнту проводять дослідження функції правого шлуночка — ехокардіографію (Ехо-КГ). Особи, у яких підтверджено дисфункцію, мають бути віднесені до групи середнього-високого ризику. У цих випадках рекомендується ретельний моніторинг з метою раннього виявлення гемодинамічних порушень та розв’язання питання про початок реперфузійної терапії.
Пацієнтів з ТЕЛА лікують відповідно до їх гемодинамічного статусу та профілю ризику. Точніше, тромболізис рекомендується пацієнтам з ТЕЛА, які гемодинамічно нестабільні та мають підвищений ризик. Якщо тромболізис протипоказаний або безуспішний, можна розглянути хірургічну емболектомію легеневої артерії або черезшкірну катетер-спрямовану терапію [12–14]. Незважаючи на те що реперфузійна терапія може врятувати життя, вона не показана всім пацієнтам з ТЕЛА через підвищений ризик кровотечі [12, 13, 15]. Тривале лікування хворих з ТЕЛА включає антикоагулянтну терапію протягом щонайменше 3–6 міс [12]. Чи слід продовжити лікування після цього періоду, залежить від ризику рецидиву [12].
Статистичних даних щодо частки ТЕЛА у пацієнтів з АКР не виявлено [6]. Через рідкісність патології стандартів лікування осіб з такими поєднаними ускладненнями не розроблено. Охарактеризовані окремі клінічні випадки видалення пухлини наднирника та тромбектомії з НПВ після попередньої антикоагулянтної терапії з приводу ТЕЛА або виконання симультанного хірургічного втручання [6, 16, 17]. У більшості випадків хворі гинуть ще до початку лікування [18].
Висновок
У наведеному клінічному спостереженні представлено можливість успішного виконання симультанного хірургічного втручання — емболектомії з легеневих артерій, видалення лівого наднирника, тромбектомії з ниркової вени та НПВ за екстреними показаннями за умови своєчасної діагностики та наявності мультидисциплінарної команди. Це симультанне оперативне втручання можна розглядати як операцію вибору при ТЕЛА у пацієнтів з пухлинами наднирників та тромбозом НПВ.
Інформація щодо конфлікту інтересів
Автори заявляють про відсутність конфлікту інтересів.
Усі етичні положення локальної етичної комісії та Гельсінської декларації 1975 р. Всесвітньої медичної асоціації (World Medical Association — ВМА) «Етичні принципи медичних досліджень за участю людини у якості об’єкта дослідження» (перегляд 2008 р.) були дотримані.
Фінансування. Стаття є фрагментом планової науково-дослідної роботи відділу хірургії поєднаної патології та захворювань заочеревинного простору ННЦХТ ім. О.О. Шалімова НАМН України, зовнішні джерела фінансування не залучали.
список використаної Літератури
1. Ng, L., & Libertino, J. M. (2003). Adrenocortical carcinoma: diagnosis, evaluation and treatment. Journal of Urology, 169, 5–11. doi.org/10.1097/01.ju.0000030148.59051.35.
2. Kassem, H., Moral, S., Morales, M., Ballesteros, E., & Brugada, R. (2019). Massive Migration of an Adrenocortical Carcinoma Thrombus. Circulation: Cardiovascular Imaging, 12(5). doi: 10.1016/j.ajodo.2024.05.015.
3. Ayati, M., Shahbazi, J., Tehranchi, A., Ayati, E., & Rezaei, Y. (2015). Adrenocortical Carcinoma With Renal Vein Thrombus Extended to Inferior Vena Cava: A Case Report. International Surgery, 100(7–8), 1190–1193. doi.org/10.9738/INTSURG-D-14-00224.1.
4. Shekhar, S., Gubbi, S., Papadakis, G., Nilubol, N., & Hannah-Shmouni, F. (2019). Adrenocortical carcinoma and pulmonary embolism from tumoral extension. Endocrinology, Diabetes & Metabolism Case Reports, 19-0095. doi: 10.1530/EDM-19-0095.
5. Lu, J., Ordinario, M., Rojo, R., Panjaitan, F., Pua, M., Lim-Uy, S., … Luis, T. (2019). MON-344 A Large Adrenal Mass with Neuroendocrine Features Presenting as Pulmonary Embolism: A Case Report. Journal of the Endocrine Society, 3. doi.org/10.1210/JS.2019-MON-344.
6. Yunoki, K., Wada, T., Miyawaki, I., Yamazaki, K., & Mima, H. (2017). Anesthetic management of one-stage scheduled surgery for adrenal cortical carcinoma complicated by massive pulmonary tumor embolism. JA Clinical Reports, 3(1), 48. doi: 10.1186/s40981-017-0115-4.
7. Aung, S., Parente, P., & Mckendrick, J. (2014). Pulmonary Embolism as an Initial Presentation of Adrenocortical Carcinoma. World Journal of Oncology, 5, 149–152. doi.org/10.14740/wjon814w.
8. Barone, G., Soracco, C., & Tribble, C. (1989). Intracaval Adrenocortical Carcinoma: A Case Report and a Review of the Operative Strategies. Vascular and Endovascular Surgery, 23, 214–221. doi.org/10.1177/153857448902300309.
9. Soscia, J., & Bonanno, C. (1963). The Budd-Chiari syndrome. American Journal of Digestive Diseases, 8(11), 929–936.
10. Castleman, B., Scully, R. E., & McNeely, B. U. (1972). Case records of the Massachusetts General Hospital. Case 46–1972. New England Journal of Medicine, 287, 1033–1040. doi: 10.1056/NEJM197211162872008.
11. Erythropoulou-Kaltsidou, A., Alkagiet, S., & Tziomalos, K. (2020). New guidelines for the diagnosis and management of pulmonary embolism: Key changes. World Journal of Cardiology, 12(5), 161–166. doi: 10.4330/wjc.v12.i5.161.
12. Konstantinides, S., Meyer, G., Becattini, C., Bueno, H., Geersing, G. J., Harjola, V., … Pepke-Zaba, J. (2019). 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). European Heart Journal, 41(4), 543–603. doi: 10.1093/eurheartj/ehz405.
13. Jaff, M. R., McMurtry, M. S., Archer, S. L., Cushman, M., Goldenberg, N., Goldhaber, S. Z., … Zierler, B. K. (2011). Management of Massive and Submassive Pulmonary Embolism, Iliofemoral Deep Vein Thrombosis, and Chronic Thromboembolic Pulmonary Hypertension. Circulation, 123(16), 1788–1830. doi: 10.1161/CIR.0b013e318214914f.
14. Beckerman, Z., & Bolotin, G. (2017). Surgical Treatment of Acute Massive Pulmonary Embolism. Advances in Experimental Medicine and Biology, 906, 75–88. doi: 10.1007/5584_2016_107.
15. Meyer, G., Vicaut, E., Danays, T., Agnelli, G., Becattini, C., Beyer-Westendorf, J., … Konstantinides, S. V. (2014). Fibrinolysis for Patients with Intermediate-Risk Pulmonary Embolism. New England Journal of Medicine, 370(15), 1402–1411. doi: 10.1056/NEJMoa1302097.
16. Aung, S. (2014). Pulmonary Embolism as an Initial Presentation of Adrenocortical Carcinoma. World Journal of Oncology, 5(3), 149–152. doi: 10.14740/wjon814w.
17. Jain, K., Gopala Krishna, R., & Basu, S. (2017). Rare case of left adrenal cortical carcinoma with level 3 inferior vena cava thrombus via adrenal vein. African Journal of Urology, 23(3), 201–203.
18. Lu, J., Ordinario, M., Rojo, R., Panjaitan, F., Pua, M., Lim-Uy, S., … San Luis, T. (2019). MON-344 A Large Adrenal Mass with Neuroendocrine Features Presenting as Pulmonary Embolism: A Case Report. Journal of the Endocrine Society, 3(1), MON-344. doi: 10.1210/js.2019-MON-344.
Адреса для листування:
Скумс Анатолій
03680, м. Київ, вул. Героїв Севастополя, 30
Національний науковий центр хірургії та трансплантології ім. О.О. Шалімова
E-mail: skums@gmail.com
Correspondence:
Anatolii Skums
30 Heroiv Sevastopolia str., Kyiv, 03680
Shalimov National scientific center of surgery and transplantation
E-mail: anatolii.skums@gmail.com














Leave a comment