Біопсія «сторожових» лімфатичних вузлів при меланомі шкіри
Скорода Л.В., Ковальчук Э.Н., Паливец А.Ю., Сукач Г.Г., Солодянникова О.И., Коровин С.И., Кукушкина М.Н.
Резюме. На сьогоднішній день біопсія «сторожових» лімфатичних вузлів при меланомі шкіри є стандартною діагностичною процедурою. Факторами, які мають прогностичне значення для появи мікрометастазів в регіонарних лімфатичних вузлах, є товщина пухлини за Breslow, поява виразок у ній, рівень інвазії за Clark IV–V, вік хворого. Наявність або відсутність мікрометастазів в «сторожових» лімфатичних вузлах є достовірним прогностичним фактором для хворих з первинною меланомою шкіри. Питання про необхідність виконання регіонарної лімфодисекції за наявності мікрометастазів в «сторожових» лімфатичних вузлах поки залишається відкритим і вимагає подальшого дослідження.
Резюме. На сегодняшний день биопсия «сторожевых» лимфатических узлов при меланоме кожи является стандартной диагностической процедурой. Факторами, имеющими прогностическое значение для появления микрометастазов в регионарных лимфатических узлах, являются толщина опухоли по Breslow, ее изъязвление, уровень инвазии по Clark IV-V, возраст больного. Наличие или отсутствие метастазов в «сторожевых» лимфатических узлах является достоверным прогностическим фактором для больных с первичной меланомой кожи. Вопрос о необходимости выполнения регионарной лимфодиссекции при наличии микрометастазов в «сторожевых» лимфатических узлах пока остается открытым и требует дальнейшего исследования.
 История внедрения биопсии «сторожевых» лимфатических узлов в клиническую практику
История внедрения биопсии «сторожевых» лимфатических узлов в клиническую практику
Меланома кожи характеризуется ранним лимфогенным метастазированием: опухоли, расположенные на туловище, метастазируют в лимфатические узлы с частотой 67–87,7%, а меланомы других локализаций — с частотой 39–46% [1].
Начало хирургической дискуссии о целесообразности профилактического удаления клинически неизмененных регионарных лимфатических узлов при меланоме кожи было положено ещё в конце XIX века H. Snow [30]. Он считал, что раннее иссечение «инфицированных» лимфатических узлов будет предупреждать последующее распространение опухоли во внутренние органы и, таким образом, способствовать излечению пациентов. В связи с этим на протяжении десятилетий во многих онкологических клиниках проводилась так называемая профилактическая регионарная лимфодиссекция. Показанием к ее проведению была толщина меланомы кожи по Breslow от 1 до 4 мм, так как при толщине опухоли менее 1 мм выживаемость больных приближалась к 98%, а толщина более 4 мм ассоциировалась с преимущественным развитием отдаленных гематогенных метастазов.
Сторонники профилактической лимфодиссекции настаивали на ее прогностическом значении, так как от количества вовлеченных в опухолевый процесс лимфатических узлов зависит общая выживаемость больных, и ретроспективно демонстрировали повышение общей 5-летней выживаемости среди пациентов, подвергшихся профилактической лимфодиссекции по сравнению с отсроченной (терапевтической) лимфодиссекцией. Противники данного вмешательства отмечали, что в 80% случаев гистологи в удаленных тканях не находили метастазов опухоли, то есть объем операции превышал необходимый. Кроме того, регионарная лимфодиссекция сопровождается большим числом осложнений: лимфостазом, болью, парестезиями, косметическим дефектом [2].
В 1994 г. C. Slingluff и соавторы [29] опубликовали данные ретроспективного анализа хирургического лечения 4682 больных меланомой кожи, среди которых 911 пациентов подверглись профилактической лимфодиссекции. Только у 143 (16%) были выявлены метастазы в регионарных лимфатических узлах непосредственно после оперативного вмешательства, у 71 (7,8%) больного метастазы появились в отсроченный период.
Целесообразность профилактической лимфодиссекции обсуждалась на протяжении многих лет (табл. 1).
Таблица 1 Результаты исследований по профилактической лимфодиссекции
| Исследование | Дизайн | Результаты |
|---|---|---|
| Memorial Sloan-Kettering, 1975 | Ретроспективное | Преимущество для меланомы средней толщины |
| Duke University, 1983 | Ретроспективное | Преимущество для меланомы средней толщины |
| Sydney Melanoma Unit, 1985 | Ретроспективное | Преимущество для меланомы средней толщины |
| University of Pennsylvania, 1983 | Ретроспективное | Нет преимущества |
| Duke University, 1994 | Ретроспективное | Нет преимущества |
| Sydney Melanoma Unit, 1995 | Ретроспективное | Нет преимущества |
| World Health Organization, 1977 | Проспективное | Нет преимущества |
| Mayo clinic, 1986 | Проспективное | Нет преимущества |
| Intergroup melanoma, 1996 | Проспективное | Нет преимущества, кроме больных с меланомой 1–2 мм и моложе 60 лет |
| World Health Organization, 1977 | Проспективное | Нет преимущества |
В ряде исследований 70–80 годов было показано ее преимущество, однако эти исследования были ретроспективными и не учитывали ряд прогностических факторов. Следует отметить, что в двух исследованиях (Duke University, 1983 и Sydney Melanoma Unit, 1985) вначале было сообщено о преимуществе профилактической лимфодиссекции для меланомы средней толщины, однако через 10 лет эти данные были опровергнуты самими авторами [9].
В 90-х годах были опубликованы результаты четырех рандомизированных исследований по изучению влияния профилактической лимфодиссекции на общую выживаемость больных меланомой кожи. Ни одно из этих исследований не показало преимущества ее выполнения. Однако в одном из них (WHO-14) было продемонстрировано повышение общей выживаемости больных, подвергшихся профилактической лимфодиссекции, у которых были обнаружены метастазы в регионарных лимфоузлах, по сравнению с больными, которым была выполнена отсроченная (терапевтическая) регионарная лимфодиссекция после появления клинических признаков метастазирования. Эти данные свидетельствовали в поддержку концепции биопсии «сторожевых» лимфатических узлов как идеального метода стадирования меланомы кожи и гипотезы о потенциальном влиянии на общую выживаемость путем выполнения регионарной лимфодиссекции у больных с метастазами в «сторожевых» лимфатических узлах [7].
Впервые концепцию «сторожевых» лимфатических узлов выдвинул R.M. Cabanas [6] в 1977 г., который, изучив данные лимфангиографии и анатомические срезы удаленных регионарных лимфатических узлов у 100 больных раком полового члена, высказал предположение о существовании «лимфатического центра», в который в первую очередь осуществляется отток лимфы из определенных участков ткани.
Однако метод лимфангиографии, предложенный R.M. Cabanas, не получил широкого применения в практике, поскольку был дорогим, технически сложным и не всегда информативным. В 1977 г. E. Holmes и соавторы [16] сообщили об успешном применении предоперационной лимфосцинтиграфии для идентификации регионарных лимфоузлов у 32 больных меланомой кожи. Во время исследования на лимфосцинтиграммах отмечалось накопление изотопа в одном или нескольких лимфатических узлах, которые получили название «сторожевых». Было высказано предположение, что так как «сторожевой» лимфатический узел является первым регионарным лимфоузлом, получающим лимфу от первичной опухоли, то в него в первую очередь попадают опухолевые клетки при распространении по лимфатическим путям. Следовательно, биопсия «сторожевых» лимфатических узлов может быть использована для оценки поражения всего регионарного лимфоколлектора.
В 1990 г. D. Morton представил на Обществе хирургов-онкологов первые результаты клинического исследования, в котором для визуализации «сторожевых» лимфатических узлов использовался специальный лимфотропный краситель «Isosulfan blue due». Было установлено, что «сторожевые» лимфоузлы окрашиваются через 30–60 мин после введения препарата по периметру опухоли, что делало возможным использовать предложенный метод непосредственно перед операцией. В этом исследовании у 223 пациентов, больных меланомой кожи, было выявлено 194 «сторожевых» лимфатических узла. Все больные после биопсии «сторожевых» лимфатических узлов подверглись регионарной лимфодиссекции: у 40 (21%) пациентов были обнаружены метастазы опухоли, при этом у 38 — в «сторожевых» лимфатических узлах [25].
Следующим шагом явилось внедрение в практику портативного гамма-сканера для интраоперационного поиска «сторожевых» лимфатических узлов, который был описан J.C. Alex и D.N. Krag [4] в моделях на животных. Клиническое использование данного метода было представлено в 1994 г. R. Essner и соавторами на Обществе хирургов-онкологов. При этом предоперационная лимфосцинтиграфия осуществлялась при помощи стационарного гамма-томографа, а интраоперационный поиск «сторожевых» лимфатических узлов при помощи портативного гамма-сканера. Важным преимуществом метода явилась возможность определять расположение «сторожевых» лимфатических узлов непосредственно через кожу. Кроме того, стало возможным контролировать локализацию узла при разрезе тканей, а также удостовериться, что удален действительно «сторожевой» лимфатический узел по степени накопления в нем радиофармпрепарата (РФП), определяемого гамма-датчиком.
В настоящее время для идентификации «сторожевых» лимфатических узлов используют радиологический метод как самостоятельно, так и в сочетании с красителем. Использование красителя позволяет обнаруживать «сторожевые» лимфатические узлы в 82–87% случаев, а комбинированное использование красителя и радиоизотопа в 99% [24].
Критерии отбора для биопсии «сторожевых» лимфатических узлов
Большинство пациентов с первично-локализованной меланомой кожи являются кандидатами для биопсии «сторожевых» лимфатических узлов. Факторами, имеющими прогностическое значение для появления метастазов в «сторожевых» лимфатических узлах, являются: толщина опухоли по Breslow, ее изъязвление, уровень инвазии по Clark IV–V, возраст больного [11, 28].
В частности, при толщине меланомы от 1 до 2 мм метастазы в «сторожевых» лимфатических узлах выявляются в 12–19,7%, при толщине 2–4 мм — в 28–33,2% случаев, а при толщине более 4 мм — в 28–44% [26].
Следует отметить, что среди больных с меланомой кожи <1 мм метастазы определяют в 0,94–5,5% случаев. Прогностическими факторами для появления метастазов при «тонких» меланомах являются: толщина опухоли по Breslow >0,75 мм, ее изъязвление, уровень инвазии по Кларку IV–V, молодой возраст, митотический индекс >0, отсутствие опухоль-инфильтрирующих лимфоцитов, мужской пол и регрессия первичной опухоли [21]. При «тонких» меланомах частота выявления клинически определяемых метастазов выше частоты обнаружения метастазов в «сторожевых» лимфатических узлах. Так, при толщине опухоли <0,75 мм они составляют 2,3 и 0,94% соответственно, а при толщине от 0,75 мм до 1,00 мм — 8,6 и 5,5% [18].
Наряду с толщиной опухоли, возраст является важным прогностическим фактором для развития регионарных метастазов. Интересно, что увеличение возраста ассоциируется с худшим прогнозом в отношении общей выживаемости, и в то же время характеризуется снижением частоты поражения регионарных лимфатических узлов. У пациентов старше 50 лет частота поражения регионарных лимфатических узлов, в том числе «сторожевых», достоверно снижается по сравнению с пациентами молодого возраста. При этом увеличивается риск возникновения отдаленных метастазов [12].
Вопрос о возможности выполнения биопсии «сторожевых» лимфатических узлов у больных после предшествующего широкого иссечения опухоли до настоящего времени вызывает споры. Большинство онкологов рекомендуют выполнять лимфосцинтиграфию перед широким иссечением опухоли во избежание нарушения лимфатического оттока. D.L. Morton после ретроспективной оценки 47 пациентов, подвергшихся биопсии «сторожевых» лимфатических узлов после предшествующего широкого иссечения меланомы кожи, сделал вывод о возможном применении данного вмешательства, если края резекции не превышали 2 см и первичная опухоль не находилась в зоне «сомнительного» лимфооттока [22]. Другое ретроспективное исследование, включающее 142 пациента, показало, что предшествующее широкое иссечение опухоли не влияет на точность обнаружения «сторожевых» лимфатических узлов, если не выполнялась пластика перемещенным лоскутом [13].
Биопсия «сторожевых» лимфатических узлов при локализации меланомы на коже головы и шеи имеет ряд особенностей вследствие близкой расположенности первичной опухоли и регионарного лимфоколлектора, большого анатомического разнообразия путей лимфоотока и малого размера узлов. Среднее число «сторожевых» лимфатических узлов при этой локализации составляет 3,8. Половина «сторожевых» лимфатических узлов определяется вне зоны ближайшего лимфоколлектора, четверть — в «неклассических» местах, в том числе в паращитовидных узлах, которые могут быть «затенены» инъекцией радиоизотопа. Кроме того, только 7% узлов окрашивается красителем, при этом наличие остатка красителя в коже является серьезным косметическим дефектом, особенно на лице [17].
Техника выполнения биопсии «сторожевых» лимфатических узлов
Биопсия «сторожевых» лимфатических узлов при первично-локализованной меланоме кожи технически достаточно проста.
Накануне операции выполняется предоперационная лимфосцинтиграфия с использованием 99mTc, который вводится интрадермально вокруг опухоли, для идентификации регионарного лимфоколлектора и приблизительного местонахождения «сторожевых» лимфатических узлов внутри него. Коллоид изотопа фагоцитируется макрофагами внутри лимфатического узла. Это удерживает его в дренирующем узле и предотвращает его дальнейший пассаж по лимфатическим путям.
Лимфосцитиграфия проводится непосредственно после введения изотопа и через 2 часа. Динамическая лимфосцинтиграфия помогает отличить истинные «сторожевые» лимфатические узлы, в которые происходит непосредственный дренаж лимфы от первичной опухоли, от «несторожевых» лимфатических узлов, которые могут находиться рядом. Предоперационная лимфосцинтиграфия также позволяет обнаруживать эктопические лимфатические узлы, которые выявляют приблизительно в 5–10% случаев при локализации меланомы на коже конечностей, в 30–32% случаев при локализации на коже туловища и в 60% при меланоме кожи головы и шеи. Кроме того, лимфосцинтиграфия позволяет выявить больных, у которых отток лимфы происходит в 2 лимфоколлектора [34].
Выбор РФП является весьма важным. 99mTc-серный коллоид имеет размер частиц от 100 до 4000 нм, что обусловливает медленную миграцию от места введения и затрудняет выполнение динамической лимфосцинтиграфии. 99mTc-коллоид альбумин и 99mTc-человеческий сывороточный альбумин являются более предпочтительными, так как достигают «сторожевых» лимфатических узлов в течение 20 мин у 97% больных и сохраняются в них на протяжении 24 ч, не распространяясь далее. 99mTc-человеческий сывороточный альбумин быстрее распространяется от места инъекции и лучше определяется в путях лимфооттока, в то время как другие РФП дольше сохраняются в лимфоузлах и визуализируются в отсроченный период в большем количестве лимфоузлов, чем непосредственно после введения РФП [3].
Местонахождение «сторожевых» лимфатических узлов отмечается радиологом на коже пациента маркером. Следует отметить, что вследствие релаксации больного во время операции и его положения на операционном столе расположение «сторожевых» лимфатических узлов может не совсем точно совпадать с меткой на коже. Поэтому хирург должен уточнить локализацию узлов в операционной с помощью портативного гамма-сканера.
Непосредственно перед операцией пациенту интрадермально вокруг первичной опухоли вводится 1,0 мл красителя. Наиболее часто применяемыми являются Patent blue V и Isosulfan blue. Methylene blue считается менее эффективным и может вызывать некроз мягких тканей [33].
Во время операции в первую очередь широко иссекается меланома кожи, а затем выполняется биопсия «сторожевых» лимфатических узлов.
Оптимальным является использование красителя и радиоизотопа: датчик облегчает идентификацию окрашенных «сторожевых» лимфатических узлов и может идентифицировать «сторожевые» лимфатические узлы, которые не окрасились. Однако в настоящее время нет четкого представления об уровне радиоактивности в «сторожевых» и «несторожевых» лимфатических узлах. Некоторые исследователи считают, что уровень радиоактивности в «сторожевых» лимфатических узлах должен превышать уровень фона в 2 раза, другие полагают, что он должен превосходить его на 10%. K.M. McMasters с коллегами [19] представили обзор данных, полученных в ходе Sunbelt Melanoma Trial: удаление всех окрашенных лимфатических узлов и всех узлов с уровнем радиоактивности, превышающим 10%, ассоциировалось с 0,4% ложноположительных результатов.
В связи с тем, что только 1% от введенной дозы РФП достигает «сторожевых» лимфатических узлов, близкое расположение первичной опухоли и регионарного лимфоколлектора может препятствовать эффективному использованию гамма-сканера, даже если она предварительно иссечена. Это особенно актуально для меланомы в области головы и шеи, где первичная опухоль и лимфоузлы близко расположены. Поэтому достаточно часто бывает трудно определить истинный уровень радиоактивности лимфоузла до его удаления: ex vivo уровень радиоактивности может быть в 2–3 раза выше, чем in vivo [27].
После удаления «сторожевых» лимфатических узлов рана обязательно должна быть исследована еще раз гамма-датчиком.
Биопсия «сторожевых» лимфатических узлов характеризуется высокой чувствительностью и специфичностью. В ряде исследований чувствительность метода оценивают как 100%, а специфичность — 97%: только у 1–3% больных с гистологически негативными «сторожевыми» лимфатическими узлами развились метастазы в регионарных узлах в течение 2 лет.
Микрометастазы в «сторожевых» лимфатических узлах, по данным разных авторов, определяют в 15–26% случаев. Один «сторожевой» лимфатический узел находят у 59% больных, два — у 37%, три — у 3% [37]. Среднее количество «сторожевых» лимфатических узлов колеблется от 1,3 до 1,8 [9].
Биопсия «сторожевых» лимфатических узлов сопровождается небольшим числом осложнений: формирование серомы/гематомы (2,3–5,5%), инфицирование раны (1,1–4,6%), лимфостаз (0,6–0,7%), окрашивание мочи и длительный татуаж в месте введения красителя. Редко отмечается аллергическая реакция на краситель [38].
Сообщения о том, что биопсия «сторожевых» лимфатических узлов вызывает развитие транзитных метастазов, не были подтверждены. В 2006 г. были опубликованы данные проспективного рандомизированного исследования, которые доказали отсутствие влияния биопсии «сторожевых» лимфатических узлов на развитие транзитных метастазов. Среди 500 больных, которым проводили широкое иссечение опухоли, транзитные метастазы развились у 42 (8,4%) пациентов, а среди 769 больных, которым одновременно с иссечением опухоли кожи выполняли биопсию «сторожевых» лимфатических узлов, транзитные метастазы были зафиксированы у 54 (7,0%) человек [36].
Гистологическая интерпретация данных
Удаленные «сторожевые» лимфатические узлы, как правило, исследуют после фиксации. Использование свежезамороженных срезов сопровождается большим количеством ложноотрицательных результатов, к тому же часть материала может быть потеряна в процессе процедуры замораживания [32]. Лимфатические узлы могут рассекать через центральную часть («двустворчатый» метод) либо в виде параллельных срезов с интервалом в 2 мм (метод «ломтей хлеба») [8].
Гистопрепараты окрашиваются гематоксилином-эозином; в случае отрицательного результата проводится иммуногистохимическое исследование с использованием меланоцитарных маркеров (S-100, HMB-45, Melan A).
90% меланом сопровождаются положительным окрашиванием S-100, однако он также окрашивает нейроны, меланоциты и дендритные клетки. HMB-45 — более специфичен, но менее чувствителен (70%), чем S-100. Melan A используется с подтверждающей целью. Наивысшей чувствительностью и специфичностью обладает коктейль из антител, включающий S-100, HMB-45, Melan A и тирозиназу (PanMel+ (Biocare Medical, USA)), однако это дорогостоящая и технически более сложная методика [14].
Важность иммуногистохимического метода продемонстрирована в исследовании J.E. Gershenwald [15], в которое было включено 243 пациента с гистологически негативными «сторожевыми» лимфатическими узлами после рутинного окрашивания гематоксилином-эозином. У 27 (11%) из них в отсроченный период развились местные, транзитные, регионарные и отдаленные метастазы; у 10 (4,1%) развились метастазы в зоне предшествующей биопсии «сторожевых» лимфатических узлов. Пересмотр гистопрепаратов с использованием иммуногистохимического окрашивания S-100 и HMB-45 показал наличие в «сторожевых» лимфатических узлах этих больных скрытых микрометастазов.
Классификационные системы микрометастазов меланомы
Наличие метастазов в «сторожевых» лимфатических узлах является важным прогностическим фактором (табл. 2). В 2002 г. в классификацию меланомы кожи American Joint Committee on Cancer (AJCC) введено понятие регионарных микрометастазов (обозначаются буквой а) и макрометастазов (обозначаются буквой b). Макрометастазы — это клинически и/или радиологически определяемые метастазы в регионарных лимфатических узлах, подтвержденные гистологически после выполнения терапевтической лимфодиссекции (рис. 1). Микрометастазы — это клинически и радиологически неизмененные лимфатические узлы, подтвержденные гистологически после выполнения биопсии «сторожевых» лимфоузлов либо профилактической регионарной лимфодиссекции. Согласно классификации AJCC 2009 года наличие микрометастазов в лимфатических узлах может подтверждаться иммуногистохимическим методом [5]. В данной классификации микрометастаз в 1 «сторожевом» лимфатическом узле классифицируется как N1a, в 2 или 3 узлах — как N2а.
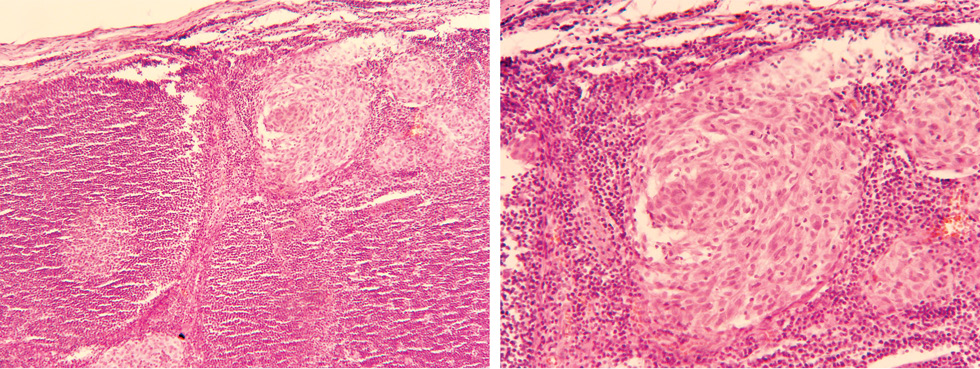
Таблица 2 Общая 5-летняя выживаемость больных меланомой кожи ІА–ІІІС стадии
| Стадия | TNM | 5-летняя выживаемость |
|---|---|---|
| ІА | T1aN0M0 | 97 |
| ІВ | T1bN0M0 | 88 |
| T2aN0M0 | ||
| ІІА | T2bN0M0 | 79 |
| T3aN0M0 | ||
| ІІВ | T3bN0M0 | 71 |
| T4aN0M0 | ||
| ІІС | T4bN0M0 | 53 |
| ІІІА | T1-4aN1aM0 | 78 |
| T1-4aN2aM0 | ||
| ІІІВ | T1-4bN1aM0 | 59 |
| T1-4bN2aM0 | ||
| T1-4aN2bM0 | ||
| T1-4aN2cM0 |
Однако вовлечение «сторожевых» лимфатических узлов в опухолевый процесс может быть разным: от наличия одной меланомной клетки до полного замещения лимфатического узла опухолью. В связи с этим для более точного прогнозирования предложено несколько классификационных систем.
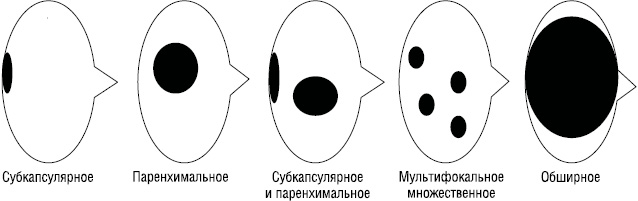
D.J. Dewar предложил классификацию в зависимости от микроанатомической локализации метастазов в «сторожевом» лимфатическом узле: cубкапсулярная, паренхимальная, комбинированная (cубкапсулярная и паренхимальная), мультифокальная множественная, обширное вовлечение лимфоузла диаметром >5 мм либо экстракапсулярное распространение опухоли (рис. 2). При субкапсулярной локализации микрометастазов меланомы не было выявлено ни одного случая поражения «несторожевых» лимфоузлов, что является благоприятным прогностическим фактором [10].
H. Starz [31] положил в основу так называемой S-классификации глубину инвазии опухолевых клеток в «сторожевом» лимфатическом узле, которая измеряется с помощью окулярного микрометра и определяется как расстояние между внутренним слоем капсулы лимфатического узла и клетками меланомы в его паренхиме. Предложено выделять III стадии: SІ<0,3 мм; SІІ 0,3–1 мм; SІІІ>1,0 мм. При стадиях SІ и SІІ прогрессия заболевания в течение 5 лет наступает у 15% больных, а при SІІІ — у 50%.
A.C. van Akkoi [35] предложил использовать максимальный размер самого крупного микрометастаза в «сторожевом» лимфатическом узле (Роттердамская классификация). Общая 5-летняя выживаемость пациентов с микрометастазами <0,1 мм составила 91%, с размерами от 0,1 мм до 1,0 мм — 61% и с диаметром >1,0 мм — 51% (p<0,001) .
A. Meier [20] использовал 1 основной критерий (максимальный размер самого крупного микрометастаза (<0,1; ≥0,1 мм)) и 2 дополнительных (глубину инвазии опухолевых клеток в паренхиме лимфатического узла (≤2 мм; >2 мм) и вовлечение капсулы лимфоузла (наличие или отсутствие)) для определения групп больных, имеющих благоприятный и неблагоприятный прогноз, так называемая Ганноверская балльная система (табл. 3).
Таблица 3 Ганноверская балльная система
| Группа | Основной критерий | Дополнительный критерий | Прогноз |
|---|---|---|---|
| 1-я | Максимальный размер микрометастаза <0,1 мм |
Прогноз, аналогичный для отрицательных СЛУ * | |
| 2-я | Максимальный размер микрометастаза >0,1 мм |
Максимум 1 дополнительный параметр | Средний прогноз |
| 3-я | Максимальный размер микрометастаза >0,1 мм |
Оба дополнительных параметра |
Неблагоприятный прогноз |
*СЛУ — «сторожевые» лимфатические узлы.
Многоцентровые исследования по биопсии «сторожевых» лимфатических узлов
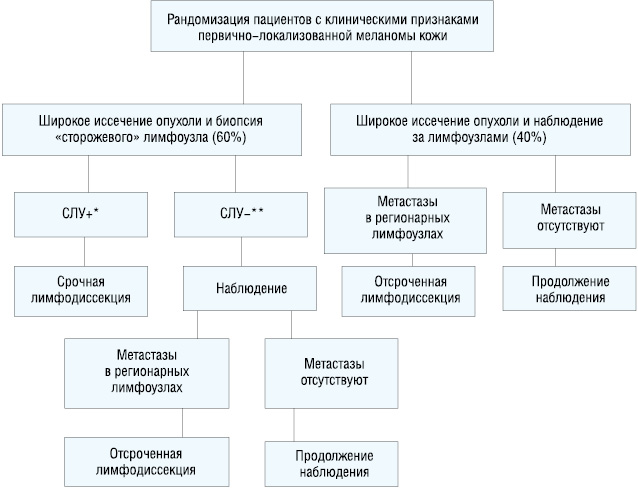
Первое многоцентровое исследование по биопсии «сторожевых» лимфатических узлов (Multicenter Selective Lymphadenectomy Trial, MSLT-I) проходило с 1994 по 2002 гг. В исследование включено 1269 пациентов с локализованной меланомой кожи, толщиной более 1,0 мм либо с уровнем инвазии по Кларку более IV. Больные рандомизированы в 2 группы в соотношении 2 : 3. Первой группе больных выполнялось широкое иссечение опухоли с биопсией «сторожевых» лимфатических узлов и последующей срочной регионарной лимфодиссекцией в случае обнаружения микрометастазов меланомы. Второй — широкое иссечение опухоли с последующим наблюдением за регионарными лимфатическими узлами и выполнением отсроченной регионарной лимфодиссекции в случае развития в них макрометастазов (рис. 3). В результате исследования установлено достоверное увеличение 5-летней безрецидивной выживаемости среди пациентов, перенесших биопсию «сторожевых» лимфатических узлов, по сравнению с больными, подвергшимся только широкому иссечению опухоли: она составила 78,3±1,6% и 73,1±2,1% соответственно (р=0,009). В то же время общая 5-летняя выживаемость оказалась одинаковой: 87,1±1,3% и 86,6±1,6% (р=0,58).
В группе больных, перенесших биопсию «сторожевых» лимфатических узлов наличие микрометастазов было важным прогностическим фактором: 5-летняя выживаемость больных с положительными «сторожевыми» лимфатическими узлами составила 72,3±4,6%, а с отрицательными — 90,2±1,3% (р<0,001). Микрометастазы в «сторожевых» лимфатических узлах были выявлены в 16% случаев. Макрометастазы в регионарных лимфоузлах в группе наблюдения в отсроченный период выявлены в 15,6% случаев. Среднее количество пораженных лимфоузлов при наличии микрометастазов составило 1,4, а при наличии макрометастазов — 3,3. Общая 5-летняя выживаемость больных, подвергшихся немедленной регионарной лимфодиссекции после выявления микрометастазов составила 72,3±4,6%; у пациентов, которым регионарная лимфодиссекция проводилась отсроченно после появления клинических признаков заболевания, она составила 52,4±5,9% (р=0,007) [23].
Несмотря на то что в результате исследования MSLT-I доказана важность выполнения биопсии «сторожевых» лимфатических узлов для прогноза и стадирования меланомы кожи, остается открытым вопрос о необходимости выполнения регионарной лимфодиссекции после обнаружения микрометастазов в «сторожевых» лимфатических узлах. На сегодняшний день в большинстве стран действующим стандартом лечения является полное удаление оставшихся лимфоузлов регионарного коллектора, в котором были обнаружены положительные «сторожевые» лимфатические узлы. Однако только в 10–15 % случаев в этих оставшихся лимфоузлах выявляются метастазы меланомы. Ряд исследователей полагает, что риск появления микрометастазов в «несторожевых» лимфатических узлах зависит от толщины первичной опухоли, размера микрометастаза, иммунного статуса «сторожевых» лимфатических узлов [11].
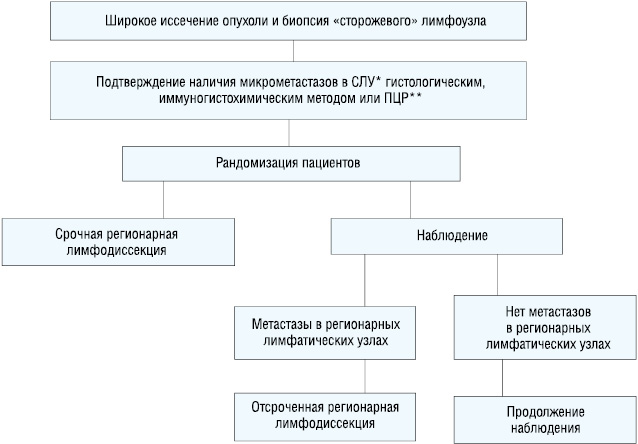
В 2004 г.стартовало второе многоцентровое исследование по биопсии «сторожевых» лимфатических узлов (Multicenter Selective Lymphadenectomy Trial, MSLT-ІI), в ходе которого происходит набор пациентов с микрометастазами меланомы кожи, выявленными гистологическим, иммуногистохимическим методами или полимерной цепной реакцией, которые рандомизируются в 2 группы. В 1-й группе пациенты подвергаются срочной лимфодиссекции. Во 2-й наблюдаются с использованием УЗИ регионарных лимфоколлекторов раз в 4 мес на протяжении первых 2 лет, а затем каждые 6 мес на протяжении последующих 3 лет. При подозрении на развитие метастаза в регионарных лимфоузлах выполняется биопсия, и в случае нахождения опухолевых клеток больному выполняется отсроченная регионарная лимфодиссекция (рис. 4). В данное исследование планируется включить 4200 пациентов до декабря 2017 г., когда будут опубликованы первые результаты исследования.
Таким образом, на сегодняшний день биопсия «сторожевых» лимфатических узлов при меланоме кожи является стандартной диагностической процедурой. Факторами, имеющими прогностическое значение для появления микрометастазов в регионарных лимфатических узлах, являются: толщина опухоли по Breslow, ее изъязвление, уровень инвазии по Clark IV–V, возраст больного. Наличие или отсутствие микрометастазов в «сторожевых» лимфатических узлах является достоверным прогностическим фактором для больных с первичной меланомой кожи. Доказанным и бесспорным фактом является влияние биопсии «сторожевых» лимфатических узлов на показатели безрецидивной выживаемости больных меланомой кожи. Вопрос о целесообразности выполнения регионарной лимфодиссекции при наличии микрометастазов в «сторожевых» лимфатических узлах пока остается открытым и требует дальнейшего изучения.
Литература
1. Пак Д.Д., Белова Е.А., Лазутина Т.Н. (2008) Исследование сторожевых лимфатических узлов у больных с меланомой кожи. Российский онкологический журнал, 4: 10–17.
2. Пак Д.Д., Лазутина Т.Н. (2008) Определение сторожевых лимфатических узлов при лечении больных меланомой кожи. Сибирский онкологический журнал,1 (25): 23–28.
3. Солодянникова О.І., Коровін С.І., Джужа Д.О. (2009) Дослідження стану сторожових лімфатичних вузлів в радіонуклідній діагностиці лімфометастазування меланом. Укр. радіологічний журнал, 3:
417–418.
4. Alex J.C., Krag D.N. (1993) Gamma-probe guided localization of lymph nodes . Surg. Oncol., 3 (2): 137–143.
5. Balch C.M., Gershenwald J.E., Soong S.J. et al. (2009) Final version of 2009 AJCC melanoma staging and classification. J. Clin. Oncol., 27: 6199–6206.
6. Cabanas R.M. (1977) An approach for the treatment of penile carcinoma. Cancer., 39: 456–465.
7. Cascinelli N., Morabito A., Santinami M. et al. (1998) Immediate or delayed dissection of regional nodes in patients with melanoma of the trunk: a randomised trial. WHO Melanoma Programme. Lancet., 351: 793–796.
8. Cook M.G., Palma S.D. (2008) Pathology of sentinel lymph nodes for melanoma. J. Clin. Pathol., 61: 897–902.
9. de Vita V.T., Lawrence T.S., Rosenberg S.A. (2011) Cancer: Principles and Practice of Oncology. 8th ed.Wolters Kluwer, Health., 3035 p.
10. Dewar D.J., Newell.B., Green M.A. et al. (2004) The Microanatomic Location of Metastatic Melanoma in Sentinel Lymph Nodes Predicts Nonsentinel Lymph Node Involvement. J. Clin. Oncol., 22: 3345–3349.
11. Ellis M.S., Weerasinghe R., Corless C. (2010) Sentinel lymph node staging of cutaneous melanoma: predictors and outcomes. Am. J. Surg., 5 (199): 663–668.
12. Faries M.B., Wright B.E., Wanek L. et al. Predictors of occult nodal metastasis in patients with thin melanoma. Arch Surg. In press.
13. Gannon C.J., Rousseau D.L., Ross M.I. et al. (2006) Accuracy of lymphatic mapping and sentinel lymph node biopsy after previous wide local excision in patients with primary melanoma. Cancer, 11(107): 2647–2652.
14. Garbe C., Eigentler T.K., Bauer J. et al. (2011) Histopathological diagnostics of malignant melanoma in accordance with the recent AJCC classification 2009: Review of the literature and recommendations for general practice. J. der Deut. Dermatol. Gesellschaft., 9: 690–
699.
15. Gershenwald J.E., Colome M.I., Lee J.E. (1998) Patterns of recurrence following a negative sentinel lymph node biopsy in 243 patients with stage I or II melanoma. J. Clin. Oncol., 16(6): 2253–2260.
16. Holmes E.C., Moseley H.S., Morton D.L. et al. (1977) A rational approach to the surgical management of melanoma. Ann. Surg., 186: 481–490.
17. Jansen L.E., Koops H.S., Nieweg O.E. et al. (2000) Sentinel node biopsy for melanoma in the head and neck region. Head Neck., 22: 27–33.
18. Karakousis G.C., Gimotty P.A., Botbyl J.D. et al. (2006) Predictors of regional nodal disease in patients with thin melanomas. Ann. Surg. Oncol., 4(13): 533–541.
19. McMasters K.M., Reintgen D.S., Ross M.I. et al. (2001) Sentinel lymph node biopsy for melanoma: how many radioactive nodes should be removed? Ann. Surg. Oncol., 8(3): 192–197.
20. Meier A., Satzger I., Völker B. et al. (2010) Comparison of classification systems in melanoma sentinel lymph nodes — an analysis of 697 patients from a single center. Cancer, 116(13): 3178–88.
21. Mitra A., Conwa C.,Walker C. (2010) Melanoma sentinel node biopsy and prediction models for relapse and overall survival. Brit. J. Cancer, 103: 1229–1236.
22. Morton D.L., Hoon D.S., Cochran A.J. et al. (2003) Lymphatic mapping and sentinel lymphadenectomy for early-stage melanoma: therapeutic utility and implications of nodal microanatomy and molecular staging for improving the accuracy of detection of nodal micrometastases. Ann Surg., 4(238): 538–549.
23. Morton D.L., Thompson J.F., Alistair J. (2006) Sentinel Node Biopsy or Nodal Observation in Melanoma. N. Engl. J. Med., 13(355): 1307–1317.
24. Morton D.L., Thompson J.F., Essner R.H. (1999) Validation of the accuracy of intraoperative lymphatic mapping and sentinel lymphadenectomy for early-stage melanoma: a multicenter trial. Multicenter Selective Lymphadenectomy Trial Group. Ann. Surg., 4 (230): 453–63.
25. Morton D.L., Wen D.R., Wong J.H. et al. (1992) Technical details of intraoperative lymphatic mapping for early stage melanoma. Arch. Surg., 127: 392–399
26. Ranieri J.M., Wagner J.D., Wenck S. et al. (2006) The prognostic importance of sentinel lymph node biopsy in thin melanoma. Ann Surg Oncol., 7(13): 927–932.
27. Rigel D.S., Robinson J.K., Ross M. et al. (2011) Cancer of the skin. 2nd ed. Elsevier, 698 p.
28. Rousseau D.L., Ross M.I., Johnson M.M. et al. (2003) Revised American Joint Committee on Cancer staging criteria accurately predict sentinel lymph node positivity in clinically node-negative melanoma patients. Ann. Surg. Oncol., 5(10): 569–574.
29. Slingluff L.J., Stidham K.R., Ricci W.M. et al. (1994) Surgical management of regional lymph nodes in patients with melanoma. Experience with 4682 patients. Ann. Surg. Oncol., 2(219): 120–130.
30. Snow H. (1892) Melanotic cancerous disease. Lancet., 2: 872.
31. Starz H., Siedlecki K., Balda B.R. et al. (2004) Sentinel lymphadenectomy and s-classification: a successful strategy for better prediction and improvement of outcome of melanoma. Ann. Surg. Oncol., 11 3 Suppl:162S–168S.
32. Stojadinovic A., Allen P.J., Clary B.M. et al. (2002) Value of Frozen-Section Analysis of Sentinel Lymph Nodes for Primary Cutaneous Malignant Melanoma. Ann. Surg., 235(1): 92–98.
33. Stradling B., Aranha G., Gabram S., et al. (2002) Adverse skin lesions after methylene blue injections for sentinel lymph node localization. Am. J. Surg., 184:
350–352.
34. Uren R.F., Thompson J.F., Howman-Giles R. et al. (2006) The role of lymphoscintigraphy in the detection of lymph node drainage in melanoma. Surgical Oncology Clinics of North America, 15: 285–300.
35. van Akkooi A.C., Nowecki Z.I., Voit C et al. (2008) Sentinel node tumor burden according to the Rotterdam criteria is the most important prognostic factor for survival in melanoma patients: a multicenter study in 388 patients with positive sentinel nodes. Ann. Surg., 248(6): 949–955.
36. van Poll D., Thompson J.F., Colman M.H. et al. (2005) A sentinel node biopsy does not increase the incidence of in-transit metastasis in patients with primary cutaneous melanoma. Ann. Sur.g Oncol., 12: 597–608.
37. Wong S.L., Kattan M.W., McMasters K.M et al. (2005) A nomogram that predicts the presence of sentinel node metastasis in melanoma with better discrimination than the American Joint Committee on Cancer staging system. Ann Surg Oncol., 12(4): 282–288.
38. Wrightson W.R., Wong S.L., EdwardsM.J. et al. (2003) Complications associated with sentinel lymph node biopsy for melanoma. Ann. Surg. Oncol., 10(6): 676–80.














Leave a comment