Збереження фертильності у пацієнтів з раком грудної залози
Сивак Л.А., Лялькін С.А., Мартинюк О.М., Досенко І.В., Верьовкіна Н.О., Тарасенко Т.Є., Смоланка І.І. (молодший)
Резюме. Сучасний комплексний підхід до лікування хворих на рак грудної залози (РГЗ) дає високі показники виживаності. Попри токсичну дію хіміопрепаратів на функцію яєчників, молоді жінки мають шанси збереження фертильності. У міжнародних онкологічних керівництвах представлено рекомендації щодо збереження функції яєчників у разі застосування хіміотерапії, і одним із доведених методів є прийом аналогів гонадотропін-рилізинг гормонів. Збереження функції яєчників дає можливість підвищення показників народжуваності серед пацієнток, що лікувалися з приводу РГЗ. Питання безпеки вагітності у пацієнток після РГЗ розкрито за результатами метааналізу 14 великих клінічних досліджень. Отже, збереження фертильності у пацієнток, що отримують хіміотерапію, дає шанс на материнство, що покращує не тільки якість життя, а й рівень соціальної адаптації жінки.Ключові слова: рак грудної залози; фертильність; гонадотропін-рилізинг гормон.
Одержано 20.11.2017
Прийнято до друку 18.01.2018
В останні роки досягнуто значного прогресу в лікуванні пацієнтів з онкологічними захворюваннями. Застосування на ранніх стадіях комбінованого та комплексного методів терапії забезпечує високі показники виживаності [1]. Особи молодого віку, особливо жінки, які фактично вилікувалися від раку, повноцінно живуть у суспільстві, і вже перед ними постає питання можливості збереження фертильності. Зростаючий інтерес до питань якості життя хворих, а також прогрес допоміжних репродуктивних технологій сприяли створенню нового напрямку в медицині, який і займається розв’язанням проблеми збереження фертильності у хворих онкологічного профілю. Онкофертильність — це медична дисципліна, яка вивчає можливість збереження репродуктивної функції у пацієнтів зі злоякісними пухлинами. Вперше термін був введений в 2006 р. Терезою К. Вудрафф (Teresa K. Woodruff; Feinberg School of Medicine Northwest University, США) як новий міждисциплінарний напрям, метою якого є консолідація зусиль онкологів і спеціалістів репродуктивної медицини у вивченні та розширенні можливостей збереження фертильності у пацієнтів онкологічного профілю [2]. Наука базується на двох основних принципах — безпеці й ефективності. Безпека полягає в збереженні репродуктивної функції, методи якого не впливають на лікування основного захворювання і не погіршують прогноз. Ефективність забезпечується використанням методів із доказовою клінічною результативністю [3].
Сучасний алгоритм прийняття рішення про можливість збереження репродуктивної функції у пацієнтів з онкологічними захворюваннями має найперше залежати від діагнозу злоякісного процесу та зацікавленості пацієнта.
Перспективне дослідження, ініційоване Dana-Farber Cancer Institut (США), оприлюднило результати опитування 200 пацієнток молодого віку з раком грудної залози (РГЗ), за якими понад 50% опитаних віком до 40 років цікавить можливість збереження фертильності з наступною вагітністю, що й спонукає науковців до активного пошуку шляхів розв’язання цієї проблеми [4].
Широкомасштабне норвезьке популяційне дослідження, у якому взяли участь 16 435 жінок та 11 845 чоловіків віком 16−25 років, які хворіли на рак, показало, що шанси відновлення фертильності у них на 40% нижчі порівняно із загальною популяцією. Водночас найнижчі шанси саме у молодих жінок із РГЗ [5]. Тому запобігання втраті фертильності наразі залишається актуальним в осіб молодого віку, які лікуються з приводу раку.
Поняття фертильності в онкології включає збереження функції яєчників для запобігання передчасній аменореї, яку найчастіше спричиняє лікування цитостатиками та променева терапія.
Більшість протипухлинних препаратів чинять свою цитотоксичну дію на проліферуючі клітини, які перебувають в мітотичному циклі. Зворотним процесом є цитотоксичне ураження тканин зі швидким поділом клітин (кістковий мозок, шлунково-кишковий тракт, тимус). Проте цитотоксичне ураження незворотне у яєчниках, де кількість ооцитів обмежена, і визначено ще внутрішньоутробно. Руйнування великої кількості фолікулів призводить до передчасного виснаження функції яєчників і навіть ранньої менопаузи. Ефект впливу хіміопрепаратів на функцію яєчників варіюється в широких межах, деякі з них не виявляють вираженого ефекту, а інші викликають постійний гіпогонадизм. Як правило, яєчники в жінок, які отримали хіміотерапію (ХТ), мають нормальне помірне зменшення кількості первинних фолікулів та інтенсивніше зменшення кількості дозріваючих фолікулів [6].
Ступінь впливу на функцію яєчників при проведенні поліхіміотерапії залежить від багатьох факторів: віку пацієнтки, протоколу лікування (виду програми поліхіміотерапії та дози хіміопрепаратів) і найбільшою мірою — базового оваріального резерву жінки [7].
За лікування з приводу онкологічної патології у жінок препубертатного віку яєчник зазнає найменшого ушкодження хіміотерапевтичними засобами. Водночас у жінок старшого віку, які мають менший оваріальний резерв, яєчники піддатливіші до набуття передчасної недостатності функції [8].
Зменшення оваріального резерву відбувається через апоптоз дозріваючих фолікулів і активацію залишкового фолікула з наступним апоптозом, що призводить до передчасного «вигорання» основного пулу. Фіброз стромальних кровоносних судин, який також є наслідком дії протипухлинних препаратів, збільшує пошкодження яєчників [9]. Клінічний прояв цієї фолікулярної втрати варіюється від повної аменореї до передчасної менопаузи і різного ступеня безпліддя.
Циклофосфамід є одним із найбільш широко застосовуваних препаратів у неоад’ювантній та ад’ювантній терапії РГЗ і має значний токсичний вплив на тканину яєчників. Механізм його дії, після активації в печінці, полягає в утворенні дволанцюгових розривів ДНК [10], пошкодження яких призводить до апоптозу. Активно проліферуючі клітини (гранульозу та стромальні) найбільш чутливі до цього препарату. Антрациклінові антибіотики, зокрема доксорубіцин, викликають «окиснювальний стрес», механізм їхньої дії в основному пов’язаний з пригніченням топоізомерази II. Аменорея і ризик зниження народжуваності є середніми з цією групою протипухлинних препаратів. Антиметаболіти, такі як метотрексат і 5-флуороурацил, чинять найменшу токсичну дію на яєчники, оскільки не завдають прямого пошкодження ДНК [10].
Схема і тривалість ХТ не є основними факторами, що спричиняють зниження або передчасне згасання функції яєчників. Обов’язково варто враховувати вік пацієнтки та комбінацію протипухлинних препаратів. Наприклад, лікування циклофосфамідом, метотрексатом і флуороурацилом упродовж 6 міс призводить до постійної оварільної недостатності у 85% жінок віком понад 40 років і лише у 30% молодих жінок. Середній термін до початку оваріальної недостатності у жінок літнього віку коротший, ніж у молодших (2–4 міс проти 6−16 міс), а оваріальна недостатність менш ймовірно буде зворотною у жінок літнього віку (близько 10% проти 50%). Частота постійної оваріальної недостатності нижча у разі застосування ХТ з режимами доксорубіцину і циклофосфаміду, ніж циклофосфаміду, метотрексату і флуороурацилу.
Клінічний випадок 1
Хвора О., 27 років. Діагноз: Ca glandulae mammae sinistrae Т4BN1AM0, стадія ІІІБ, 2-га клінічна група; патогістологічний висновок — інфільтруюча протокова карцинома; за даними імуногістохімічного дослідження Er (−), Pr (−), Her2new (3+) (рис. 1).
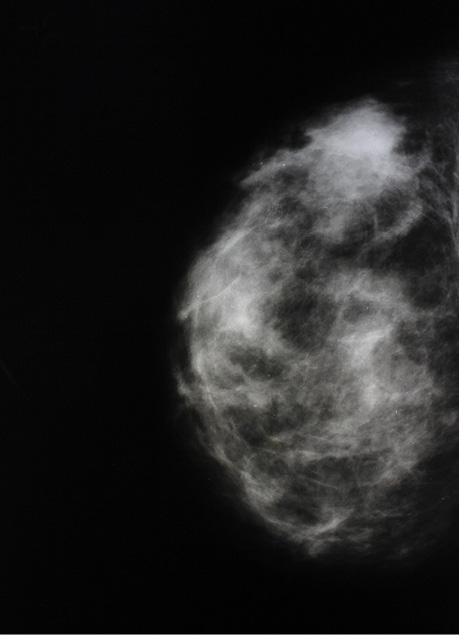
Лікування: отримала 6 курсів неоад’ювантної поліхіміотерапії (НАПХТ) за схемою FAC (5-флуороурацил, доксорубіцин, циклофосфамід); операція — квадрантектомія лівої грудної залози з регіонарною лімфодисекцією; 4 курси ад’ювантної поліхіміотерапії (АПХТ) за схемою ЕТ (епірубіцин, паклітаксел).
Аменорею відмічали після другого курсу НАПХТ і впродовж усієї НАПХТ. Менструальний цикл відновився в післяопераційний період. На другому курсі АПХТ розвинулася аменорея.
Через 6 міс після закінчення лікування — вагітність, перебіг — без ускладнень та рецидивів основного захворювання.
Клінічний випадок 2
Хвора Д., 38 років. Діагноз: Ca glandulae mammae sinistrae Т2N1M0, стадія ІІБ, 2-га клінічна група; патогістологічний висновок — інфільтративна карцинома; за даними імуногістохімічного дослідження — Er (−), Pr (−), Her2new (−) (рис. 2).
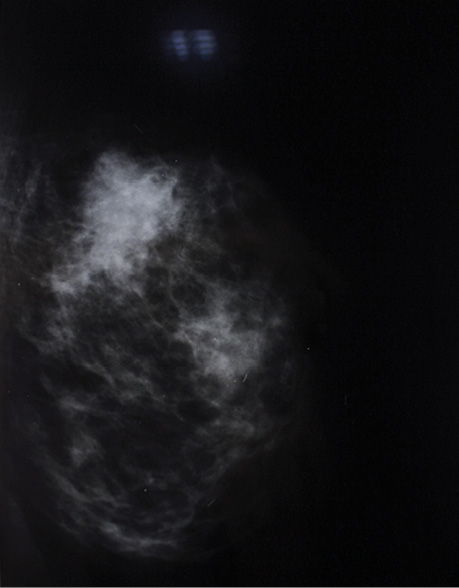
Лікування: отримала 4 курси НАПХТ за схемою FAC (5-флуороурацил, доксорубіцин, циклофосфамід); операція — мастектомія лівої грудної залози з регіонарною лімфодисекцією; 2 курси АПХТ за схемою АТ (доксорубіцин, паклітаксел).
Аменорея виникла після першого курсу НАПХТ і тривала впродовж усього періоду НАПХТ. Менструальний цикл в післяопераційний період не відновився. На момент контрольного огляду, через 9 міс спостереження після закінчення лікування, відмічалася стійка рання аменорея.
За наведеними клінічними випадками, молоді жінки віком до 35 років із застосуванням відповідних схем ХТ мають лише тимчасове зниження функції яєчників, тоді як у жінок після 38 років із використанням відповідних комбінацій виникає стійка оваріальна супресія, як наслідок — рання стійка аменорея.
Відповідно до рекомендацій сучасних міжнародних настанов, лікарі якомога раніше повинні обговорити потенційний негативний вплив цитостатичних препаратів на фертильність з усіма молодими пацієнтами, які схильні до ризику виникнення безпліддя і зацікавлені в тому, щоб після закінчення лікування раку мати дітей [11, 12]. Тому для запобігання передчасному згасанню функції яєчників варто обговорити з хворими всі можливі методи збереження фертильності.
Так, за даними літератури, фармакологічний захист яєчників за допомогою гонадотропін-рилізинг гормону (ГнРГ) під час ХТ є альтернативним варіантом збереження функції гонад з тією перевагою, що не відстрочує початок ХТ і є широкодоступним [13].
Аналоги ГнРГ мають такі протективні механізми функції яєчників:
1. Створення препубертатного, гіпогонадного стану: використання аналогів ГнРГ викликає першочергово стимуляцію секреції гіпофізарного лютеїнізуючого гормону і фолікулостимулюючого гормону. У подальшому відбувається зниження цих показників до препубертатного рівня. Цей механізм запобігає підвищенню рівня фолікулостимулюючого гормону і стримує нормальну фізіологічну втрату примордіальних фолікулів, основану на мобілізації клітин з наступною атрезією.
2. Внаслідок зниження рівня естрогенів — знижується кровопостачання тканини яєчників.
3. Безпосередній вплив на рецептори ГнРГ — напряму знижують гонадотоксичність ХТ [3].
На сьогодні активно вивчається вплив ХТ з використанням ГнРГ на фертильність пацієнтів із РГЗ. У двох великих рандомізованих дослідженнях (POEMS і PROMISE), які проводилися паралельно, оцінювали ефективність тимчасового пригнічення функції яєчників за допомогою ГнРГ під час ХТ у пацієнтів з РГЗ.
У дослідженні POEMS-SWOG S0230 брали участь тільки жінки з ендокринно-нечутливим РГЗ [12]. Усього було залучено в дослідження 257 пацієнток із РГЗ віком 18–49 років: 131 — отримували стандартні схеми ХТ, а 128 — ХТ з гозереліном (3,6 мг 1 раз на 7 днів до першого циклу ХТ, 1 раз у 4 тиж протягом всіх курсів ХТ). Функцію яєчників оцінювали за результатами аменореї, наступної вагітності та безрецидивної виживаності. У групі з гозереліном частота настання аменореї становила 8%, що є значно нижчим показником порівняно з групою пацієнток, які отримували лише ХТ (22%). У групі пацієнток, які лікувалися цитостатичними препаратами з використанням ГнРГ, вагітність настала у 22%, що значно вище, ніж у групі ХТ без гозереліну — 11%. Безрецидивна виживаність була вищою на 11% у групі з ГнРГ і становила відповідно 89 і 78%.
Аналогічне дослідження PROMISE, у якому більшість пацієнток мали гормональний рецептор-позитивний тип захворювання та отримували ад’ювантну ендокринну терапію протягом щонайменше 5 років після закінчення ХТ. Метою дослідження була оцінка ролі аналогів ГнРГ (трипторелін) як стратегії захисту функції яєчників під час ХТ. Медіана спостереження становила 7,3 року. Загалом було включено в дослідження 226 пацієнтів. Сукупна 5-річна оцінка частоти відновлення менструального циклу у групі ХТ з триптореліном становила 72,6% та у групі лише ХТ — 64,0%. У групі ХТ із ГнРГ настало 8 вагітностей, а в групі лише на ХТ — 3. У пацієнток молодого віку одночасне введення триптореліну та ХТ підвищує ймовірність тривалого підтримання функцій яєчників, без негативного впливу на прогноз виживаності. Більша кількість зареєстрованих вагітностей у групі ХT із застосуванням триптореліну порівняно з ХТ обґрунтовує та підтверджує позитивний результат збереження фертильності [13, 14].
На етапі завершення наразі дослідження OPTION, яке включає 227 пацієнток із РГЗ, рандомізованих на групи для отримання АПХТ чи НАПХТ; без ГнРГ та з одночасним введенням ГнРГ протягом усього періоду системної цитотоксичної терапії та контрольну групу.
Первинний аналіз повністю завершений з 202 пацієнтами (що становить 89% від кількості рандомізованих). Дослідження показало зниження відсотка настання передчасної аменореї на 16,2% (38,3% — у контрольній групі та до 22,1% — в експериментальній; р=0,015).
Захисний ефект гозереліну був також підтверджений вторинним аналізом, кінцевою метою якого було виявити передчасне згасання функції яєчників, спричинених ХТ. Аналіз було проведено за участю 131 пацієнтки. Зниження передчасного згасання функції яєчників внаслідок ХТ: в експериментальній групі цей показник зареєстровано на рівні 18,5%, у контрольній — 34,8%.
Захисний ефект був більш виражений у пацієнток віком до 40 років. У цій підгрупі рівень аменореї знизився з 24,4 до 10,0%, а рівень передчасного зниження функції яєчників при ХТ — з 20,0 до 2,6%, коли ГнРГ був доданий до ХТ [15–17].
Для контролю передчасного згасання функції яєчників введено показник антимюллерового гормону, що є індикатором кількості активних фолікулів в яєчниках, який може стати біомаркером гонадотоксичності в період протипухлинної терапії. Результат дослідження показує вірогідну тимчасову супресію яєчників під час ХТ зі збереженням їх функції [18].
На вагітність, яка настала після закінчення лікування з приводу РГЗ, маємо як позитивні, так і негативні погляди науковців, онкологів, акушерів-гінекологів, у яких у подальшому перебувають під динамічним спостереженням жінки. Питання безпеки вагітності у пацієнток після РГЗ було продемонстровано в метааналізі Хатема Азімова в 2012 р. із включенням 14 клінічних досліджень, у якому було вивчено 1244 випадки РГЗ в жінок, у яких настала вагітність після закінчення лікування. У ході аналізу доведено зниження рівня смертності на 41% порівняно з контрольною групою. У висновках Х. Азімов відзначив той факт, що хворі на РГЗ не повинні бути позбавлені можливості майбутньої вагітності [19].
Це підтверджує факт існування терміну «ефект здорової матері» (healthy mother effect), що вперше був введений R. Salani [20]. Жінок, які на моральному, фізіологічному та психологічному рівні досягли певного одужання після комбінованого лікування РГЗ і завагітніли, фактично можна вважати вилікуваними пацієнтками.
Висновки
Під час визначення подальшої тактики лікування пацієнток молодого віку з РГЗ варто також обговорити і можливі ризики впливу цитотоксичної терапії на тканину яєчників, що безпосередньо залежить від віку пацієнтки, режиму ХТ, дози препаратів, початкового оваріального резерву, та передбачити шляхи запобігання ранній стійкій аменореї.
Доведеним та безпечним методом захисту фертильної функції пацієнток є застосування в ході хіміотерапевтичного лікування аналогів ГнРГ, які є ефективними для запобігання ранній менопаузі. Ця стратегія може бути включена в клінічну практику. Проте потребують подальшого вивчення додаткові дослідження, пов’язані з функцією яєчників і народжуваністю.
Таким чином, мультидисциплінарний підхід до проблеми лікування молодих жінок з РГЗ із використанням методів збереження фертильності при проведенні ХТ дає шанс вилікуваним пацієнткам мати власних дітей, що покращує як якість життя, так і рівень соціальної адаптації жінки.
Список використаної літератури
1. Федоренко З.П., Михайлович Ю.Й., Гулак Л.О. та ін. (2017) Рак в Україні, 2015–2016. Захворюваність, смертність, показники діяльності онкологічної служби. Бюл. Нац. канцер-реєстру України, 18: 130 с.
2. Woodruff T., Zoloth L., Campo-Engelstein L., Rodriguez S. (Eds) (2010) Oncofertility: Ethical, Legal, Social, and Medical Perspectives. Springer, New York.
3. Боярський К.Ю., Гайдуков С.Н. (2013) Онкофертильність: можливість збереження репродуктивної функції у онкологічних хворих. Питання онкології, 59(5): 555–560.
4. Partridge A.H., Kathryn J.R., Kennedy J. et al. (2012) The Medical Birth Registry. Model Program to Improve Care for a Unique Cancer Population: Young Women With Breast Cancer. J. Oncol. Pract., 8(5): e105–e110.
5. Welt C.K., Shapiro Ch.L., Barbieri R.L. et al. (2017) Ovarian failure due to anticancer drugs and radiation (https://www.uptodate.com/contents/ ovarian-failure-due-to-anticancer-drugs-and-radiation).
6. Anderson R.A., Themmen A.P., Al-Qahtani A. et al. (2006) The effects of chemotherapy and long-term gonadotrophin suppression on the ovarian reserve in premenopausal women with breast cancer. Hum. Reprod., 21(10): 2583–2592.
7. Minton S.E., Munster P.N. (2002) Chemotherapy-induced amenorrhea and fertility in women undergoing adjuvant treatment for breast cancer. Cancer Control, 9: 466–472.
8. Roness H., Kalich-Philosoph L., Meirow D. et al. (2014) Prevention of chemotherapy-induced ovarian damage: possible roles for hormonal and non-hormonal attenuating agents. Hum. Reprod. Update, 20(5): 759–774.
9. Lambertini M., Del Mastro L., Pescio M.C. et al. (2016) Cancer and fertility preservation: international recommendations from an expert meeting. BMC Med., 14: 1.
10. Mahajan N. (2015) Fertility preservation in female cancer patients: An overview. J. Hum. Reprod. Sci., 8(1): 3–13.
11. Peccatori F.A., Azim H.A. Jr., Orecchia R. et al. (2013) Cancer, pregnancy and fertility: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann. Oncol., 24: 160–170.
12. Moore H.C., Unger J.M., Phillips K.A. et al. (2015) Goserelin for ovarian protection during breast-cancer adjuvant chemotherapy. N. Engl. J. Med., 372(10): 923–932.
13. Lambertini M., Ginsburg E.S., Partridge A.H. (2015) Update on fertility preservation in young women undergoing breast cancer and ovarian cancer therapy. Curr. Opin. Obstet. Gynecol., 27(1): 98–107.
14. Lambertini M., Boni L., Michelotti A. et al. (2014) Long-term outcome results of the phase III PROMISE-GIM6 study evaluating the role of LHRH analog (LHRHa) during chemotherapy as a strategy to reduce ovarian failure in early breast cancer patients. J. Clin. Oncol. (http://ascopubs.org/doi/abs/10.1200/jco.2014.32.26_suppl.105).
15. Biglia N., Peccatori F.A. (2015) Breast Cancer, Fertility Preservation and Reproduction. Springer, 102. ISBN: 978-3-319-17277-4.
16. Lambertini M., Poggio F., Levaggi A. et al. (2015) Protecting Ovaries During Chemotherapy Through Gonad Suppression: A Systematic Review and Meta-analysis. Obstet. Gynecol., 126 (4): 901.
17. Broer S.L., Broekmans F.J.M., Laven J.S.E., Fauser B.C.J.M. (2014) Anti-Mullerian hormone: ovarian reserve testing and its potential clinical implications. Hum. Reprod., 20(5): 688–701.
18. Leonard R.C.F., Adamson D.J.A., Bertelli G. et al. (2017) GnRH Agonist for Protection Against Ovarian Toxicity During Chemotherapy for Early Breast Cancer. Ann. Oncol., 28(8): 1811–1816.
19. Azim H.A., Santoro L., Russell-Edu W. et al. (2012) Prognosis of pregnancy-associated breast cancer: a meta-analysis of 30 studies. Cancer Treat. Rev., 38(7): 834–842.
20. Salani R., Billingsley C., Crafton S. (2014) Cancer and pregnancy: an overview for obstetricians and gynaecologist. Am. J. Obstet. Gynecol., 211: 7–14.
Сохранение фертильности у пациентов с раком грудной железы
Национальный институт рака, Киев
Резюме. Современный комплексный подход в лечении больных раком грудной железы (РГЖ) дает высокие показатели выживаемости. Несмотря на токсическое действие химиопрепаратов на функцию яичников, молодые женщины имеют шансы сохранения фертильности. В международных онкологических руководствах представлены рекомендации по сохранению функции яичников при применении химиотерапии, и одним из доказанных методов является прием аналогов гонадотропин-рилизинг гормонов. Сохранение функции яичников дает возможность повышения показателей рождаемости среди пациенток, лечившихся по поводу РГЖ. Вопрос безопасности беременности у пациенток после РГЖ раскрыт по результатам метаанализа 14 клинических исследований. Следовательно, сохранение фертильности у пациенток, получающих химиотерапию, дает шанс на материнство, что улучшает не только качество жизни, а и уровень социальной адаптации женщины.
рак грудной железы; фертильность; гонадотропин-рилизинг гормон.
Мартинюк Олена Михайлівна
03022, Київ, вул. Ломоносова, 33/43
Національний інститут раку
E-mail: olenamart81@gmail.com
Correspondence:
Martynyuk Olena
33/43 Lomonosova str., Kyiv 03022
National Cancer Institute
E-mail: olenamart81@gmail.com














Leave a comment