Променева діагностика екстранодальних лімфом
Резюме. Позитронно-емісійна томографія у поєднанні з комп’ютерною томографією і контрастна комп’ютерна томографія є стандартними методиками в діагностиці лімфом згідно з класифікацією Lugano (2014). Їхнє комплексне використання необхідно при первинній діагностиці лімфом та контрольних дослідженнях на етапах специфічного лікування. Магнітно-резонансна томографія є стандартним методом тільки для екстранодальної лімфоми з ураженням центральної нервової системи. У цій роботі визначено аспекти КТ-діагностики первинної екстранодальної лімфоми шлунка, уточнено особливості комп’ютерних зображень, що дозволяють запідозрити екстранодальну лімфому. Також розглянуто нюанси диференційної діагностики первинної екстранодальної лімфоми шлунка з іншими подібними злоякісними процесами.
Резюме. Позитронно-эмиссионная томография в сочетании с компьютерной томографией и контрастная компьютерная томография являются стандартными методиками в диагностике лимфом согласно классификации Lugano (2014). Их комплексное использование необходимо при первичной диагностике лимфом и контрольных исследованиях на этапах специфического лечения. Магнитно-резонансная томография является стандартным методом только для экстранодальной лимфомы с поражением центральной нервной системы. В данной работе определены аспекты КТ-диагностики первичной экстранодальной лимфомы желудка, уточнены особенности компьютерных изображений, позволяющих заподозрить экстранодальную лимфому. Также рассмотрены нюансы дифференциальной диагностики первичной экстранодальной лимфомы желудка с другими подобными злокачественными процессами.

Введение
Неходжкинская лимфома (НХЛ) является злокачественным заболеванием лимфатической системы, занимает 10-е место по распространенности и 11-е — в структуре смертности от злокачественных патологий в мире. По данным Всемирной организации здравоохранения, в 2012 г. в мире зарегистрирован 385 741 случай заболевания НХЛ, что составляет 2,7% [1] от общего количества заболевших. От НХЛ в мире в 2012 г. умерли 199 670 человек, а это 2,4% от общего количества умерших от онкологических заболеваний [2]. В Украине в 2015 г. зарегистрированы 2092 [3] заболевших НХЛ. Заболеваемость составляет 5,8 на 100 тыс. населения. Умерли от этой патологии 1048 человек, смертность — 2,9 на 100 тыс. населения. В первый год умирают 32,4% заболевших. Более 90% больных НХЛ — это люди среднего и преимущественно пожилого возраста. Детская заболеваемость НХЛ низкая, по разным источникам, от 1 до 10%. В 2015 г. в Украине заболели 60 детей в возрасте 0–17 лет, что составляет 0,9 случая на 100 тыс. населения и 2,9% [3] от общего количества заболевших.
25–40% НХЛ являются экстранодальными, то есть возникающими в органах и тканях, не относящихся к лимфатической системе и в норме содержащих лимфоидную ткань. Экстранодальная лимфома может поражать любой орган человека, но в основном локализуется в желудочно-кишечном тракте (ЖКТ) (30–40%) [4], коже (до 10%) и центральной нервной системе (2—4% первичных и 5–30% вторичных поражений).
Лимфомы ЖКТ — самые распространенные из экстранодальных лимфом, представляют 10–15% всех случаев НХЛ и 30–40% [5] всех случаев экстранодальных лимфом. При этом лимфомы желудка составляют 60–75% [6] всех лимфом ЖКТ и 1–5% всех случаев злокачественных заболеваний желудка [7]. Лимфома тонкого кишечника занимает 2-е место по распространенности, составляет 20–30% всех гастроинтестинальных лимфом [8]. Распространенность лимфомы толстого кишечника составляет 6–12%, при этом слепая кишка поражается с наибольшей частотой вследствие обилия лимфоидной ткани в этой области. Самая редко вовлекаемая часть — это прямая кишка, доля ее поражения составляет меньше 1% [9]. Первичная лимфома пищевода также является очень редким заболеванием, составляет до 1% от всех лимфом ЖКТ [10]. Чаще всего пищевод вовлекается вторично от нодальных форм лимфом средостения и шеи.
Лучевая диагностика экстранодальных, как и всех видов лимфом, по данным последней редакции классификации Lugano [11], представлена позитронно-эмиссионной томографией в сочетании с компьютерной томографией (ПЕТ-КТ), контрастной компьютерной томографией (КТ) с приоритетным использованием ПЕТ-КТ. ПЭТ-сканирование и контрастная КТ являются стандартными диагностическими тестами для лимфомы. Ядерно-магнитный резонанс — стандарт только для исследований поражения центральной нервной системы. Злокачественные клетки лимфомы метаболизируют сахар активнее, чем нормальные клетки. ПЭТ-сканирование — это технология получения изображений с помощью радиоактивной глюкозы, которая быстрее и в больших количествах накапливается в злокачественных клетках по сравнению с нормальными, в результате чего клетки лимфомы дают более выраженное накопление радионуклидов при сканировании. ПЭТ-КТ полезно использовать для уточнения степени распространения лимфомы в организме [12]. Также может быть использована для определения реакции злокачественного процесса на лечение [13]. К сожалению, ПЭТ-сканирование может давать ложноположительные результаты в случае воспалительного процесса в различных тканях организма [12], что снижает ее показатели информативности и специфичности. Поэтому лучевые методы диагностики необходимы и достоверны в высокой степени при повторном обследовании пациента на этапах специфического лечения лимфомы для определения характера и степени терапевтического ответа [14]. При первичной диагностике экстранодальных лимфом лучевые методы не имеют высоких показателей точности и достоверности вследствие невозможности визуальной дифференциальной диагностики лимфом с другими подобными злокачественными процессами [4]. В случае лимфом окончательный диагноз может быть установлен только на основании дополнительных морфологических исследований. Возможности ПЭТ-КТ для диагностики первичных экстранодальных лимфом ЖКТ недостаточно изучены, по чувствительности метод сравним с контрастным КТ-исследованием (81–86%) [15], по специфичности превышает показатели контрастной КТ.
Учитывая актуальность повышения точности лучевой диагностики, целью данного исследования были определение специфических особенностей диагностических изображений, полученных методом КТ при стандартных условиях, и систематизация критериев дифференциальной диагностики экстранодальных лимфом.
Объект и методы исследованияВ период 2012–2016 гг. в Национальном институте рака обследованы и получили лечение 89 пациентов (100%) с экстранодальной лимфомой (61 (68,5%) мужчина и 28 (31,5%) женщин). Распределение лимфомы по локализации в организме было следующим (табл. 1). Все случаи экстранодальной лимфомы гистологически подтверждены.
| Локализация | Количество больных | |
| n | % | |
| Пищевод | 4 | 4,6 |
| Желудок | 64 | 71,9 |
| Тонкий кишечник | 5 | 5,6 |
| Толстый кишечник | 9 | 10,1 |
| Репродуктивная система | 7 | 7,8 |
| Всего | 89 | 100 |
Классификацию первичных лимфом ЖКТ по анатомической распространенности проводят при помощи системы Lugano, принятой в 1993 г., дополненной и усовершенствованной в 2011 и 2014 г. (табл. 2).
| Стадии | Описание |
| I | Ограниченное поражение слизистой, подслизистой оболочки единичного органа ЖКТ |
| II (а) | Вовлечение регионарных лимфоузлов |
| II (b) | Отдаленное поражение лимфоузлов брюшной полости |
| III | Распространение опухоли через серозную оболочку с поражением прилежащих органов |
| IV | Диссеминация опухоли с вовлечением наддиафрагмальных лимфоузлов |
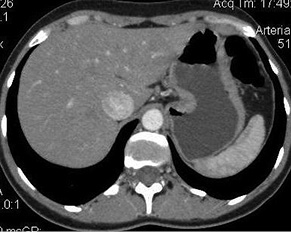
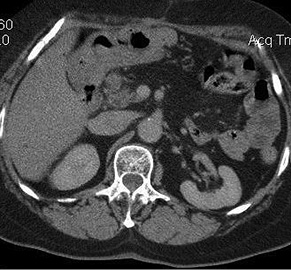
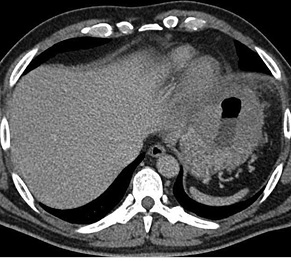
Стадия I по анатомической классификации экстранодальной лимфомы по Lugano определяет ограниченное единичное или множественное очаговое поражения слизистой и подслизистой оболочки ЖКТ в пределах одного органа (рис. 1). Стадия II характеризует распространение опухоли в брюшную полость (IIа — локальное поражение регионарных лимфатических узлов (рис. 2), IIb — отдаленное поражение узлов брюшной полости). Стадия III отмечает проникновение опухоли через серозную оболочку с вовлечением соседних органов или тканей (рис. 3). IV стадия характеризует массивную диссеминацию опухоли с вовлечением наддиафрагмальных узлов. Для статистического анализа традиционно используется Международная классификация TNM, согласно которой пациенты были распределены по степени распространенности злокачественного процесса (табл. 3).
| Т-стадия | Количество больных | |
| n | % | |
| T1 | 17 | 19,1 |
| T2a | 19 | 21,3 |
| T2b | 16 | 18,0 |
| T3 | 11 | 12,4 |
| T4 | 14 | 15,7 |
| Стадия не установлена | 12 | 13,5 |
| Всего | 89 | 100 |
Существуют диагностические критерии [16] отличия первичной экстранодальной лимфомы от вторичного поражения органов ЖКТ при нодальных формах лимфом. При первичной лимфоме ЖКТ:
- у обследуемого пациента нет пальпируемых поверхностных лимфатических узлов;
- нет гепатоспленомегалии;
- отсутствуют изменения в средостении (гиперплазия лимфоузлов или лимфопролиферативные процессы);
- данные цитологического исследования мазков периферической крови и костного мозга являются нормальными;
- преимущественное поражение солитарного органа ЖКТ.
По указанным критериям экстранодальные лимфомы разделены на первичные и вторичные. Первичная лимфома диагностирована в 67 (75,3%) случаях, вторичная — в 22 (24,7%). В данном исследовании проведен ретроспективный анализ диагностических изображений экстранодальных лимфом желудка у 64 человек, выполненных при помощи КТ в стандартных условиях с внутривенным контрастированием. Оценивали степень распространения злокачественного процесса в желудке и на прилежащие органы, структуру лимфопролиферативного процесса, толщину стенки, складчатость слизистой оболочки, состояние наружного контура и прилежащей клетчатки, наличие и размеры лимфоузлов брюшной и грудной полости.
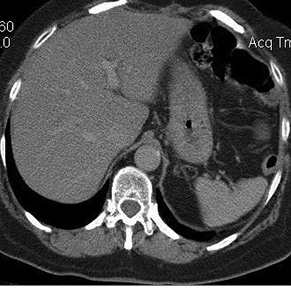
Результаты и их обсуждениеПо морфологической структуре 90% лимфом ЖКТ представляют собой два гистологических подтипа [10]. Это диффузная крупноклеточная В-клеточная лимфома (рис. 4) и MALT-лимфома маргинальной зоны (слизисто-ассоциированная лимфоидная опухоль — mucosa-associated lymphoid tissu), являющаяся лимфоидной диффузной инфильтрацией слизистой оболочки органов ЖКТ (см. рис. 1). В нашем исследовании у 74 (83,1%) пациентов выявлена лимфома В-клеточная и у 15 (16,9%) лиц диагностирована MALT-лимфома.
Контрастная КТ, как стандартная общедоступная методика, является базисной в первичной и контрольной диагностике лимфом. На КТ-изображениях при этом могут быть следующие изменения:
- солитарная или множественные опухолевые массы (рис. 5);
- милиарное узелковое поражение;
- лимфоматозная отграниченная инфильтрация (рис. 6);
- диффузная инфильтрация органа.
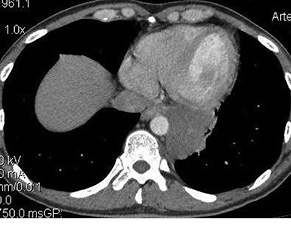
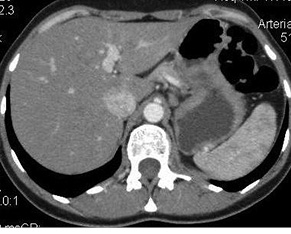
Наиболее характерным проявлением экстранодальной лимфомы в желудке является лимфоматозная отграниченная инфильтрация, выявленная в 45 (70,3%) случаях, диффузная инфильтрация отмечена у 12 (18,8%) больных. Солитарные или множественные опухолевые массы определяют чаще вторичные экстранодальные или поздние стадии первичных лимфом, их доля составила 10,9% (7 случаев).
КТ при первичной экстранодальной лимфоме в ЖКТ чаще всего выявляет следующие патологические изменения стенки:
- гиповаскулярное диффузное или локальное утолщение стенки (рис. 7);
- гиповаскулярные полиповидные узелковые изменения;
- гиповаскулярную опухолевую массу, единичную или множественные (рис. 8).
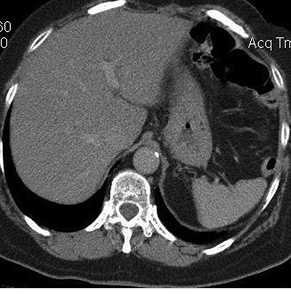
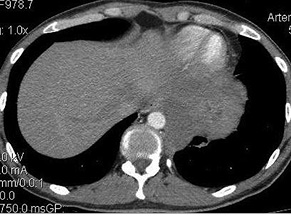
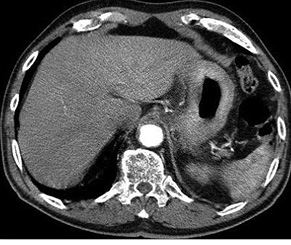
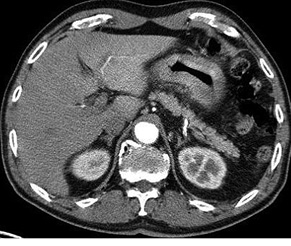
Для экстранодальных лимфом не характерна множественная локализация. Поражение единичного органа в случае экстранодальных лимфом ЖКТ и репродуктивной системы выявлено в 63 случаях (94% всех первичных лимфом). Дифференциальную диагностику экстранодальных лимфом ЖКТ проводят с инфильтративным, скиррозным раком и гастроинтестинальной стромальной опухолью (gastrointestinal stromal tumor — GIST), при локализации в тонком кишечнике также необходимо дифференцировать между болезнью Крона и карциноидной опухолью. Инфильтративный рак желудка (рис. 9, 10) характеризуется диффузным утолщением стенки во всех отделах, усиленной васкуляризацией патологического процесса, повышенной плотностью тканей и характерной для карциномы инфильтрацией окружающей клетчатки в виде нечеткого наружного контура опухоли.
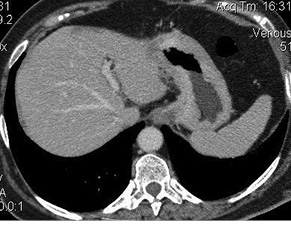
Диффузно-фиброзный рак (скирр) желудка (рис. 11) — редкая форма, составляющая 5% случаев всех карцином. По своей структуре больше всего подобен лимфоме, также уменьшена васкуляризация вследствие преобладания фиброзной ткани и не характерна наружная инфильтрация. В дифференциальной диагностике между лимфомой и скирром имеет значение анамнез заболевания. Рак желудка имеет более выраженные клинические проявления, такие как изматывающая ночная боль, резкое истощение, желудочные кровотечения и усиленные диспептические проявления, не характерные для лимфомы.
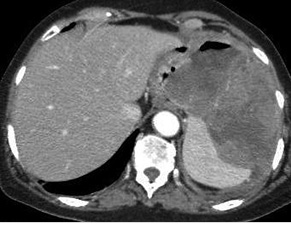
GIST составляют, по разным источникам, 0,1–3% всех злокачественных новообразований ЖКТ и принадлежат к наиболее частым мезенхимальным опухолям данной локализации. В желудке выявляют 55–59% [17] таких образований, в тонком кишечнике — 25–32%, в толстом кишечнике — 3–6%, в пищеводе — 0,7% (рис. 12, 13).
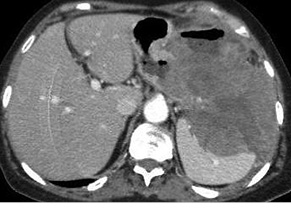
Характерные признаки, позволяющие дифференцировать лимфому от других злокачественных процессов:
- лимфома уменьшает плотность органа по сравнению с нормальной стенкой ЖКТ;
- опухолевая масса при лимфоме гиповаскулярна, что не характерно ни для одной из перечисленных групп;
- лимфома не вызывает сужения просвета полого органа, в некоторых случаях просвет, наоборот, расширяется. В случае GIST также очень редко бывает обструкция органа, но для карциномы сужение просвета часто является основным симптомом;
- лимфома не инфильтрирует прилежащую жировую клетчатку, что для инфильтративного рака желудка является характерным;
- регионарные лимфоузлы при экстранодальной лифоме поражаются реже, но в случае вовлечения имеют большие размеры;
- нелеченые лимфомы никогда не имеют кальцинатов.
В проведенном исследовании все изученные КТ-изображения экстранодальных лимфом соответствовали изложенным выше характеристикам.
Выводы
1. КТ является стандартным методом диагностики экстранодальных лимфом.
2. Лучевая диагностика экстранодальных лимфом основана на выявлении четких специфических особенностей злокачественного процесса, характерных для лимфом.
3. Применение критериев лучевой дифференциальной диагностики злокачественных процессов, возникающих в ЖКТ, повышает точность диагностики и улучшают показатели диагностической эффективности КТ.
Список использованной литературы
1. Bray F., Ren J.S., Masuyer E., Ferlay J. (2013) Estimates of global cancer prevalence for 27 sites in the adult population in 2008. Int. J. Cancer, 132(5): 1133–1145. doi: 10.1002/ijc.27711. Epub 2012 Jul 26.
2. Ferlay J., Soerjomataram I., Dikshit R. et al. (2014) Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int. J. Cancer. doi:10.1002/ijc.29210 PMID:25220842. Epub. 9 Oct. 2014.
3. Федоренко З.П., Михайлович Ю.В., Гулак Л.О. та ін. (2016) Рак в Україні, 2014–2015. Захворюваність, смертність, показники діяльності онкологічної служби. Гол. ред.: О.О. Колеснік. Бюл. Нац. канцер-реєстру України, Київ, № 17. 144 с.
4. Ghimire P., Wu G.-Y., Zhu L. (2011) Primary gastrointestinal lymphoma. World J. Gastroenterol., 17(6): 697–707.
5. Manzella A., Borba-Filho P. (2013) Abdominal Manifestations of Lymphoma: Spectrum of Imaging Features. ISRN Radiology, 2013, Article ID 483069, 11 p.
6. Psyrri A., Papageorgiou S., Economopoulos T. (2008) Primary Extranodal Lymphomas of Stomach: Clinical Presentation, Diagnostic Pitfalls and Management. Ann. Oncol., 19(12): 1992–1999.
7. Kwee T.C., Kwee R.M., Nievelstein R.A.J. (2008) Imaging in staging of malignant lymphoma: a systematic review. Blood, 111(2): 504–516.
8. Howell J., Auer-Grzesiak I., Urbanski S. (2010) Increasing Incidence of Primary Gastro-Intestinal Non-Hodgkin Lymphoma in North American population; population based study (submitted Am. J. Gastroenterol., Aug.).
9. Lee W.-K., Lau E.W.F., Duddalwar V.A. et al. (2008) Abdominal manifestations of extranodal lymphoma: spectrum of imaging findings. Am. J. Roentgenol., 191(1): 198–206.
10. Ghai S., Pattison J., Ghai S. et al. (2007) Primary gastrointestinal lymphoma: Spectrum of imaging findings with pathologic correlation. Radiographics, 27: 1371–1388.
11. Cheson B.D., Fisher R.I., Barrington S.F. et al. (2014) Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: The Lugano Classification. J. Clin. Oncol., Aug. 11. pii: JCO.2013.54.8800.
12. Barrington S.F., Mikhaeel N.G. (2014) When should FDG-PET be used in the modern management of lymphoma? Br. J. Haematol., 164(3): 315–328.
13. Cerci J.J., Trindade E., Pracchia L.F. et al. (2010) Cost effectiveness of positron emission tomography in patients with Hodgkin’s lymphoma in unconfirmed complete remission or partial remission after first-line therapy. J. Clin. Oncol., 28(8): 1415–1421.
14. Kostakoglu L., Cheson B.D. (2014) Current role of FDG PET/CT in lymphoma. Eur. J. Nucl. Med. Mol. Imaging., 41(5): 1004–1027.
15. Almuhaideb A., Papathanasiou N., Bomanji J. (2011) F-FDG PET/CT Imaging In Oncology. Ann. Saudi Med., 31(1): 3–13.
16. Колесник Е.А. (2003) Malignant lymphomas of the gastrointestinal tract. Онкологія, 5(1): 63–68.
17. Soreide K., Sandvik O.M., Soreide K. (2016) Global epidemyoligy of gastrotntistinal stromal tumour (GIST): A systematic review of population-based cohort studies. Cancer Epidemiol., 40: 39–46.
Адрес:
Чернобай Татьяна Николаевна
03022, Киев, ул. Ломоносова, 33/43
Национальный институт рака
E-mail: Chernobie17@gmail.com
Тел.: (044) 257-21-06














Leave a comment