Особливості променевої діагностики рідкісних захворювань грудної залози пухлинної природи
Головко Т.С., Скляр С.Ю., Крахмалева Л.П., Кротевич М.С., Процык В.С.
Резюме. Удосконалення методів діагностики раку грудної залози — актуальне питання клінічної онкології. Стаття присвячена підвищенню якості диференційної діагностики захворювань грудної залози. Ретроспективно проаналізовано архів обстежень пацієнток, що звернулися в Національний інститут раку з підозрою на рак грудної залози, яким проводили стандартні дослідження. Виділена група пацієнток з рідкісними захворюваннями грудної залози, проаналізовані особливості їх променевої діагностики. Фахівець, який проводить перше обстеження пацієнтки, з урахуванням усіх використаних діагностичних методів повинен розглядати кожне вузлове утворення як явище, що вимагає диференційної діагностики для виключення злоякісного процесу.
Резюме. Усовершенствование методов диагностики рака грудной железы — актуальнейший вопрос клинической онкологии. Статья посвящена повышению качества дифференциальной диагностики заболеваний грудной железы. Ретроспективно проанализирован архив обследований пациенток, обратившихся в Национальный институт рака с подозрением на рак грудной железы, которым проводили стандартные исследования. Выделена группа пациенток с редкими заболеваниями грудной железы, проанализированы особенности их лучевой диагностики. Специалист, производящий первое обследование пациентки, с учетом всех применяемых диагностических методов должен рассматривать каждое узловое образование как явление, требующее дифференциальной диагностики для исключения злокачественного процесса.

Введение
Неуклонный рост заболеваемости и смертности от рака грудной железы (РГЖ) в последние десятилетия поднимает вопросы совершенствования ранней диагностики этой патологии на одно из первых мест в клинической онкологии [1, 2]. На сегодня, несмотря на определенный технический прогресс в этой области [3, 4] и увеличение средней продолжительности жизни онкологических больных, смертность женщин от РГЖ в Украине постоянно увеличивается и приближается к 8000 случаев в год [5].
Единственным реальным путем повышения эффективности лечения этого заболевания, повышения качества жизни радикально пролеченных пациенток и снижения смертности в настоящее время является улучшение ранней диагностики.
Успешное решение задач, связанных с ранней диагностикой РГЖ, возможно лишь при условии повышения качества знаний в этой области. Цель исследования — улучшение дифференциальной диагностики заболеваний грудной железы.
Материалы и методы исследования
Мы ретроспективно проанализировали архив обследований пациенток в возрасте 10–85 лет, обратившихся в Национальный институт рака с подозрением на объемные образования грудной железы. Женщинам в возрасте младше 40 лет в качестве первичного обследования проводили ультразвуковое исследование (УЗИ) грудных желез линейным датчиком с частотой 10–5 МГ и 14–6 МГ, которое в случае необходимости дополнялось рентгенологическим/маммографией в двух стандартных проекциях. Женщинам в возрасте старше 40 лет проводили как рентгенологическое, так и УЗИ.
При неясных ситуациях выполняли дополнительные маммографические укладки и прицельные снимки с увеличением. УЗИ в В-режиме дополнялось цветным (ЦДК) и энергетическим (ЭДК) допплеровским картированием. В этих же случаях нами был применен новый метод визуальной пальпации — эластография [6, 7].
В процессе динамических обследований пациенток с новообразованиями грудной железы мы подтвердили, что соноэластографический модуль позволяет проводить оценку тканевой эластичности в режиме реального времени при помощи мягкого давления, осуществляемого стандартным ультразвуковым датчиком.
Всем больным с наличием локального уплотнения в грудной железе проводили пункционную биопсию. При отсутствии признаков пролиферации, определяемых цитологическим или (при трепан-биопсии) гистологическим методом, больных наблюдали в динамике и назначали патогенетическую терапию. Пациенты, у которых при исследовании была выявлена высокая степень пролиферации эпителия грудной железы, были прооперированы, а их диагноз верифицирован гистологически. Из всего количества обследованных была выделена группа пациенток с редкими (отмечаемыми <5%) заболеваниями грудной железы опухолевой природы, у которых были проанализированы особенности лучевой диагностики.
Результаты исследований
Группу наблюдения заболеваний грудной железы опухолевой природы, требующих дифференциальной диагностики, составили 44 пациентки, из которых у 16 выявлены опухолевые образования доброкачественной природы — листовидные опухоли, у 3 — пограничные листовидные опухоли с явлениями резко выраженной дисплазии окружающих тканей, у 9 — диагностирована саркома грудной железы, у 7 — лимфома, у 4 — опухолевыми образованиями оказались метастазы меланомы, у 1 — метастазы рака желудка в грудную железу. В 14 случаях мы отмечали РГЖ у мужчин.
Листовидная опухоль — истинное фиброэпителиальное новообразование, включающее эпителиальный и стромальный компоненты. В литературе насчитывают около 30 названий этой опухоли (гигантская фиброаденома, фибросаркома, филлоидная фиброаденома и др.). Диагностируют листовидную опухоль в любом возрасте, чаще до 40 лет. Заболевание составляет 5% среди всех опухолей грудной железы. Клинически образование представляет собой быстрорастущий узел, хорошо отграниченный от окружающих тканей, нередко имеющий дольчатое строение со щелевидными или кистозными полостями. Мы отмечали листовидные опухоли размерами 0,5–25 см.
На основании гистологического исследования выделяют 3 группы так называемой зрелости ткани листовидной опухоли. Для доброкачественной листовидной опухоли характерна четкость границ, выраженная капсула, минимальная эпителиальная атипия клеток стромы, отсутствие митозов, равномерное распределение желез и стромы, отсутствие инфильтрации окружающих тканей.
Для пограничной листовидной опухоли характерна нечеткость контуров, умеренная атипия стромы, наличие митозов до 10 в десяти полях зрения, определяется начальная инвазия в окружающую ткань. Отдельные участки опухоли можно расценивать как фибросаркому низкой степени злокачественности.
Для злокачественной листовидной опухоли характерна выраженная атипия стромальных клеток с обилием митозов (более 10 на десять полей зрения), наличие инфильтрации окружающих тканей, характерно преобладание стромы над железистой тканью, часто отмечают участки гетерогенных сарком инфильтративного роста.
Рентгенологически листовидная опухоль при небольших размерах неотличима от простой фиброаденомы, так как на ранних стадиях своего развития по своей гистоархитектонике близка к ней. При размерах более 3 см она отличается неоднородностью структуры, контуры остаются четкими, ровными, но полицикличными, что создает впечатление нескольких узлов, часто отмечают симптом гиперваскуляризации, возможно включение в структуру мелкой извести. При УЗИ сонографическая картина соответствует морфологическому субстрату и представляет собой участок гипоэхогенной неоднородной структуры, нередко с наличием полостей в виде анэхогенных зон.
Озлокачествление листовидной фиброаденомы рентгенологически может обусловить нечеткость контуров опухоли, патологическую перестройку окружающей ткани в виде появления тяжистости по периферии образования за счет обилия и извитости сосудов и злокачественной перестройки соединительной ткани. Сонографически в этих случаях определяется образование неоднородной гипоэхогенности с нечеткими контурами. Мы считаем, что появление признаков малигнизации лучше прослеживается при допплеросонографии, что может быть объяснимо за счет усиления кровотока.
Примером собственного опыта авторов может быть следующее наблюдение.
Пациентка С., 1981 г.р. обратилась с жалобами на наличие образования в левой грудной железе, которое в течение месяца увеличилось в 2 раза.
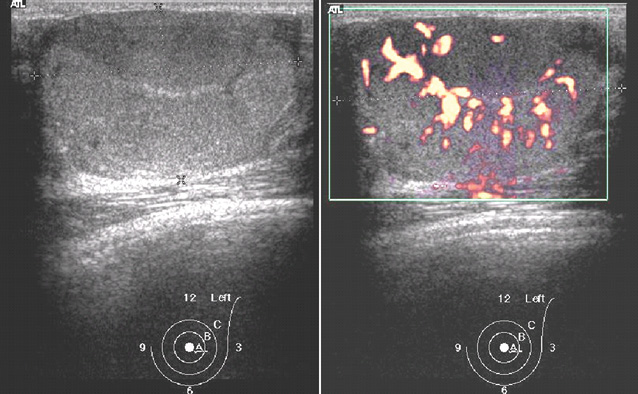
Клинически в левой грудной железе в верхне-наружном квадранте определялось округлой формы образование с гладкими контурами, средней степени плотности. При УЗИ лоцировалась солидная овальная опухоль с четкими ровными контурами, гомогенная с межузловым типом васкуляризации (рис. 1).
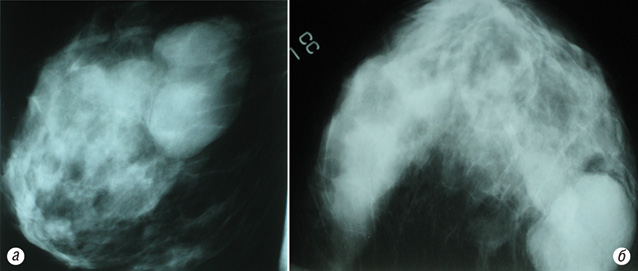
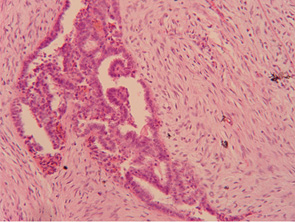
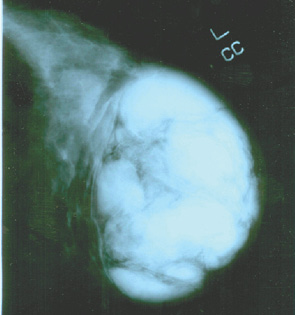
Рентгенологически (рис. 2а, б) в левой грудной железе определяли многоузловое интенсивное образование с ровными четкими контурами, однородное, размер до 3,5 см, при этом окружающие ткани не были изменены (рис. 3).
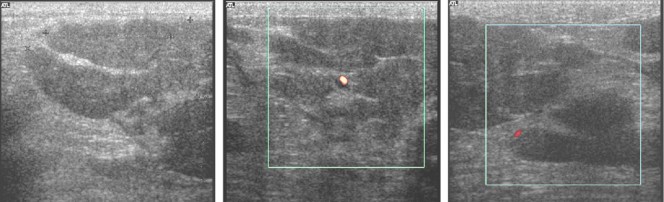
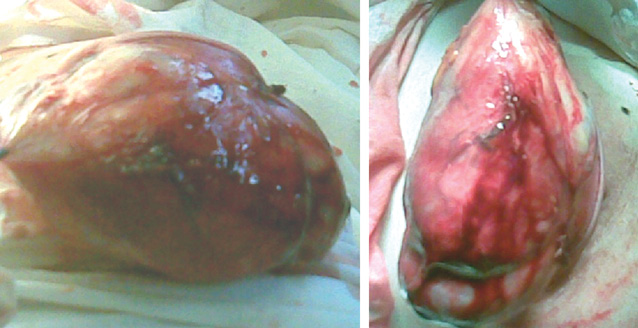
Характерным клиническим примером является также пациентка Р., 1992 г.р., которая обратилась в Национальный институт рака с жалобами на увеличение более чем в 2 раза правой грудной железы. Размеры железы увеличивались на протяжении 1,5 года. При УЗИ определяли гипоэхогенные узлы различной формы, достаточно однородные, анэхогенных зон распада и сосудистых сигналов лоцировано не было (рис. 4). При рентгенологическом исследовании (рис. 5) все поле зрения занимал опухолевый узел, размеры которого составляли >12 см (рис. 6, 7).
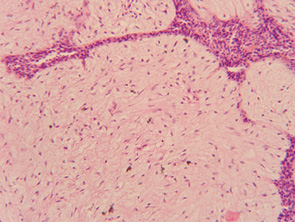
Диагноз листовидной опухоли грудной железы поставить только клинически не представляется возможным, утверждение «узнаем, когда разрежем» в данном случае недопустимо и может навредить пациенту. Для планирования адекватного противоопухолевого лечения необходимо проводить дифференциальную диагностику с фиброаденомой, саркомой и РГЖ.
Саркома — неэпителиальная злокачественная опухоль, которая составляет 0,6–4,0% всех случаев новообразований грудной железы. Морфологически различают липосаркому, ангиосаркому, фибросаркому, хондроостеоидную саркому, ретикулоклеточную саркому, стромальную саркому Берга и др. Клиническая картина при саркомах грудной железы зависит от ее гистологического строения. В целом эти опухоли характеризуются довольно медленным ростом. Период от первых признаков болезни до установления диагноза и оперативного лечения иногда составляет от 1 мес до 30 лет. В силу своего преимущественно экспансивного роста к моменту обнаружения опухолевые узлы достигают больших размеров (иногда >10 см). Клинически, как правило, в грудной железе определяют безболезненные опухоли с довольно четкими, местами бугристыми контурами. Для мезинхимальных сарком часто характерны признаки воспаления кожи над опухолью или окружающих тканей. Долгое время растущие саркомы грудных желез ведут себя как простые фиброаденомы или листовидные опухоли (не инфильтрируют и не фиксируют кожу, не изменяют сосок и ареолу), но при достижении больших размеров в 50% случаев отмечают спаянность опухолевого узла с кожей, а также расширение кожной венозной сети.
Характерной особенностью сарком является гематогенное метастазирование, лимфатические узлы, как правило, не поражаются: чаще всего отмечают местное рецидивирование, при прогрессировании поражаются легкие и кости. Прогноз заболевания зависит от распространения опухоли, степени ее дифференцировки. Рентгенологическая картина при саркомах довольно типичная: визуализируется образование округлой или овальной формы с довольно четкими, нередко бугристыми контурами, однородной структуры. Однако в зависимости от гистологического строения могут отмечать различные варианты. Так, при остеогенной саркоме могут выявлять участки оссификации или кистоподобные полости вокруг опухоли, при УЗИ нередко фиксируется симптом гиперваскуляризации. Дифференциальную диагностику необходимо проводить с листовидной опухолью, фиброаденомой и РГЖ.
Клиническим примером может быть следующий случай.
Пациентка Н.,1967 г.р., обратилась с жалобами на стремительное увеличение размеров и повышение плотности правой грудной железы. Клинически было выявлено значительное ассиметричное увеличение правой грудной железы, при пальпации на всем протяжении определялось диффузное уплотнение ткани железы, кожа была интактна. Увеличения лимфатических узлов в правой аксиллярной зоне отмечено не было.
На эхограмме визуализировалось солидное с четкими ровными контурами образование округлой формы, достаточно гомогенное, в режиме ЦДК определяли повышение васкуляризации образования и усиление кровотока вокруг него (рис. 8).
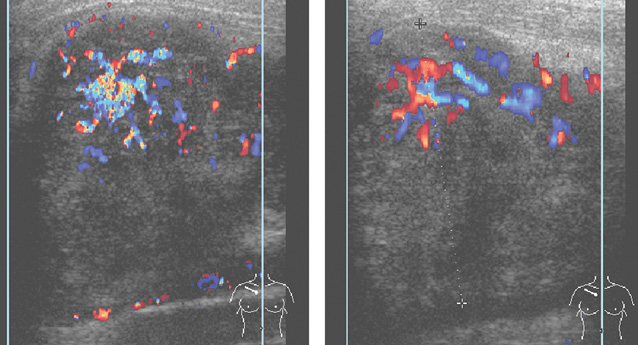
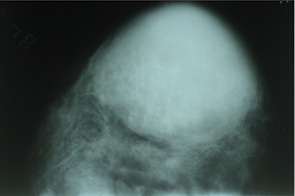
На маммограммах (рис. 9) — центрально под соском, занимая половину объема левой грудной железы, определяли округлое, однородное, интенсивное образование с четкими относительно ровными контурами, размерами до 8 см, было отмечено усиление фиброзного рисунка по периферии опухоли. Окружающие ткани компримированы.
Таким образом, комплексное клинико-рентгенологическое и УЗИ в В-режиме с ЦДК и ЭДК допплеровским картированием может предоставить достоверную информацию при выявлении саркомы грудной железы. Обязательным является дооперационное цитологическое или морфологическое исследование ткани опухоли.
РГЖ у мужчин — редкое заболевание, составляет 0,9–1,7% общего числа больных раком этой локализации, чаще отмечается у лиц старшей возрастной группы (после 60 лет). Для РГЖ у мужчин характерна односторонняя локализация. Клинически выявляют опухолевидное образование деревянистой плотности с четкими контурами, часто связанное с соском. Опухоль быстро прорастает в кожу и грудную стенку, рано метастазирует. Прогностически РГЖ у мужчин менее благоприятен чем у женщин. Показатели общей 5- и 10-летней выживаемости составляют по данным литературы 66 и 52% соответственно.
Рентгенкартина чаще неспецифическая, поскольку контуры опухоли ровные. Звездчатую форму отмечают лишь в 10% случаев, микрокальцинаты — в 30% случаев. Гистологические разновидности РГЖ у мужчин такие же, как у женщин. Для выявления опухоли целесообразно использование комплекса диагностических методов, включающего клинический, рентгенологический и сонографический. Обязательным является проведение пункционной или трепан-биопсии.
Дифференциальную диагностику следует проводить с липомами, атеромами, гранулемами, инородными телами и др.
Клиническим примером может быть следующий случай.
Пациент Р., 1954 г.р., обратился в поликлинику Национального института рака с жалобами на уплотнение в области левого соска. При клиническом осмотре было выявлено образование, распложенное под ареолой, округлой формы с бугристыми контурами, плотной консистенции, неподвижное по отношению к коже ареолы.
Эхографически в левой грудной железе определяли анэхогенное с четкими неровными контурами образование неоднородной структуры за счет плотных вегетаций внутри (рис. 10), в режиме ЦДК слабоваскуляризированное.

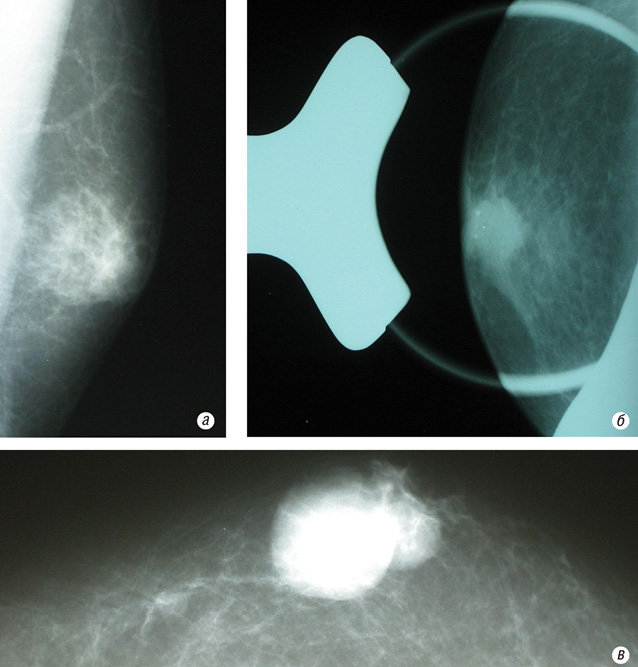
При обследовании на маммограммах (рис. 11а, б, в) в левой грудной железе, под соском определяли интенсивную неоднородную тень с нечеткими неровными контурами, отмечали симптом гиперваскуляризации. При проведении прицельных снимков с увеличением в прямой проекции выявлена группа точечных микрокальцинатов.
Клинико-рентгеносонографически был установлен диагноз РГЖ у мужчины, который был верифицирован цитологическим методом. Проведено противоопухолевое комбинированное радикальное лечение.
Лимфома — это злокачественная опухоль лимфоидной ткани, подобно солидным опухолям имеет первичный опухолевый очаг. Частота лимфом среди злокачественных образований грудной железы составляет 0,1–0,17%.
Для этого вида опухоли характерны не только регионарное метастазирование, но и диссеминация по всему организму одновременно с формированием состояния, напоминающего лимфоидные лейкозы. Лимфома является системным заболеванием и требует комплексного подхода к диагностике и лечению. Несмотря на многообразие клинических проявлений, для лимфом характерно быстрое прогрессирование болезни и неблагоприятный прогноз. В 40% случаев изменения в грудной железе сопровождаются признаками воспаления. У 50% больных с клиническими проявлениями болезни определяют пораженные аксиллярные лимфатические узлы (от единичных до конгломератов).
Рентгенологические признаки лимфом разнообразны в зависимости от локализации и распространения в грудной железе. Узловые образования чаще правильной округлой формы с ровными, а порой — с тяжистыми контурами, иногда имеют дольчатое строение с нечеткими очертаниями. В ряде случаев отмечают уплотнение ткани пораженной грудной железы с локализацией от одного квадранта до изменения всей железы. Степень злокачественности лимфом определяется при гистологическом и иммуногистохимическом исследовании опухоли.
Клиническим примером лимфомы грудной железы может быть следующий случай.
Пациентка П., 1973 г.р., обратилась с жалобами на ухудшение общего состояния здоровья: постоянная слабость, повышение температуры тела по вечерам до субфебрильных показателей. Одновременно с этим она отметила появление плотности в верхне-наружном квадранте правой грудной железы. При клиническом осмотре было выявлено асимметричное узловое образование в области верхне-наружного квадранта правой грудной железы, контуры его были бугристыми, консистенция неоднородная. Кожные покровы над опухолью не были изменены.
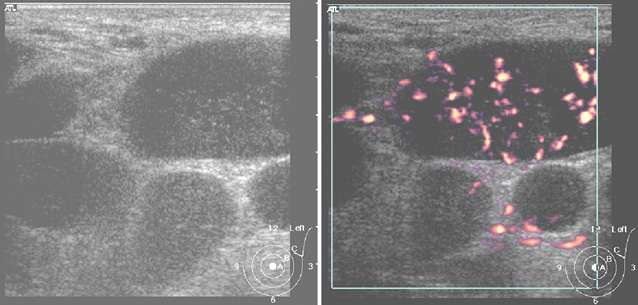
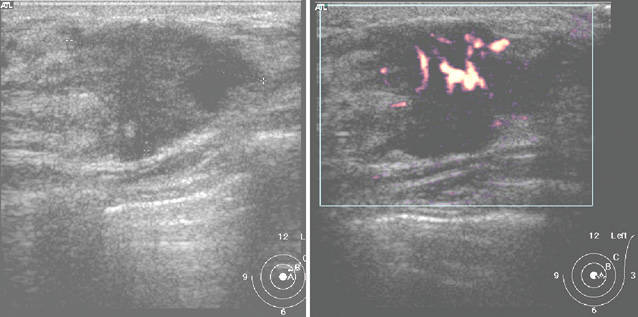
При УЗИ на эхограмме определяли гипоэхогенное образование с нечеткими ровными контурами (рис. 12). Характерным для него были округлые, гипоэхогенные контуры, при обследовании аксиллярной зоны на стороне поражения лоцировались сливающиеся в единые конгломераты пораженные лимфатические узлы (рис. 13). При УЗИ с использованием ЦДК — фиксирована умеренная васкуляризация очага поражения.
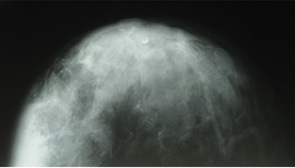
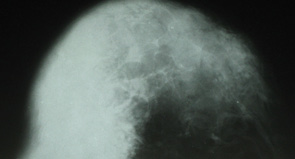
При рентгенологическом обследовании на маммограмме (рис. 14) определяли неоднородное интенсивное образование в верхне-наружном квадранте правой грудной железы. Контуры его были неровными и нечеткими. Размер составлял 3,5 см, был зафиксирован симптом гиперваскуляризации.
На протяжении 2,5 года после установления гистологического и иммуногистохимического диагноза пациентка получала комплексное лечение по поводу лимфомы правой грудной железы). Однако динамика была отрицательной — при контрольном рентгенологическом исследовании отмечали повышение интенсивности и увеличение в размерах до 5 см затемнения в правой грудной железе (рис. 15).
Редкость и разнообразие клинико-рентгеносонографических проявлений лимфом обусловливают трудности их дифференциальной диагностики, решить которые возможно только на основании комплекса методов с обязательным использованием иммуногистохимического диагноза.
Данные литературы свидетельствуют, что метастазы злокачественных новообразований в грудную железу отмечают крайне редко, чаще всего это происходит вследствие гематогенного распространения злокачественно трансформированной ткани яичников и меланомы. В большинстве случаев морфоструктура опухолевого образования, выявляемого в грудной железе, соответствует гистологической картине первичной опухоли.
При рентгенологическом обследовании, как правило, определяются единичные или множественные округлые образования с довольно четкими ровными контурами. Наличие косвенных симптомов — расширение диаметра сосудов, гиперваскуляризация, усиление структуры ткани вокруг образования — в большинстве случаев отсутствуют.
Клиническим примером метастатического поражения грудной железы может быть следующий случай.
Пациентка М., 1975 г.р., обратилась с жалобами на наличие множественных уплотнений в обеих грудных железах, проявившихся на протяжении последних 2–3 мес. При клиническом осмотре определяли наличие в обеих грудных железах множественных округлых образований, деревянистой плотности с четкими ровными контурами. При клиническом осмотре из анамнеза выяснено, что полгода назад пациентке была удалена злокачественная меланома кожи волосистой части головы.
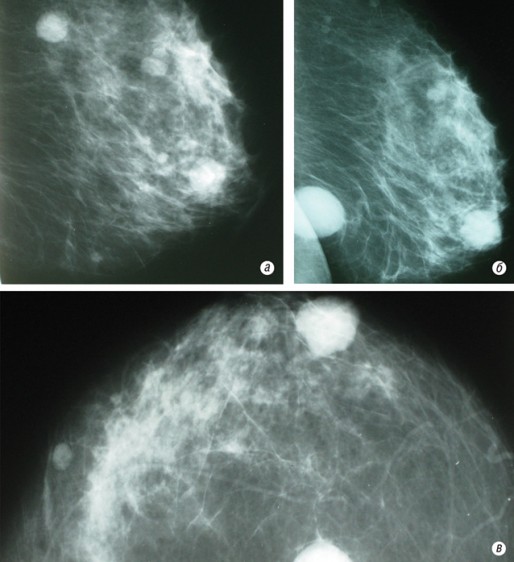
При рентгенологическом обследовании (см. рис. 16а, б, в) в обеих грудных железах определяли однородные диффузно-множественные округлые образования с четкими ровными контурами, размерами 0,5–2,0 см в диаметре.
Выводы
Усовершенствование методов лучевой диагностики РГЖ — актуальнейший вопрос современной клинической онкологии. Повышение качества дифференциальной диагностики заболеваний грудной железы позволяет выявить заболевание на ранних стадиях, что делает возможным как повышение эффективности противоопухолевого лечения, так и улучшение качества последующей жизни радикально леченных пациентов.
Специалист, производящий первое обследование пациентки, с учетом всех применяемых диагностических методов должен рассматривать каждое узловое образование как явление, требующее дифференциальной диагностики для исключения злокачественного процесса.
С учетом постоянного роста заболеваемости женского населения злокачественными новообразованиями грудной железы вполне обоснованным является требование онкологической настороженности и повышения качества знаний у специалистов в данной области.
Диагностические мероприятия, проводимые в комплексе (с применением современных методов исследования, с учетом данных соноэластографии и изучения васкуляризации патологических процессов в грудной железе) значительно повышают точность дифференциальной диагностики и до минимума исключают процент диагностических ошибок.
Литература
- 1. Труфанов Г.Е. (2009) Руководство по лучевой диагностике заболеваний молочных желез. 157–192.
- 2. Харченко В.П., Рожкова Н.И. (2009) Маммология. Национальное руководство. М.: ГЭОТАР-Медиа: 126–179.
- 3. Фисенко Е.П. (2009) Изменения кровотока как критерий диагностики рака молочной железы. Е.П. Фисенко. Ангиология и сосудистая хирургия., 15(1): 33–38.
- 4. Аллахвердян Г.С., Чекалова М.А. (2011) Возможности ультразвукового исследования в диагностике патологии поверхностных лимфатических узлов. Г.С. Аллахвердян, М.А. Чекалова. Ультразвуковая и функциональная диагностика, 1: 77–84.
- 5. Федоренко З.П., Гайсенко А.В., Гулак Л.О. (2009) Рак в Україні. Бюл. Національного канцер-реєстру, 10: 70.
- 6. Доценко Н.Я., Доценко С.Я., Боев С.С. и др. (2011) Сонография в исследовании упруго-эластических свойств кровеносных сосудов. Сучасні медичні технології, 1: 94–97.
- 7. Постнова Н.А., Васильев А.Ю., Зыкин Б.И. и др. (2011) Возможности эластографии сдвиговой волны в дифференциальной диагностике заболеваний молочной железы. Диагностическая и интервенционная радиология, 5(2): 324–325.














Leave a comment