Обинутузумаб в качестве первой линии терапии при хроническом лимфолейкозе: обновленные результаты исследования CLL11
Дайджест
Среди опухолей лимфатической системы хронический лимфолейкоз (ХЛЛ) составляет около 7% случаев. ХЛЛ — в основном болезнь людей пожилого возраста. Более 70% заболевают в возрасте старше 60 лет, средний возраст пациентов составляет 65–69 лет. У менее 10% заболевание возникает в возрасте до 40 лет. Ежегодная заболеваемость ХЛЛ составляет 3–3,5 на 100 тыс. жителей, увеличиваясь до 20 на 100 тыс. для лиц в возрасте старше 65 и до 50 на 100 тыс. — для возрастной категории старше 70 лет [1].
Выбор подходов к терапии пациентов с ХЛЛ зависит от ряда факторов: возраста пациента, распространенности опухолевого процесса, наличия и тяжести сопутствующей патологии, биологических характеристик опухоли и др. Применение современных таргетных препаратов для лечения ХЛЛ позволяет расширить возможности терапии пациентов пожилого возраста, а также существенно увеличить продолжительность их жизни.
Обинутузумаб — новое гликоинжиниринговое гуманизированное моноклональное антитело ІІ типа, которое связывается с CD20-рецептором. В доклинических исследованиях обинутузумаб показал более высокую противолейкемическую активность по сравнению с таковой у негликоинжиниринговых анти-CD20-антител — ритуксимаба и офатумумаба [2–4].
Обинутузумаб в сочетании с хлорамбуцилом показан для лечения взрослых пациентов с ХЛЛ, которые ранее не получали лечения и имеют сопутствующие заболевания, что делает невозможным проведение терапии на основе флударабина в полных дозах. Решение об одобрении препарата было основано на первичных результатах исследования CLL11 (NCT01010061), в ходе которого изучали применение обинутузумаба в сочетании с хлорамбуцилом, ритуксимаба в сочетании с хлорамбуцилом или монотерапии хлорамбуцилом у пациентов, которые ранее не получали лечения и имеют сопутствующие заболевания [5]. При анализе данных по состоянию на май 2013 г., схема терапии обинутузумаб + хлорамбуцил продемонстрировала превосходство над схемой ритуксимаб + хлорамбуцил в отношении выживаемости без прогрессирования заболевания (ВБП) и ответа на лечение. Добавление обинутузумаба к хлорамбуцилу привело к повышению общей выживаемости (ОВ) по сравнению с лечением только хлорамбуцилом, тогда как добавление ритуксимаба к хлорамбуцилу по сравнению с только хлорамбуцилом не привело к статистически достоверному увеличению ОВ. Также не отмечено значимых различий в ОВ между группой, получавшей обинутузумаб + хлорамбуцил, и пациентами, которым была назначена терапия комбинацией ритуксимаб + хлорамбуцил.
В 2015 г. опубликованы обновленные результаты данного исследования относительно ВБП и ОВ по итогам апреля 2014 г. [6]. Так, в исследовании приняли участие 781 пациент с ХЛЛ, которые ранее не получали лечения и нуждались в проведении терапии на фоне тяжелой коморбидной патологии. Все участники были включены в исследование в период с апреля 2010 г. по июль 2012 г. и рандомизированы на три группы: первая получала обинутузумаб + хлорамбуцил, вторая — ритуксимаб + хлорамбуцил, а третья — только хлорамбуцил. Диагноз ХЛЛ был установлен в соответствии с критериями Международной рабочей группы по хроническому лимфолейкозу (International Workshop on Chronic Lymphocytic Leukemia) [7]. Тяжесть коморбидной патологии оценивали по системе CIRS (Cumulative Illness Rating Scale) и путем расчета клиренса креатинина, используя формулу Кокрофта — Голта. Таким образом, в исследование были включены пациенты, соответствовавшие следующим критериям: CIRS >6 и/или клиренс креатинина 30–69 мл/мин [8, 9].
Обинутузумаб вводили в дозе 1000 мг в 1-й, 8-й и 15-й день 1-го цикла терапии и в 1-й день 2–6-го циклов терапии (продолжительность каждого цикла — 28 дней). Первое введение обинутузумаба было разделено на 2 дня. Ритуксимаб вводили в дозе 375 и 500 мг/м2 площади поверхности тела в 1-й день 1-го цикла и 2–6-го циклов соответственно. Хлорамбуцил в таблетках назначали в дозе 0,5 мг/кг массы тела в 1-й и 15-й день 1–6-го цикла. Для оценки эффективности терапии в качестве первичной конечной точки был выбран показатель ВБП. Вторичные конечные точки включали оценку ОВ и продолжительности времени до начала следующей линии терапии. Для анализа результатов и сравнения выживаемости были использованы методология Каплана — Мейера и двусторонний log-rank тест.
Группы пациентов были хорошо сбалансированы по демографическим показателям и характеристикам заболевания. Медиана возраста пациентов, включенных в исследования, составила 73 года. При этом наиболее распространенными коморбидными заболеваниями были заболевания почек, сердечно-сосудистой, дыхательной систем и опорно-двигательного аппарата, а также метаболизма (медиана CIRS составила 8, диапазон 0–22). Делеции 17p или 11q и немутировавший IGHV выявлены у 8% пациентов, получавших обинутузумаб + хлорамбуцил, 16% больных, применявших ритуксимаб + хлорамбуцил, и 61% пациентов, получавших только хлорамбуцил. Данный анализ не показал каких-либо ранее не проявлявшихся побочных реакций. На рис. 1–6 показаны обновленные данные ВБП и ОВ. Показатель ВБП значительно улучшился для группы, получавшей обинутузумаб + хлорамбуцил, по сравнению с группой, которой была назначена терапия по схеме ритуксимаб + хлорамбуцил. Так, медиана ВБП составила 29,2 мес по сравнению 15,4 мес соответственно (отношение рисков — ОР — 0,40; 95% доверительный интервал — ДИ — 0,33–0,50; p<0,001).
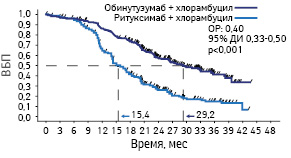
Адаптировано из: Goede V., Fischer K., Engelke A. et al., 2015 [6]

группы, получавшей обинутузумаб + хлорамбуцил, по сравнению с пациентами, получавшими ритуксимаб + хлорамбуцил
Адаптировано из: Goede V., Fischer K., Engelke A. et al., 2015 [6]
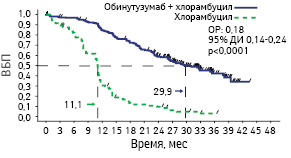
Адаптировано из: Goede V., Fischer K., Engelke A. et al., 2015 [6].
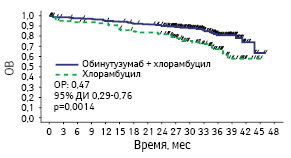
Адаптировано из: Goede V., Fischer K., Engelke A. et al., 2015 [6]
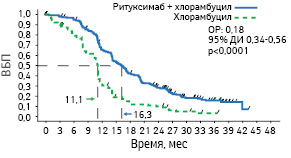
Адаптировано из: Goede V., Fischer K., Engelke A. et al., 2015 [6]
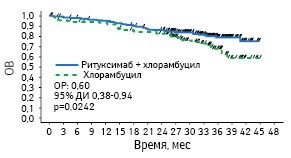
Адаптировано из: Goede V., Fischer K., Engelke A. et al., 2015 [6]
Период до следующей линии терапии также был больше на 10 мес у пациентов, получавших обинутузумаб + хлорамбуцил, по сравнению с теми, кому была назначена терапия ритуксимабом + хлорамбуцилом, — 42,7 против 32,7 мес соответственно (ОР 0,54; 95% ДИ 0,40–0,72; p<0,001). На данном этапе нет возможности продемонстрировать статистически достоверное преимущество показателя ОВ для пациентов, получавших обинутузумаб + хлорамбуцил, по сравнению с группой, которой назначали терапию ритуксимабом + хлорамбуцилом (ОР 0,70; 95% ДИ 0,47–1,02; р=0,0632). Такой результат связан с небольшим количеством умерших больных в группах, получавших обинутузумаб + хлорамбуцил и ритуксимаб + хлорамбуцил. Так, в группе из 333 пациентов, получавших обинутузумаб + хлорамбуцил, зафиксировано 45 летальных случаев, а в группе ритуксимаб + хлорамбуцил (330 больных) — 63. Тем не менее подтверждено ранее отмеченное улучшение ОВ для группы, получавшей обинутузумаб + хлорамбуцил, по сравнению с пациентами, которым была назначена монотерапия хлорамбуцилом (ОР 0,47; 95% ДИ 0,29–0,76; р= 0,0014). Среди пациентов, рандомизированных в тот же период, в группе, получавшей обинутузумаб + хлорамбуцил, зарегистрировано 37 случаев смерти среди 238 больных, а в группе, которой назначали хлорамбуцил, зафиксировано 34 летальных случая среди 118 пациентов. Таким образом, лечение комбинацией ритуксимаб + хлорамбуцил привело к повышению ОВ по сравнению с монотерапией хлорамбуцилом (ОР 0,60; 95% ДИ 0,38–0,94; р=0,0242). Среди пациентов, рандомизированных в тот же период, в группе применения ритуксимаба + хлорамбуцила зарегистрировано 44 эпизода смерти среди 233 пациентов, а в группе, которой назначали хлорамбуцил, отмечено 34 летальных случая среди 118 пациентов. Следует подчеркнуть, что показатель ОВ был лучше в группах пациентов, получавших терапию по схеме обинутузумаб + хлорамбуцил или ритуксимаб + хлорамбуцил, по сравнению с больными, у которых применяли монотерапию хлорамбуцилом, хотя многие пациенты, которым назначали монотерапию хлорамбуцилом, также получали лечение в рамках следующих линий терапии, включая химиоиммунотерапию (таблица).
Таблица. Последующие линии терапии, которые получали пациенты после лечения с применением схем обинутузумаб + хлорамбуцил, ритуксимаб + хлорамбуцил или хлорамбуцила
| Первая линия терапии | |||
| Обинутузумаб + хлорамбуцил, n (%) | Ритуксимаб + хлорамбуцил, n (%) | Хлорамбуцил, n (%) | |
| Пациенты в группе терапии | 333 (100) | 330 (100) | 118 (100) |
| Пациенты, которые получали хотя бы один новый тип лечения | 76 (23) | 117 (35) | 70 (59) |
| Последующие типы терапии, которые назначались пациентам | |||
| Флударабин + циклофосфамид или флударабин | 3 (1) | 8 (2) | 4 (3) |
| Флударабин + циклофосфамид или флударабин + ритуксимаб | 14 (4) | 20 (6) | 7 (6) |
| Флударабин + циклофосфамид или флударабин + офатумумаб | 0 (0) | 2 (1) | 0 (0) |
| Флударабин + циклофосфамид или флударабин + обинутузумаб | 0 (0) | 0 (0) | 0 (0) |
| Бендамустин | 10 (3) | 6 (2) | 3 (3) |
| Бендамустин + ритуксимаб | 17 (5) | 33 (10) | 18 (15) |
| Бендамустин + офатумумаб | 0 (0) | 0 (0) | 0 (0) |
| Бендамустин + обинутузумаб | 2 (1) | 1 (<1) | 0 (0) |
| Хлорамбуцил | 13 (4) | 12 (4) | 7 (6) |
| Хлорамбуцил + ритуксимаб | 2 (1) | 0 (0) | 2 (2) |
| Хлорамбуцил+ офатумумаб | 0 (0) | 0 (0) | 0 (0) |
| Хлорамбуцил+ обинутузумаб | 0 (0) | 0 (0) | 30 (25) |
| CHOP(-like) | 0 (0) | 3 (1) | 0 (0) |
| CHOP(-like) + ритуксимаб | 4 (1) | 3 (1) | 2 (2) |
| COP(-like) | 0 (0) | 3 (1) | 2 (2) |
| COP(-like) + ритуксимаб | 0 (0) | 6 (2) | 3 (3) |
| Ритуксимаб без химиотерапии | 8 (2) | 6 (2) | 0 (0) |
| Офатумумаб без химиотерапии | 1 (<1) | 4 (1) | 0 (0) |
| Обинутузумаб без химиотерапии | 0 (0) | 0 (0) | 0 (0) |
| Алемтузумаб без/с химиотерапией | 2 (1) | 6 (2) | 1 (1) |
| Экспериментальное лечение | 4 (1) | 12 (4) | 1 (1) |
| Другое | 3 (1) | 7 (2) | 3 (3) |
На основании полученных данных сделан вывод о том, что добавление какого-либо из моноклональных антител (ритуксимаба или обинутузумаба) в первой линии химиотерапии приводит к продлению жизни и влияет на течение ХЛЛ у пациентов пожилого возраста, что согласуется с результатами, полученными по показателю ОВ при проведении химиоиммунотерапии в исследованиях с участием молодых пациентов [10, 11]. В недавно опубликованном исследовании, в котором сравнивали офатумумаб в сочетании с хлорамбуцилом с монотерапией хлорамбуцилом в качестве первой линии терапии у пациентов пожилого возраста, также пока не сообщается о наличии статистически достоверного преимущества относительно ОВ при использовании химиоиммунотерапии [12], которое, однако, может быть отмечено при последующих анализах более поздних данных. Основываясь на полученных результатах, можно говорить о том, что химиоиммунотерапию с применением анти-CD20-антител следует рассматривать в качестве стандарта медицинской помощи у пациентов всех возрастных групп, ранее не получавших лечения по поводу ХЛЛ и нуждающихся в терапии. Тем не менее преимущества применения анти-CD20-антител в сочетании с новыми таргетными препаратами требуют в дальнейшем детального изучения [13–16]. Представленные результаты показывают, что оптимизация лечения с использованием новых или модифицированных анти-CD20-антител может иметь большой потенциал в терапии пациентов с ХЛЛ. В анализируемом исследовании [5] применение обинутузумаба вместо ритуксимаба в сочетании с хлорамбуцилом позволило увеличить медиану ВБП почти в 2 раза — практически до 30 мес. Наблюдения в рамках данного исследования продолжаются, в будущем ожидаются дальнейшие обновления данных ОВ для обинутузумаба по сравнению с другими режимами терапии.
Список использованной литературы
1. Жевак Т.Н., Чеснокова Н.П., Шелехова Т.В. (2011) Хронический лимфолейкоз: современные концепции этиологии, патогенеза и особенностей клинического течения (обзор). Саратовский научно-медицинский журнал, 7(2).
2. Patz M., Isaeva P., Forcob N. et al. (2011) Comparison of the in vitro effects of the anti-CD20 antibodies rituximab and GA101 on chronic lymphocytic leukaemia cells. Br. J. Haematol., 152: 295–306.
3. Mossner E., Brunker P., Moser S. et al. (2010) Increasing the efficacy of CD20 antibody therapy through the engineering of a new type II anti-CD20 antibody with enhanced direct and immune effector cell-mediated B-cell cytotoxicity. Blood, 115: 4393–4402.
4. Herter S., Herting F., Mundigl O. et al. (2013) Preclinical activity of the type II CD20 antibody GA101 (obinutuzumab) compared with rituximab and ofatumumab in vitro and in xenograft models. Mol. Cancer Ther., 12: 2031–2042.
5. Goede V., Fischer K., Busch R. et al. (2014) Obinutuzumab plus chlorambucil in patients with CLL and coexisting conditions. N. Engl. J. Med., 370: 1101–1110.
6. Goede V., Fischer K., Engelke A. et al. (2015) Obinutuzumab as frontline treatment of chronic lymphocytic leukemia: updated results of the CLL11 study. Leukemia, 29: 1602–1604.
7. Hallek M., Cheson B.D., Catovsky D. et al. (2008) Guidelines for the diagnosis and treatment of chronic lymphocytic leukemia: a report from the International Workshop on Chronic Lymphocytic Leukemia updating the National Cancer Institute-Working Group 1996 guidelines. Blood, 111: 5446–5456.
8. Parmelee P.A., Thuras P.D., Katz I.R., Lawton M.P. (1995) Validation of the Cumulative Illness Rating Scale in a geriatric residential population. J. Am. Geriatr. Soc., 43: 130–137.
9. Cockcroft D.W., Gault M.H. (1976) Prediction of creatinine clearance from serum creatinine. Nephron, 16: 31–41.
10. Hallek M., Fischer K., Fingerle-Rowson G. et al. (2010) Addition of rituximab to fludarabine and cyclophosphamide in patients with chronic lymphocytic leukaemia: a randomised, open-label, phase 3 trial. Lancet, 376: 1164–1174.
11. Tam C.S., O’Brien S., Wierda W. et al. (2008) Long-term results of the fludarabine, cyclophosphamide, and rituximab regimen as initial therapy of chronic lymphocytic leukemia. Blood, 112: 975–980.
12. Hillmen P., Robak T., Janssens A. et al. (2013) Ofatumumab + chlorambucil versus chlorambucil alone in patients with untreated chronic lymphocytic leukemia (CLL): results of the phase III study complement 1 (OMB110911). Blood, 122: 528.
13. Burger J.A., Keating M.J., Wierda W.G. et al. (2014) Safety and activity of ibrutinib plus rituximab for patients with high-risk chronic lymphocytic leukaemia: a single-arm, phase 2 study. Lancet Oncol., 15: 1090–1099.
14. Byrd J.C., Brown J.R., O’Brien S. et al. (2014) Ibrutinib versus ofatumumab in previously treated chronic lymphoid leukemia. N. Engl. J. Med., 371: 213–223.
15. Furman R.R., Sharman J.P., Coutre S.E. et al. (2014) Idelalisib and rituximab in relapsed chronic lymphocytic leukemia. N. Engl. J. Med., 370: 997–1007.
16. O’Brien S., Furman R.R., Coutre S.E. et al. (2014)Ibrutinib as initial therapy for elderly patients with chronic lymphocytic leukaemia or small lymphocytic lymphoma: an open-label, multicentre, phase 1b/2 trial. Lancet Oncol., 15: 48–58.














Leave a comment